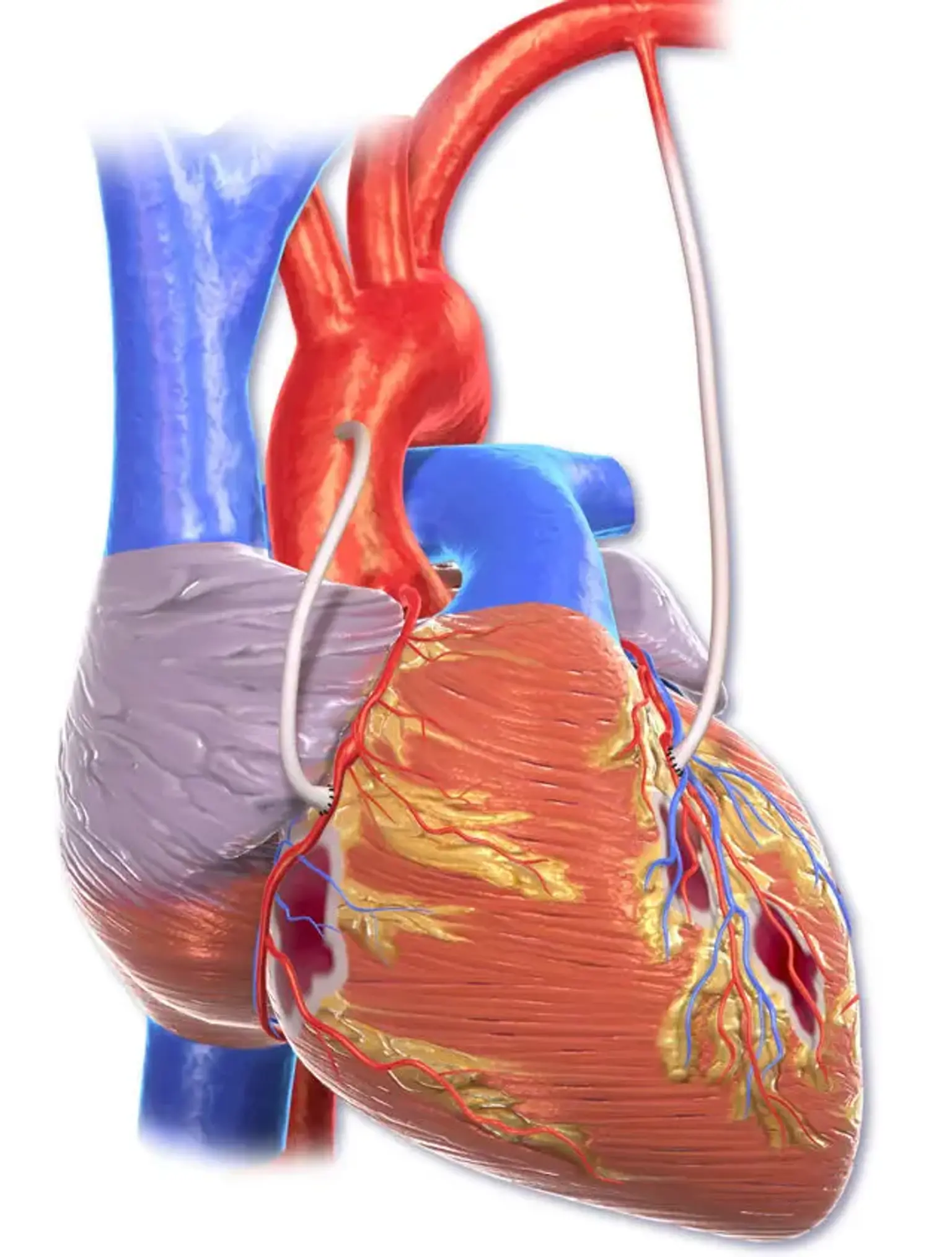
الكسب غير المشروع لتجاوز الشريان التاجي (CABG)
نظره عامه
CABG هو إجراء جراحي مهم يتم فيه تجاوز العوائق العضلية في الشرايين التاجية للمريض باستخدام القنوات الوريدية أو الشريانية التي يتم حصادها. يعيد الالتفافية تدفق الدم إلى عضلة القلب الإقفارية ، ويستعيد الوظيفة والجدوى ويخفف من أعراض الذبحة الصدرية.
يتم إجراء ما يقرب من 400000 عملية CABG كل عام ، مما يجعلها الجراحة الجراحية الكبرى الأكثر انتظاما ؛ ومع ذلك ، فقد تحولت الاتجاهات الجراحية حيث أصبحت الخيارات البديلة مثل العلاج الطبي والتدخل التاجي عن طريق الجلد (PCI) أكثر شعبية.
جراحة تحويل مسار الشريان التاجي
تطعيم مجازة الشريان التاجي (CABG) هو إجراء يستخدم لتحسين نوعية الحياة وتقليل الوفيات المرتبطة بالقلب لدى الأفراد المصابين بمرض الشريان التاجي (CAD). CAD هو أكبر سبب للوفاة في الولايات المتحدة والعالم الصناعي ، حيث يؤثر على 16.5 مليون بالغ أمريكي (تتراوح أعمارهم بين 20 عاما) كل عام.
وهي مسؤولة عن 530،989 حالة وفاة في الولايات المتحدة كل عام ، ومن المتوقع أن تؤثر العواقب طويلة الأجل ل CAD ، بما في ذلك ضعف البطين الأيسر وفشل القلب ، على ما يقرب من 8 ملايين شخص فوق سن 18 بحلول عام 2030.
تم إجراء جراحة CABG لأول مرة في 1960s بهدف توفير تخفيف الأعراض ، وتحسين نوعية الحياة ، وتعزيز متوسط العمر المتوقع لمرضى CAD. بالمقارنة مع العلاج الطبي ، زاد CABG معدلات البقاء على قيد الحياة في الأفراد الذين يعانون من مرض متعدد الأوعية الدموية وترك المرض الرئيسي بحلول 1970s.
يطلب نموذج علاج CAD الجديد نهج فريق القلب الذي يقوم فيه طبيب القلب وجراح القلب بتقييم تصوير الأوعية التاجية معا وتزويد المريض بأفضل بديل متاح لإعادة التوعي التاجي ، سواء كان ذلك زرع دعامة الشريان التاجي عن طريق الجلد أو CABG. في الوقت الحالي ، يكون مريض CABG العادي أكبر سنا ، وقد خضع لتدخل تاجي سابق عن طريق الجلد (PCI) ، ولديه أمراض مصاحبة أكثر بكثير.
على الرغم من هذه المخاطر ، لا يزال CABG أحد أهم العمليات الجراحية في تاريخ الطب الحديث ، بعد أن أنقذ على الأرجح المزيد من الأرواح وقدم تخفيفا أكبر للأعراض من أي جراحة كبرى أخرى. إن الأساليب الجديدة طفيفة التوغل ، والاختراقات في إدارة وحدة التخدير والعناية المركزة (ICU) ، والتقدم التكنولوجي تدفع حدود هذه العملية إلى آفاق جديدة.
بشكل عام ، هناك نوعان من الإجراءات الجراحية CABG: على المضخة وخارج المضخة ، مع الفرق هو أن CABG على المضخة يستخدم دائرة تحويل مسار المجازة القلبية الرئوية والقلب الموقوف للعمل. عادة ما يستخدم الشريان الثديي الداخلي الأيسر (LIMA) وطعوم الوريد الصافن (SVG) من الأطراف السفلية كقنوات تطعيم الالتفافية.
الشريان الثديي الداخلي الأيمن (RIMA) والشريان الكعبري والشريان المعدي الفوقي هي بعض القنوات الأخرى التي يمكن زرعها. يتم تحديد نوع وموضع الطعوم من خلال تشريح المريض وموقع الشرايين المسدودة. عادة ما يتم تطعيم LIMA إلى الشريان النازل الأمامي الأيسر (LAD) ، بينما يتم استخدام القنوات الأخرى للوصول إلى الشرايين المسدودة الأخرى.
علم التشريح وعلم وظائف الأعضاء
اثنين من الشرايين التاجية الرئيسية تزود عضلة القلب في القلب: الشريان التاجي الرئيسي الأيسر والشريان التاجي الأيمن (RCA). عادة ما يكون الشريان التاجي الرئيسي الأيسر قسما قصيرا ينقسم إلى الشرايين الأمامية اليسرى الهابطة (LAD) والشرايين المحيطة بها. ينقسم LAD إلى فروع قطرية ، في حين ينقسم الشريان المحيطي إلى فروع هامشية منفرجة. ينقسم RCA إلى فرعين: الشريان الهابط الخلفي (PDA) والفروع الهامشية.
اعتمادا على الشريان الذي يزود الحاجز بين البطينين و PDA ، يمكن تصنيف الدورة الدموية التاجية إلى أنظمة مهيمنة على اليسار واليمين ومهيمن مشترك. يزود الشريان المحيطي PDA في نظام مهيمن على اليسار ، في حين أن RCA يزود PDA في نظام مهيمن على اليمين. مع إمدادات الأوعية الدموية المهيمنة المشتركة ، يتم تغذية PDA بواسطة كل من RCA والشرايين المحيطة في نفس الوقت.
يؤدي الانسداد في أي من الشرايين التاجية إلى نقص مقابل في تروية عضلة القلب ، ونقص التروية ، وإذا ترك دون علاج يمكن أن يؤدي إلى احتشاء دائم أو تلف في القلب.
معلومات تاريخية
في عام 1912 ، حصل أليكسيس كاريل على جائزة نوبل في علم وظائف الأعضاء والطب لعمله. مكنته معرفته بالعلاقة بين الذبحة الصدرية وتضيق الشريان التاجي من مفاغرة جزء من الشريان السباتي من الشريان الأورطي الصدري الهابط إلى الشريان التاجي الأيسر في نموذج الكلاب.
قام آرثر فاينبرغ ، وهو جراح كندي بارز ، بزرع الشريان الصدري الداخلي الأيسر (الثديي) مباشرة في عضلة القلب في البطين الأيسر الأمامي في المرضى الذين يعانون من الذبحة الصدرية الشديدة في أواخر 1940s. والمثير للدهشة أن عددا قليلا من الأفراد كان لديهم انخفاض كبير في الأعراض نتيجة لهذه الجراحة.
أجرى سابستون أول عملية مخططة لتحويل مسار الوريد الصافن لإعادة الأوعية الدموية التاجية في جامعة ديوك في عام 1962. استخدم كوليسوف الشريان الصدري الداخلي الأيسر (الثديي) لتجاوز الشريان النازل الأمامي الأيسر دون مجازة قلبية رئوية في عام 1964 ، وكان كاربنتييه رائدا في استخدام طعوم الشريان الكعبري كقنوات CABG في عام 1973.
ازدهر CABG كعلاج وحيد ل CAD طوال 1970s وأوائل 1980s. انخفض عدد جراحات CABG التي أجريت مع تطوير وإدخال واعتماد واسع النطاق لدعامات الشريان التاجي عن طريق الجلد في 1980s و 1990s. ومع ذلك ، فإن العديد من التجارب متعددة المراكز التي تقارن CABG بالعلاج الحالي للدعامات ، قد أثبتت بوضوح مزايا CABG ، خاصة عندما يتم تضمين ميزات محددة للمريض مثل مرض السكري ، و CAD متعدد الأوعية ، واعتلال عضلة القلب الإقفاري.
مؤشرات ل CABG
عندما يكون هناك انسداد عالي الجودة في أي من الشرايين التاجية الرئيسية و / أو فشل التدخل التاجي عن طريق الجلد (PCI) في القضاء على الانسداد ، غالبا ما ينصح CABG. فيما يلي توصيات الفئة 1 من إرشادات ACCF/AHA لعام 2011:
- ترك المرض الرئيسي أكبر من 50 ٪
- مرض الشريان التاجي ثلاثي الأوعية الدموية بنسبة تزيد عن 70٪ مع أو بدون تورط LAD القريب
- مرض الأوعية الدموية: LAD بالإضافة إلى شريان رئيسي آخر
- تضيق شديد يزيد عن 70٪ في مريض يعاني من أعراض ذبحية كبيرة على الرغم من الحد الأقصى للعلاج الدوائي
- في أحد الناجين من الموت القلبي المفاجئ مع عدم انتظام دقات القلب البطيني المرتبط بنقص التروية ، كان أحد أمراض الأوعية الدموية أكثر من 70٪.
تشمل المؤشرات الأخرى ل CABG ما يلي:
- تعطيل الذبحة الصدرية (الفئة الأولى)
- نقص التروية الذي يستمر في سياق احتشاء عضلة القلب غير المرتفع للجزء ST (NSTEMI) الذي يكون مقاوما للعلاج الطبي (الفئة الأولى)
- ضعف وظيفة البطين الأيسر، ولكن عضلة القلب قابلة للحياة، لا تعمل فوق العيب التشريحي الذي يمكن إعادة توعيته.
- CAD شديد سريريا مع تضيق بنسبة 70 في المائة أو أعلى في واحد أو أكثر من الأوعية ، وكذلك الذبحة الصدرية الحرارية على الرغم من العلاج الدوائي و PCI
- CAD شديد سريريا بنسبة 70٪ أو أكثر من التضيق في 1 أو أكثر من الأوعية الدموية في الناجين من السكتة القلبية المفاجئة التي يعتقد أنها ناجمة عن عدم انتظام ضربات القلب البطيني الإقفاري
- CAD شديد سريريا مع تضيق بنسبة 50٪ أو أكثر في 1 أو أكثر من الأوعية الدموية في المرضى الذين يخضعون لجراحة القلب لأسباب أخرى (على سبيل المثال ، استبدال الصمام أو جراحة الأبهر)
يمكن إجراء CABG كعلاج طارئ في إعداد ارتفاع الجزء ST MI (STEMI) إذا لم يكن التدخل التاجي عن طريق الجلد (PCI) ممكنا أو إذا فشل PCI وكان هناك ألم طويل الأمد ونقص تروية يؤثر على جزء كبير من عضلة القلب على الرغم من العلاج الطبي.
تشمل العوامل التي تزيد من فائدة البقاء على قيد الحياة من CABG ما يلي:
- جزء طرد البطين الأيسر بنسبة 45٪ أو أقل
- داء السكري
- القلس التاجي الإقفاري
- فشل PCI ، مع أو بدون MI الحاد (AMI)
موانع
لا ينصح باستخدام CABG للأفراد الذين لا تظهر عليهم أعراض والذين هم في خطر منخفض من MI أو الوفاة. كما يتم استبعاد المرضى الذين سيستفيدون قليلا من إعادة التوعي التاجي.
على الرغم من أن سن الشيخوخة ليست موانع ، إلا أنه يجب التعامل مع CABG بحذر لدى كبار السن ، وخاصة أولئك الذين تزيد أعمارهم عن 85 عاما. هؤلاء الأفراد هم أيضا أكثر عرضة للإصابة بمشاكل في الفترة المحيطة بالجراحة بعد CABG. في المرضى الذين يعانون من CAD معقدة ، يعد نهج فريق القلب متعدد التخصصات الذي يركز على اتخاذ القرارات المشتركة أمرا بالغ الأهمية لتزويد المريض بأفضل فرصة لخطة إعادة التوعي الناجحة.
إجراء تحويل مسار الشريان التاجي
بالإضافة إلى تصوير الأوعية التاجية الذي اكتشف مرض الشريان التاجي ، سيحتاج المريض إلى اختبارات مختلفة أجريت استعدادا للجراحة. ستكون هناك حاجة إلى اختبارات معملية مثل تعداد الدم الكامل (CBC) ، ولوحات التمثيل الغذائي بما في ذلك اختبارات وظائف الكبد ، وألواح التخثر ، والهيموغلوبين A1c. قد تكون الاختبارات الأخرى ، بما في ذلك مخطط كهربية القلب (ECG) ، وتخطيط صدى القلب ، والتصوير بالموجات فوق الصوتية السباتية ، والأشعة السينية للصدر ، وربما رسم خرائط الصدر أو الوريد بالأشعة المقطعية للأطراف السفلية ، ضرورية.
لتجنب عدم انتظام ضربات القلب مثل الرجفان الأذيني ، غالبا ما يتم إعطاء الأدوية قبل الجراحة مثل حاصرات بيتا خلال الفترة المحيطة بالجراحة. في السابق ، تم حجب الأسبرين قبل 5 إلى 7 أيام من الجراحة ، ولكن يقترح الآن أن يبدأ أو يستمر قبل الجراحة.
عندما يصل المريض إلى المستشفى ، سيتم إنشاء الوصول عن طريق الوريد ، وسيتم فحص أدويته واختباراته قبل الجراحة. ستتم إزالة الشعر من مواقع الجراحة ، وسيتم إعطاء المريض حمام الكلورهيكسيدين.
معدات
لا تتطلب هذه الجراحة الجراحية الهامة المعدات اللازمة لمعظم العمليات الجراحية الأخرى فحسب ، بل تتطلب أيضا العديد من المعدات المتخصصة ، مثل آلة المجازة القلبية الرئوية مع جهاز تبريد سخان لتدفئة الدم وتبريده.
الافراد
يتم إجراء العملية من قبل فريق متخصص في جراحة القلب والأوعية الدموية مع تدريب مكثف وخبرة في رعاية هؤلاء المرضى المعقدين. يتكون الفريق من جراح القلب والصدر ومساعديهم وأطباء التخدير والممرضات والفنيين الجراحيين وأخصائيي التروية
تقييم المخاطر
ويجري تطوير نماذج المخاطر للتنبؤ بالوفيات لمدة 30 يوما بعد عزل CABG. أكثر المتنبئات استخداما في جراحة القلب هي نظام Euroscore ونموذج مخاطر جراحة القلب لعام 2008 الصادر عن جمعية جراحي الصدر (STS). العمر ، MI السابق ، PVD ، الفشل الكلوي ، حالة الدورة الدموية ، و EF كلها عوامل مشتركة في هذين النموذجين المتميزين. ثمانية من العوامل الأكثر صلة ، بما في ذلك العمر ، والحدة الجراحية ، وحالة إعادة الجراحة ، ومستوى الكرياتينين ، وغسيل الكلى ، والصدمة ، وأمراض الرئة المزمنة ، و EF ، تفسر 78 في المائة من التباين في نموذج STS.
التطبيب المسبق
يسعى التطبيب المسبق إلى تقليل احتياجات عضلة القلب من الأكسجين عن طريق خفض معدل ضربات القلب والضغط الشرياني الجهازي ، وكذلك لزيادة تدفق الدم في عضلة القلب باستخدام موسعات الأوعية. يجب تناول الأدوية التالية حتى وقت الجراحة:
- حاصرات بيتا، حاصرات قنوات الكالسيوم، والنترات
- اسبيرين
العوامل المدارة هي كما يلي:
- تيمازيبام على الفور قبل الجراحة
- ميدازولام، جرعة صغيرة عن طريق الوريد (IV) في غرفة العمليات قبل إدخال خط الشرايين
يجب أن يحصل كل مريض على 2 وحدة من الدم (للحالات الخفيفة) أو 6 وحدات من الدم والبلازما المجمدة الطازجة والصفائح الدموية المتطابقة (للحالات المعقدة). يمكن اعتبار حمض الترانيكساميك (1 غرام من البلعة قبل الشق الجراحي ، يليه تسريب 400 ملغ / ساعة أثناء الجراحة) لتقليل النزيف المنصفي بعد العملية الجراحية وكمية منتجات الدم اللازمة (أي خلايا الدم الحمراء والبلازما المجمدة الطازجة)
تخدير
عادة ما يتم إجراء جراحة القلب تحت التخدير العام العميق باستخدام أنبوب القصبة الهوائية. نادرا ما يستخدم النوعان التاليان من الحصار العصبي المحوري كمساعدين:
- ضخ المواد الأفيونية داخل القراب
- التخدير فوق الجافية الصدري (عادة ما يكون جرعة منخفضة من التخدير الموضعي / التسريب الأفيوني)
تقنيه
تبدأ العملية بعد أن يكون المريض في غرفة العمليات ويتم توصيله بالشاشات القياسية. قبل الحث على التخدير العام ، قد يدخل طبيب التخدير خطا شريانيا لمراقبة ضغط دم المريض بشكل غازي. بعد تحريض التخدير العام والتنبيب للمريض ، يمكن إدخال خط مركزي للوصول الوريدي وقسطرة الشريان الرئوي ، يليه إدخال محول صدى القلب عبر المريء.
قبل الشق الجراحي ، يتم إعداد المريض ولفه بشكل معقم ، ويتم إعطاء مهلة. يقوم الجراح بإجراء بضع القص الإنسي للتحضير لإزالة ليما لاستخدامها كقناة. يستخدم المساعد المدرب، أو عادة مساعد الطبيب أو المساعد الأول للممرضة أو جراح آخر، إجراءات مفتوحة أو بمساعدة الفيديو لإزالة الوريد الصافن من إحدى الساقين أو كلتيهما في نفس الوقت.
بعد الحصول على قنوات كافية ، يصف الجراح مضادات التخثر ، وغالبا ما يكون الهيبارين ، ليتم إعطاؤها استعدادا للمجازة القلبية الرئوية (CPB). يتم تعليب الشريان الأورطي وقلب المريض مركزيا ، ويتم توصيل الأنابيب بدائرة المجازة القلبية الرئوية. بعد بدء CPB ، يتم إيقاف القلب مع شلل القلب عالي البوتاسيوم بحيث يمكن للجراح مفاغرة القنوات التي تم حصادها إلى الشرايين التاجية البعيدة عن العوائق.
كقنوات لتطعيم مجازة الشريان التاجي ، يمكن استخدام الشرايين أو الأوردة (CABG). أثبت منشور رئيسي من كليفلاند كلينك مزايا البقاء على قيد الحياة لتطعيم الشريان الصدري الداخلي الأيسر (الثديي) إلى الشريان التاجي الأمامي الأيسر النازل منذ سنوات عديدة. هذا لا يزال صحيحا. في الواقع ، إن أمكن ، يوفر تطعيم الشريان الصدري الداخلي الثنائي (الثديي) فائدة كبيرة للبقاء على قيد الحياة على المدى الطويل. تظهر الأدلة القوية أن استخدام طعم شريان إضافي بدلا من الكسب غير المشروع الوريدي يرتبط بنتائج محسنة على المدى الطويل.
يعد الوريد الصافن الأكبر حجما ، وفي حالات نادرة ، الوريد الصافن القصير أكثر الطعوم استخداما في الوريد ، في حين أن الشريان الصدري الداخلي (الثديي) هو أكثر عمليات زرع الشريان استخداما. أعيد إدخال طعم الشريان الكعبري في الممارسة السريرية في 1990s ويستمر في إظهار معدلات المباح العالية بنسبة 80٪ أو أكثر بعد 10 سنوات من المتابعة ، خاصة إذا كان تضيق الأوعية الدموية المستهدف أكبر من 90٪.
الجانب السلبي لترقيع الوريد الصافن هو أن المباح ينخفض مع مرور الوقت: يتم حظر 10-20٪ بعد عام واحد من الجراحة بسبب الأخطاء الفنية والجلطة وتضخم التنسج الداخلي. 1-2 في المئة أخرى من ترقيع الأوردة تسد كل عام من 1 إلى 5 سنوات بعد الجراحة، و 4-5 في المئة أخرى تسد كل عام من 6 إلى 10 سنوات. يحدث انسداد الطعم الوريدي الذي يحدث بعد عام أو أكثر من CABG بسبب تصلب الشرايين في الوريد ، والذي يصاحبه تطور تضخم الحقم الوريدي.
فقط 50-60 ٪ من الطعوم الوريدية الصافنة هي براءة اختراع بعد 10 سنوات من الجراحة ، ونصفها فقط خال من تصلب الشرايين الوعائي. يجب على المرضى تناول الأدوية المضادة للصفيحات مدى الحياة ، وعادة ما تكون في شكل جرعة منخفضة يومية (81 ملغ) من الأسبرين ، كجزء من الوقاية الثانوية المناسبة.
تحافظ طعوم الشريان الصدري الداخلي (الثديي) ، على عكس ترقيع الوريد الصافن ، على المباح طوال الوقت. أكثر من 90٪ من ترقيع الشريان الصدري الداخلي (الثديي) لا تزال براءة اختراع بعد 10 سنوات. عندما يتم تجاوز الشريان التاجي الأمامي الأيسر ، يجب استخدام الشريان الصدري الداخلي الأيسر (الثديي) كقناة.
ترتبط القنوات ب ostia الجديدة المتولدة في الشريان الأورطي القريب بعد أن يقوم الجراح بمفاغرة الأجزاء البعيدة. ثم يتم شطف الشلل القلبي بعيدا ، ويبدأ القلب في الانقباض ، وقد يقوم الجراح بفحص الطعوم لتدفق الدم والكفاءة ، وكذلك النزيف من مواقع المفاغرة. ثم يتم إغلاق الصدر بأسلاك قصية ، ويتم نقل المريض إلى وحدة الرعاية الحرجة لمراقبة استقرار الدورة الدموية وإخراجها.
التعقيدات
السكتة الدماغية ، وعدوى الجروح ، وفشل الكسب غير المشروع ، والفشل الكلوي ، والرجفان الأذيني بعد العملية الجراحية ، والوفيات كلها عواقب محتملة ل CABG. تم الإبلاغ عن معدل السكتة الدماغية بعد CABG يتراوح بين 1٪ و 2٪ ، اعتمادا على ميزات المريض وعوامل الخطر للسكتة الدماغية ، والتي تشمل العمر المتقدم ، والسكتة الدماغية السابقة ، وتصلب الشرايين الأبهري ، ومرض الشريان المحيطي ، والرجفان الأذيني في الفترة المحيطة بالجراحة ، والسكري.
تبلغ معدلات الإصابة بالجرح القصي حوالي 1٪ وتتأثر بمتغيرات الخطر مثل السمنة والسكري ومرض الانسداد الرئوي المزمن (COPD) وطول العملية.
من المرجح أن يكون فشل ترقيع الوريد الصافن (SVG) في غضون 30 يوما بعد الجراحة ويحدث بسبب العديد من الأسباب مثل حجم الوريد وطوله المفرط ، والجريان السطحي البعيد وضعف التدفق ، وفرط التخثر والجلطة. مع تكرار تصوير الأوعية بعد CABG ، شوهدت معدلات فشل SVG تصل إلى 25٪. بدلا من ذلك ، تستمر الطعوم الشريانية مثل الشريان الثديي الداخلي الأيسر (LIMA) والطعوم الشريانية الشعاعية لفترة أطول ولها معدلات مباحية تصل إلى 90٪ بعد 10 سنوات.
تختلف معدلات الفشل الكلوي بعد العملية الجراحية بعد CABG من 2٪ إلى 3٪ ، مع 1٪ بحاجة إلى غسيل الكلى. أمراض الكلى قبل الجراحة ، والشيخوخة ، والسكري ، ونوع الجراحة ، وخلل LV ، والصدمة كلها عوامل خطر. على الرغم من أنه لم يثبت بالتأكيد أن أي أدوية تقلل من معدلات القصور الكلوي الناجم عن CABG ، إلا أن CABG خارج المضخة قد يقدم فائدة على CABG على المضخة.
الرجفان الأذيني خلال أول 5 أيام بعد CABG متكرر إلى حد ما ، مع معدلات تتراوح من 20 ٪ إلى 50 ٪ ، ويرتبط بزيادة المراضة ، بما في ذلك زيادة خطر الإصابة بالسكتة الدماغية الانصمام والوفاة. وقد ثبت أن الاستراتيجية الأكثر فعالية لتقليل حدوث الرجفان الأذيني بعد العملية الجراحية هي العلاج قبل الجراحة مع حاصرات بيتا وربما الأميودارون.
يختلف خطر الوفاة في الفترة المحيطة بالجراحة بعد إجراء عملية تحويل مسار الشريان التاجي وفقا للمراضة المصاحبة ، وإلحاح الجراحة ، وحجم حالة المرفق الذي يتم فيه إجراء العملية ، والتي تتراوح من 1٪ إلى 2٪.
نتائج
وفقا لتحليل تلوي لست تجارب سريرية عشوائية شملت 6055 مريضا من عصر التطعيم الشرياني والدعامات ، فإن تطعيم مجازة الشريان التاجي (CABG) يؤدي إلى انخفاض في الوفيات طويلة الأجل واحتشاء عضلة القلب (MIs) بالإضافة إلى انخفاض في عمليات إعادة التوعي المتكررة في المرضى الذين يعانون من مرض الشريان التاجي متعدد الأوعية ، بغض النظر عما إذا كان المرضى مصابين بالسكري أم لا.
وجد تحليل تلوي لثماني تجارب عشوائية شملت 3612 مريضا بالغا يعانون من مرض السكري ومرض الشريان التاجي متعدد الأوعية (CAD) أن CABG قلل من خطر الوفاة لجميع الأسباب بنسبة 33٪ بعد 5 سنوات بالمقارنة مع PCI. عندما تمت مقارنة المرضى الذين لديهم CABG بمجموعات فرعية من المرضى الذين حصلوا إما على دعامات معدنية عارية أو دعامات مضادة للعقاقير ، لم يختلف الانخفاض النسبي في المخاطر بشكل كبير.
المرضى الذين تتراوح أعمارهم بين 51 و 70 عاما وأولئك الذين تزيد أعمارهم عن 70 عاما والذين تلقوا CABG خلال نفس الفترة الزمنية كان أداؤهم أسوأ بكثير من حيث البقاء على قيد الحياة. كانت أمراض الكلى المزمنة أو جزء طرد البطين الأيسر المنخفض أو أمراض الأوعية الدموية الطرفية أو مرض الانسداد الرئوي المزمن عوامل الخطر الرئيسية للوفاة الناجمة عن جميع الأسباب.
خلصت دراسة العلاج الجراحي لفشل القلب الإقفاري (STICH) (STICHES) إلى أن معدلات الوفاة من أي سبب ، والوفاة من أسباب القلب والأوعية الدموية ، والوفاة من أي سبب أو دخول المستشفى لأسباب القلب والأوعية الدموية كانت أقل بكثير في المرضى الذين خضعوا ل CABG وتلقوا الرعاية الطبية.
علاوة على ذلك ، كان هناك تباين كبير على مستوى المستشفى في معدلات STEMI CABG ، وكثيرا ما تم إجراء CABG في غضون 1-3 أيام من تصوير الأوعية. المرضى الذين تلقوا CABG وأولئك الذين لم يكن لديهم معدلات وفيات مماثلة في المستشفى.
وجد تحليل تلوي ل 6637 مريضا يعانون من CAD الرئيسي الأيسر غير المحمي من تسع تجارب على مدى فترة 14 عاما (2003-2016) أن PCI مع دعامات التخلص من الأدوية كان مرتبطا بوفيات قلبية وأسباب مماثلة ولكن انخفاض معدلات السكتة الدماغية ومعدلات أكبر من إعادة التوعي المتكرر. بالنسبة للأحداث القلبية والدماغية الوعائية الضارة الكبيرة ، لم يحقق الاتجاه الذي يفضل CABG مقابل PCI أهمية إحصائية.
من حيث نوعية الحياة بعد CABG مقابل PCI ل CAD متعدد الأوعية ، يعمل كلا الإجراءين على تحسين تواتر الذبحة الصدرية. ومع ذلك ، في 1 شهر بعد الإجراء ، يميل مرضى PCI إلى التعافي بشكل أسرع ولديهم حالة صحية أفضل على المدى القصير من مرضى CABG ، ولكن في 6 أشهر وأطول بعد الإجراء ، يبدو أن مرضى CABG لديهم تخفيف أفضل للذبحة الصدرية ونوعية الحياة من مرضى PCI.
استنتاج
الطعم الالتفافي للشريان التاجي (CABG) هو تقنية جراحية تستخدم لعلاج أمراض القلب التاجية بهدف تحسين نوعية الحياة وخفض الوفيات المرتبطة بالقلب. يعيد توجيه الدم حول الأجزاء الضيقة أو المسدودة من الشرايين الرئيسية ، مما يزيد من تدفق الدم وتوصيل الأكسجين إلى القلب.