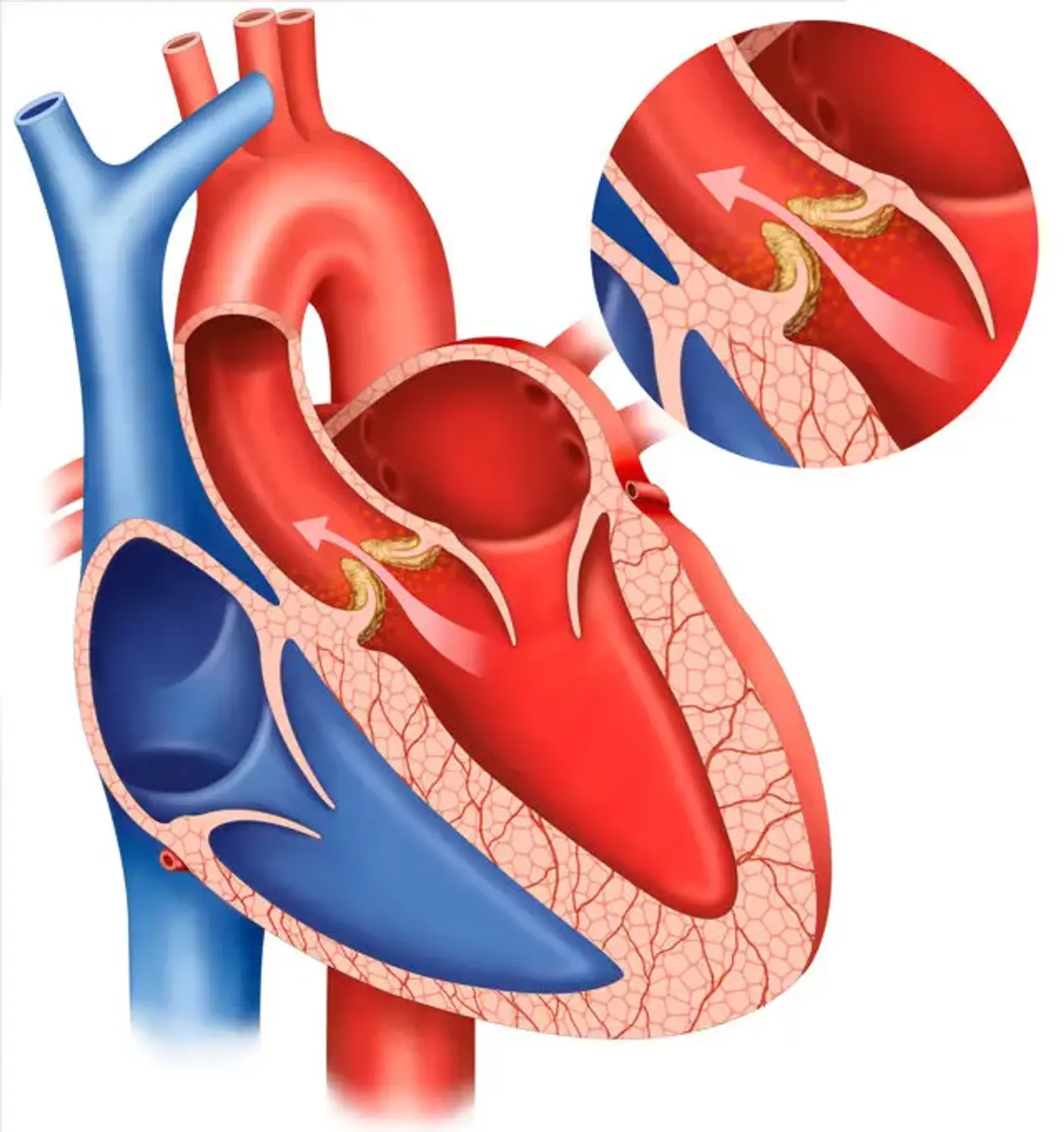
Aortenklappenersatz (AVR)
Überblick
Aortenklappeninsuffizienz (AVR) ist definiert als diastolischer Aortenblutrückfluss in den linken Ventrikel (LV). Akute AR ist durch signifikante Lungenödeme und Hypotonie gekennzeichnet und gilt als chirurgischer Notfall. Chronisch schwere AVR führt zu einer Kombination aus LV-Volumen und Drucküberlastung. Es wird von systolischer Hypertonie und breitem Pulsdruck begleitet, die periphere körperliche Symptome wie gebundene Impulse erklären.
Systolische Hypertonie verursacht eine Erhöhung der Nachlast, was zu progressiver LV-Dilatation und systolischer Dysfunktion führt. Die Echokardiographie ist der bedeutendste diagnostische Test für AVR. Es ermöglicht die Bestimmung der AVR-Quelle sowie des Schweregrads von AR und seiner Auswirkungen auf LV-Größe, Funktion und Hämodynamik.
Viele Menschen mit chronischer schwerer AVR können jahrelang mit normaler LV-Funktion und ohne Symptome leben. Diese Personen benötigen keine Operation, aber sie sollten engmaschig auf das Auftreten von Symptomen oder LV-Dilatation / Dysfunktion überwacht werden. Bevor die LV-Ejektionsfraktion unter 55% fällt oder die LV-enddiastolische Dimension 55 mm erreicht, sollte eine Operation in Betracht gezogen werden.
Sofern keine signifikanten Komorbiditäten oder andere Kontraindikationen vorliegen, sollten symptomatische Personen operiert werden. Das Hauptziel der vasodilatatorbasierten medikamentösen Behandlung ist es, die Operation bei asymptomatischen Patienten mit normaler LV-Funktion zu verschieben oder Patienten zu behandeln, für die eine Operation nicht möglich ist.
Der Zweck der vasodilatatorischen Behandlung besteht darin, den systolischen arteriellen Druck signifikant zu senken. Zukünftige Therapeutika könnten sich auf molekulare Wege konzentrieren, um LV-Remodeling und Fibrose zu vermeiden.
Epidemiologie der AVR
Die Häufigkeit chronischer AVR und das Auftreten akuter AVR sind noch unbekannt. Selbst bei gesunden Personen ist die Rückverfolgung von AVR durch Echokardiographie eine häufige Beobachtung. Es scheint Männer mehr zu betreffen als Frauen (13 Prozent vs. 8,5 Prozent). Die AVR-Prävalenz steigt mit dem Alter und ist am häufigsten nach dem 50. Lebensjahr. Die Häufigkeit von AVR in den Vereinigten Staaten wird auf 4,9 bis 10% geschätzt.
Wie entwickelt sich AVR und verursacht klinische Symptome?
AVR induziert eine Zunahme des Volumens des linken Ventrikels. Eine Zunahme des enddiastolischen LV-Volumens führt zu LV-Dilatation und exzentrischer Hypertrophie. Dadurch kann ein höheres Hubvolumen ausgeworfen werden. Das gesamte Schlagvolumen, das von der LV bei AVR-Patienten ausgestoßen wird, ist die Summe aus dem effektiven Schlagvolumen und dem Regurgitantvolumen. Infolgedessen ist AVR mit einer höheren Vorspannung verbunden. Nach Laplaces Regel erhöht die LV-Dilatation die systolische LV-Spannung. Dies, zusammen mit dem höheren systolischen Blutdruck, der durch die Erhöhung des gesamten Vorwärtshubvolumens verursacht wird, führt zu einer größeren Nachlast.
Die Kombination von LV-Dilatation und Hypertrophie kompensiert die LV-Funktion. Im Laufe der Zeit kann die Wandverdickung jedoch nicht mit der hämodynamischen Belastung Schritt halten, was zu einer Abnahme der systolischen Funktion und der Ejektionsfraktion führt.
Die LV dekompensiert, was zu einer verminderten Compliance und einem höheren enddiastolischen LV-Druck und -Volumen führt. Der linke Vorhof, der Lungenarterienkeil, der pulmonale arterielle, der rechtsventrikuläre (RV) und der rechte Vorhofdruck steigen mit fortschreitender Krankheit an, aber das effektive (vorwärts) Herzzeitvolumen nimmt ab. Aufgrund einer Lungenstauung treten Symptome einer Herzinsuffizienz wie Dyspnoe, Orthopnoe und paroxysmale nächtliche Dyspnoe auf.
Eine größere LV-Masse erfordert einen erhöhten myokardialen Sauerstoffverbrauch. Zusätzlich wird der koronare Perfusionsdruck gesenkt. Myokardischämie und Belastungsbeschwerden in der Brust resultieren daraus.
Die Kompensationsmechanismen der LV entwickeln sich bei Personen mit akuter schwerer AR nicht schnell genug, um die regurgitierende Volumenbelastung aufzunehmen. Ein schneller Anstieg des diastolischen LV-Drucks kann zu einem abrupten Lungenödem und einem kardiogenen Schock führen. Infolge des abrupten akuten Anstiegs des LV-Volumens und -Drucks kann sich sogar eine diastolische Mitralinsuffizienz entwickeln.
Was sind die möglichen Ursachen für AVR?
AR wird durch Fehlkoaptation der Aortenblättchen verursacht, die durch Anomalien in den Aortenblättchen, ihren Stützstrukturen wie Aortenwurzel und Annulus oder beidem verursacht wird.
Primäre Klappenerkrankung:
Häufige Ursachen sind kalzifische Aortenklappenerkrankungen, die normalerweise mit Aortenstenose (AS) assoziiert sind, aber mit einem gewissen Grad an AR assoziiert sein können; infektiöse Endokarditis, die die Anatomie der Blättchen verändert; und ein Riss oder eine Platzwunde in der aufsteigenden Aorta, die zu einem Aortenhöckerprolaps aufgrund des Verlusts der Kommissurstütze führt.
AR kann durch eine angeborene bikuspide Aortenklappe (BAV) aufgrund eines unzureichenden Verschlusses oder Prolaps der Klappe verursacht werden, während AS eine häufigere Folge von BAV ist. Weniger häufige Ursachen für angeborene AR sind unikommissurale und quadricuspidale Klappen sowie fenestrierte Klappenrupturen.
Aortenhöckerprolaps entwickelt sich bei bestimmten Menschen mit Ventrikelseptumdefekt (VSD). Rheumatische Erkrankungen verursachen eine fibröse Infiltration der AV-Höcker, die eine Retraktion verursacht und die normale Öffnung während der Systole und den Verschluss während der Diastole verhindert. Die Verschmelzung der Kommissuren kann zu gemischten AS und AVR führen. Die rheumatische Mitralklappenerkrankung geht häufig mit einer rheumatischen Aortenklappenerkrankung einher.
Progressive AVR kann auch durch myxomatöse Aortenklappendegeneration verursacht werden. Sekundäre AVR können durch Verdickung und Vernarbung der AV-Blättchen entstehen, die durch membranöse Subaortenstenose verursacht werden. AVR wurde auch als Komplikation der perkutanen Aortenballonvalvotomie und des Transkatheter-Aortenklappenersatzes dokumentiert.
Klappen-AVR wird aufgrund des strukturellen Abbaus einer bioprothetischen Klappe immer häufiger. Aortenhöckeravulsion oder -ruptur ist eine seltene Ursache für akute AVR. Andere weniger häufige Ursachen von AVR sind systemischer Lupus erythematodes, Takayasu-Krankheit, Whipple-Krankheit, rheumatoide Arthritis, ankylosierende Spondylitis, Jaccoud-Arthropathie, Syphilis, Morbus Crohn und appetitzügelnde Medikamente.
Primäre Aortenwurzelerkrankung:
Die ringförmige Erweiterung der Aorta bewirkt, dass sich die AV-Blättchen trennen, was zu AVR führt. Altersbedingte Veränderungen, zystische mediale Nekrose, die häufig mit dem Marfan-Syndrom verbunden ist, oder Osteogenesis imperfecta können degenerative Veränderungen in der Aortenwurzel hervorrufen. Ankylosierende Spondylitis, Behcet-Krankheit, Psoriasis-Arthritis, Arthritis im Zusammenhang mit reaktiver Arthritis, Colitis ulcerosa, schubförmige Polychondritis und Riesenzellarteriitis sind alle mit Aortenwurzelerweiterung verbunden.
Schwere, chronische systemische Hypertonie kann den Aortenring erweitern, wodurch AVR fortschreitet. Eine retrograde Aortendissektion kann den Aortenringus einschließen und stören, was zu AVR führt.
Was sind die Symptome und körperlichen Anzeichen bei Patienten mit AVR?
Nach Anamnese:
Chronische AVR-Symptome treten allmählich auf, manchmal über Jahrzehnte. Belastungsdyspnoe, Orthopnoe, paroxysmale nächtliche Dyspnoe, Angina pectoris, Herzklopfen und Kopfklopfen sind alle Symptome. Nächtliche Angina tritt auf, wenn sich der Herzschlag während des Schlafes verlangsamt, was dazu führt, dass der arterielle diastolische Druck auf gefährlich niedrige Werte sinkt.
Durch körperliche Untersuchung:
Als Folge der systolischen Hypertonie und des reduzierten diastolischen Drucks ist AVR mit einem erweiterten Pulsdruck verbunden. Der apikale LV-Impuls ist hyperdynamisch und lateral und minderwertig verschoben. Ein starker systolischer Nervenkitzel kann in der Nähe der Basis des Herzens, der suprasternalen Kerbe und oberhalb der Halsschlagadern gefühlt werden. Die riesigen Vorwärtshubvolumina und der niedrige diastolische Druck der Aorta induzieren es.
S1 ist normal, während S2 entweder angehoben (weil zu einer erweiterten Aortenwurzel) oder abgesenkt wird (wenn die Aortenblättchen verdickt sind). Ein hochfrequentes, geblasenes, dekrescendo-diastolisches Rauschen ist am besten in der dritten Interkostallücke an der linken Brustbeingrenze zu hören. Das Geräusch von AR ist gegen Ende des Ablaufs leichter zu erkennen, wenn sich der Patient nach vorne lehnt.
Das Geräusch nimmt mit hockender oder isometrischer Aktivität zu und nimmt mit blutdrucksenkenden Verfahren ab. Bei moderater AVR ist dieses Geräusch früh diastolisch und schreitet zu holodiastolisch mit schwerer AVR fort.
Periphere Anzeichen einer schweren chronischen AVR-Folge eines erweiterten Pulsdrucks werden im Folgenden beschrieben:
- Austin Flint murmelt: Leises Grollen in der Mitte des diastolischen Gemurmels hört man am besten an der Spitze. Es wird angenommen, dass es durch einen vorzeitigen Verschluss der Mitralklappe aufgrund des AR-Jets verursacht wird.
- Becker-Zeichen: Vorhandensein einer sichtbaren Pulsation der Netzhautarterien durch ein Ophthalmoskop
- Bisferien Puls: Biphasischer Puls aufgrund des Rückflusses von Blut in der frühen Diastole
- Corrigan-Zeichen: Wasserschlagpuls mit abrupter Dehnung und schnellem Kollaps.
- de Musset Zeichen: Kopfwippen mit jeweils arterieller Pulsation.
- Duroziez Zeichen: Systolisches Geräusch über der Oberschenkelarterie, wenn es proximal komprimiert wird, und ein diastolisches Geräusch, wenn es distal mit einem Stethoskop komprimiert wird.
- Gerhardt-Zeichen: Pulsationen der Milz werden in Gegenwart von Splenomegalie nachgewiesen.
- Hügelzeichen: Blutdruck in der unteren Extremität ist größer als Blutdruck in der oberen Extremität
- Mayne-Zeichen: Abfall des diastolischen Blutdrucks von mehr als 15 mmHg beim Anheben des Arms
- Müller-Zeichen: Systolische Pulsation des Zäpfchens
- Quincke-Zeichen: Kapillarpulsation (Spülung und Blass am besten an der Nagelwurzel, wenn Druck auf die Nagelspitze ausgeübt wird).
- Rosenbach-Zeichen: Pulsation der Leber
- Traube-Schild: Dröhnende "pistolenschüssige" systolische und diastolische Klänge über der Oberschenkelarterie
- Es sollte beachtet werden, dass diese namensgebenden Zeichen unterschiedliche Empfindlichkeiten und Besonderheiten aufweisen. Die Evidenz über den Einfluss der Schwere der Aorteninsuffizienz auf die Manifestation dieser Anzeichen ist spärlich.
Bei akuter AVR hängen Symptome und körperliche Befunde mit einem verminderten Schlaganfallvolumen zusammen. Die Patienten zeigen Tachykardie, Tachypnoe und Lungenödem. Da die körperlichen Untersuchungsbefunde der akuten AR subtiler sind als die der chronischen AR, ist die Diagnose schwierig zu stellen, wenn ein Patient mit Dyspnoe und Schock auftritt. Ein hoher Verdachtsindex ist für eine schnelle Diagnose unerlässlich.
Wie wird AVR ausgewertet und diagnostiziert?
Die Aufarbeitung der Aorteninsuffizienz umfasst die folgenden Tests.
- Echokardiographie
Die primäre diagnostische Technik ist die Echokardiographie, die eine genaue Beurteilung der Aortenklappenarchitektur, der Aortenwurzelanatomie und der LV liefert.
Chronische AVR ist durch linksventrikuläre Dilatation gekennzeichnet. Bis zu späteren Phasen ist die systolische Funktion normal, wie ein Abfall der EF oder eine Zunahme der endsystolischen Dimension zeigt.
Bei schwerer AVR beträgt die zentrale Strahlbreite mehr als 65 % des LV-Ausflusstrakts (LVOT), das Regurgitantvolumen beträgt 60 ml / Schlag, die effektive Regurgitantöffnungsfläche ist größer als 0,30, die Regurgitantfraktion beträgt 50%, die Vena contracta ist größer als 0,6 cm und es gibt eine diastolische Flussumkehr in der proximalen absteigenden thorakalen Aorta.
Bei Personen mit schwerer AVR zeigt das kontinuierliche Dopplerprofil des AVR-Jets eine schnelle Verzögerungszeit an. Eine hohe Steigung bedeutet, dass sich der Druck zwischen Aorta und LV während der Diastole schneller ausgleicht.
Sowohl bei akuten als auch bei chronischen AVR kann ein hochfrequentes diastolisches Flattern des vorderen Mitralblattes beobachtet werden, das durch den Aufprall des regurgitierenden Jets verursacht wird.
Eine transthorakale 2-dimensionale und M-Mode-Echokardiographie (TTE) und / oder ein transösophageales Echokardiogramm (TEE) am Krankenbett können zur Diagnose einer akuten AR (TE) verwendet werden.
- Kardiale Magnetresonanz
Die kardiale MRT (CMR) ist eine alternative diagnostische Methode, die besonders bei Personen nützlich ist, die trotz Echokardiographie aufgrund unzureichender akustischer Fenster eine weitere Beurteilung benötigen. Es ist die präziseste nichtinvasive Methode zur Bestimmung des LV-endsystolischen Volumens, des diastolischen Volumens und der Masse. Die antegraden und retrograden Strömungsvolumina in der aufsteigenden Aorta können verwendet werden, um den Schweregrad der AVR genau abzuschätzen.
- Herzkatheterisierung
Wenn es eine Unstimmigkeit zwischen der klinischen Präsentation und der nichtinvasiven Bildgebung gibt, kann die Angiographie Informationen über den Schweregrad von AVR, Hämodynamik und Koronararterienarchitektur liefern. Dabei wird schnell Kontrastmittel in die Aortenwurzel injiziert und die rechte und linke vordere Schrägprojektion aufgezeichnet.
Wie wird AVR behandelt?
Akute AVR:
Eine Notfalloperation wird bei schwerer akuter AVR empfohlen. Die medizinische Behandlung ist eingeschränkt und wird nur zur kurzzeitigen Stabilisierung des Patienten eingesetzt. Um den Vorwärtsfluss zu verbessern, werden intravenöse Diuretika und Vasodilatatoren (wie Natriumnitroprussid) verwendet, um die Nachlast zu reduzieren. Zur Verbesserung des Herzzeitvolumens können Inotrope wie Dopamin oder Dobutamin verwendet werden. Betablocker werden vermieden, da sie CO senken und die Herzfrequenz verlangsamen, wodurch die LV mehr Zeit für die diastolische Füllung hat. Eine intraaortale Ballongegenpulsation wird nicht empfohlen.
Die Operation kann bei Patienten mit akuter AVR verschoben werden, die durch aktive infektiöse Endokarditis verursacht werden und 5 bis 7 Tage nach Beginn der Antibiotika hämodynamisch stabil waren. Wenn jedoch eine hämodynamische Instabilität oder Abszessentwicklung auftritt, muss das Verfahren durchgeführt werden.
Chronische AVR:
Überwachung während des gesamten Krankheitsverlaufs: Asymptomatische Personen mit leichter oder mittelschwerer AVR und normaler Herzgröße sollten alle 12 oder 24 Monate klinisch und echokardiographisch untersucht werden. Asymptomatische Patienten mit persistierender schwerer AVR und normaler LV-Funktion sollten alle 6 Monate untersucht werden.
Medizinische Therapie: Es gibt nur wenige Indikationen für eine medizinische Behandlung bei AVR. Vasodilatator-Behandlung sollte verwendet werden, um systemische arterielle Hypertonie im Zusammenhang mit chronischer AVR zu behandeln. Es ist bevorzugt, Dihydropyridin-Kalziumkanalblocker oder Angiotensin-Converting-Enzym-Inhibitoren/Angiotensin-Rezeptorblocker (ACEIs/ARBs) zu verwenden.
- Staging der chronischen AR: Chronische AR wird in 4 Stufen eingeteilt, basierend auf der ACC/AHA-Leitlinie 2020 für die Behandlung von Patienten mit Herzklappenerkrankungen:
- Stufe A: Patienten mit einem Risiko für AR. Diese Patienten haben keine hämodynamischen Folgen oder Symptome.
- Stufe B: Progressive AR. Patienten haben eine leichte bis mittelschwere AR, aber eine normale systolische LV-Funktion und keine klinischen Symptome.
- Stufe C: Asymptomatische schwere AR. Die Patienten haben eine AR-Jetbreite von mindestens 65% des linksventrikulären Ausflusstrakts (LVOT). Stadium C wird in Abhängigkeit von der systolischen LV-Funktion weiter unterteilt als:
- C1: Normale LVEF (>50%) und leichte bis mäßige LV-Dilatation (LVESD <50 mm).
- C2: Reduzierte LVEF (<50%) mit schwerer LV-Dilatation (LVESD >50 mm).
- Stufe D: Symptomatische schwere AR. Befunde eines schweren AR-Jets auf Echokardiographie. Es kann entweder normale oder abnormale LVEF haben. Symptome sind Belastungsdyspnoe, Angina pectoris oder Herzinsuffizienz.
Chirurgische Behandlung: Die Behandlungsrichtlinien für AR basieren auf den Empfehlungen der American Heart Association / American College of Cardiology aus dem Jahr 2020. Aortenklappenersatz (AVR) ist die bevorzugte Therapie für Personen mit schwerer symptomatischer chronischer AR und schwerer asymptomatischer chronischer AVR mit LV-systolischem Versagen (LVEF 50 Prozent).
AVR ist auch eine praktikable Wahl für Personen mit schwerer AVR, die asymptomatisch sind und eine normale LV-Funktion (LVEF 50 Prozent) haben, aber eine erhebliche LV-Dilatation aufweisen (LVESD-Index >25 mm / m2 oder LVESD >50 mm).
AVR kann auch für Patienten mit schwerer AVR untersucht werden, die asymptomatisch sind und eine normale systolische LV-Funktion in Ruhe haben (LVEF 50 Prozent, Stadium C1), aber angesichts des minimalen chirurgischen Risikos des Eingriffs eine zunehmende signifikante LV-Dilatation (LV-enddiastolische Dimension >65 mm) aufweisen.
Trotz der Tatsache, dass die Leitlinien eine Herzklappenoperation empfehlen, wenn sich Symptome, linksventrikuläre systolische Dysfunktion oder linksventrikuläre Dilatation entwickeln, stellen neuere Studien, die Hinweise auf subklinische myokardiale Dysfunktion und irreversible Myokardfibrose bei Patienten mit chronischer AR zeigen, die aktuellen Empfehlungen zum Zeitpunkt der Intervention in Frage.
Prognose der AVR
Akute AVR:
Das operative Risiko bei akuter schwerer Aorteninsuffizienz ist signifikant höher als bei chronischer schwerer Aorteninsuffizienz. Patienten mit akuter AVR haben oft erschwerende Zustände wie infektiöse Endokarditis oder ein sezierendes Aneurysma, was ihre Prognose reduziert.
Chronische AVR:
Auch wenn die AVR schwerwiegend ist, ist eine asymptomatische chronische AVR häufig mit einer allgemein positiven Prognose für viele Jahre verbunden. Quantitative Messungen des AVR-Schweregrads sowie der LV-Größe und der systolischen Funktion sind gute Prädiktoren für die klinische Prognose. Wenn die LV-Dysfunktion früh entdeckt wird, bevor die EF signifikant sinkt, bevor die LV-Dilatation erfolgt und bevor Symptome auftreten, ist es wahrscheinlicher, dass sie reversibel ist. Eine Operation ist erforderlich, bevor dauerhafte Veränderungen auftreten, da die Operation die Herztodrate bei Hochrisikopersonen verbessert.
Wenn ein AVR-Patient symptomatisch wird, verschlechtert sich sein Zustand schnell. Herzinsuffizienz, akutes Lungenödem und abrupter Tod sind alle Möglichkeiten. Nur 30% der Personen mit NYHA Klasse III oder IV Symptome überleben vier Jahre ohne Operation.
Komplikationen von AVR
Die frühen Stadien der chronischen AR sind subklinisch und es gibt möglicherweise keine Anzeichen oder Symptome. Wenn die Krankheit jedoch fortschreitet, hat sie Auswirkungen auf die Herzhämodynamik und -funktion. Es kann progressive linksventrikuläre systolische Dysfunktion, kongestive Herzinsuffizienz, ischämische Kardiomyopathie, Arrhythmie und möglicherweise abrupten Tod verursachen. Bei Personen mit kongestiven Symptomen oder Belastungsintoleranz überwiegen die Vorteile einer Operation die Gefahren; Folglich ist eine Klappenoperation gut gerechtfertigt, um Probleme zu vermeiden.
Schlussfolgerung
Die Aortenklappeninsuffizienz (AVR) ist eine Herzklappenerkrankung, die durch einen unzureichenden Aortenklappenverschluss gekennzeichnet ist, was zu einem Blutrückfluss von der Aorta in den linken Ventrikel (LV) während der Diastole führt.
Aorteninsuffizienz kann akut (aufgrund einer bakteriellen Endokarditis oder Aortendissektion) oder chronisch (aufgrund einer angeborenen Bikuspidalklappe oder rheumatischem Fieber) sein und durch einen Klappendefekt oder eine Aortenanomalie verursacht werden.
Die meisten Fälle von akutem AVR führen zu einer schnellen Abnahme der LV-Funktion, gefolgt von Lungenödemen und Herzdekompensation. Chronische AR kann lange Zeit kompensiert werden und wird erst symptomatisch, wenn eine Linksherzinsuffizienz auftritt.
Ein S3 und ein hohes, decrescendo-frühes diastolisches Murmeln sind bei der Auskultation zu hören. Ein erweiterter Pulsdruck ist ein weiteres charakteristisches diagnostisches Merkmal. Das wichtigste diagnostische Instrument, sowohl für die Feststellung der Diagnose als auch für die Beurteilung des Grades der Erkrankung, ist die Echokardiographie.
Die konservative Therapie für asymptomatische Personen umfasst die Symptomkontrolle und körperliche Aktivität wie toleriert. Patienten, die symptomatisch sind oder eine stark verminderte LV-Funktion haben, benötigen einen chirurgischen Eingriff, am häufigsten einen Aortenklappenersatz.