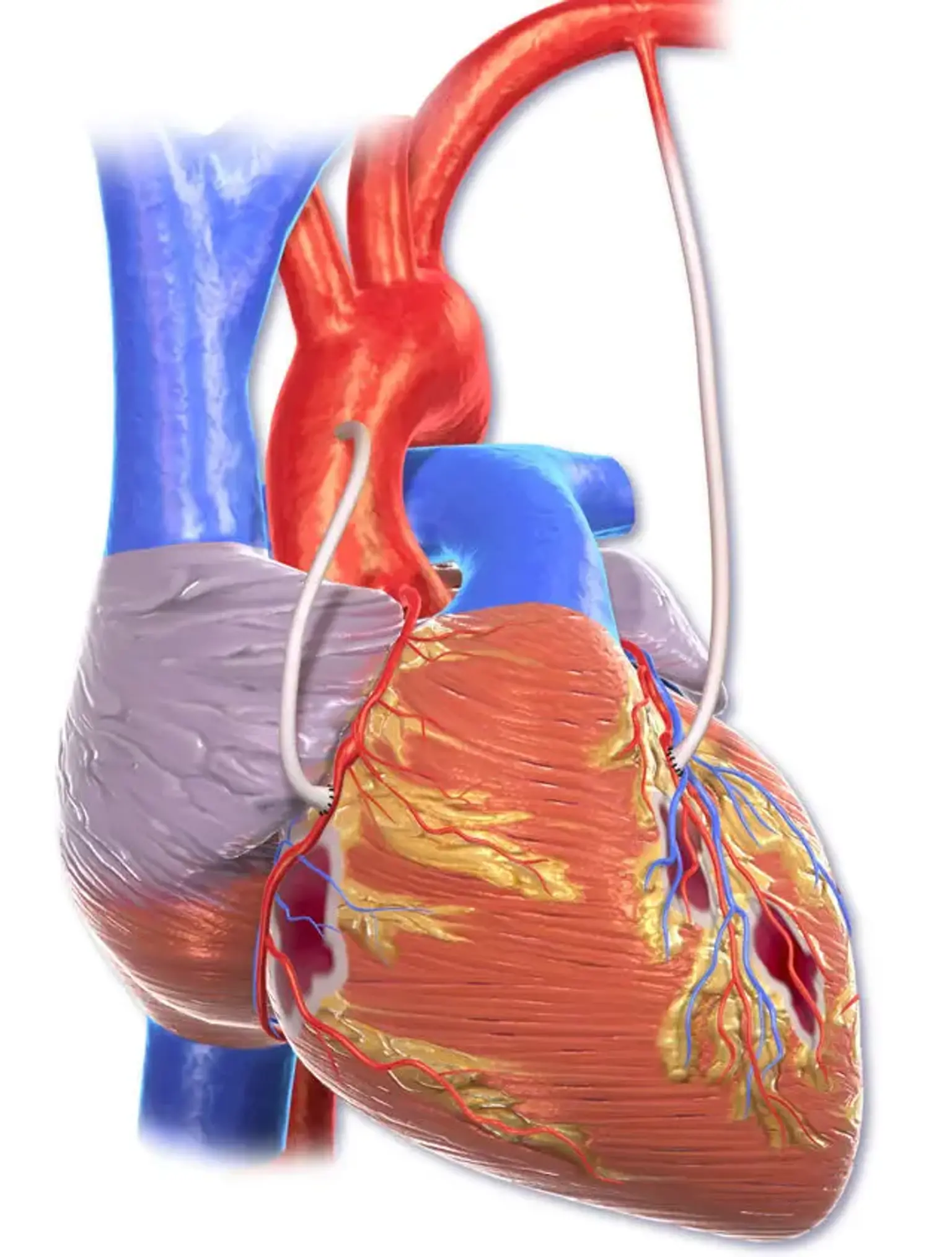
Injerto de derivación de la arteria coronaria (CABG)
Visión general
La CABG es un procedimiento quirúrgico complejo en el que las obstrucciones ateromatosas en las arterias coronarias de un paciente se evitan utilizando conductos venosos o arteriales cosechados. El bypass restaura el flujo sanguíneo al miocardio isquémico, restaurando la función y la viabilidad y aliviando los síntomas anginosos.
Casi 400,000 operaciones de CABG se llevan a cabo cada año, lo que la convierte en la cirugía cardiaca que se realiza con mayor regularidad; sin embargo, las tendencias quirúrgicas han cambiado a medida que las opciones alternativas, como la terapia médica y la intervención coronaria percutánea (ICP), se han vuelto más populares.
Cirugía CABG
El injerto de derivación de la arteria coronaria (CABG) es un procedimiento utilizado para mejorar la calidad de vida y minimizar la mortalidad relacionada con el corazón en individuos con enfermedad arterial coronaria (EAC). EAC es la mayor causa de muerte en los Estados Unidos y el mundo industrializado, afectando a 16.5 millones de adultos estadounidenses (de 20 años) cada año.
Es responsable de 530,989 muertes en los Estados Unidos cada año, y se espera que las consecuencias a largo plazo de la EAC, incluso la disfunción ventricular izquierda y la insuficiencia cardíaca, afecten a casi 8 millones de personas mayores de 18 años para 2030.
La cirugía CABG se realizó por primera vez en la década de 1960 con el objetivo de proporcionar alivio sintomático, mejorar la calidad de vida y mejorar la esperanza de vida de los pacientes con EAC. En comparación con el tratamiento médico, la CABG aumentó las tasas de supervivencia en individuos con enfermedad multivaso y abandonó la enfermedad principal en la década de 1970.
El nuevo paradigma de tratamiento EAC exige un enfoque de equipo cardíaco en el que el cardiólogo y el cirujano cardíaco evalúen la angiografía coronaria juntos y proporcionen al paciente la mejor alternativa disponible para la revascularización coronaria, ya sea la implantación de un stent coronario percutáneo o CABG. Por el momento, el paciente promedio de CABG es mayor, ha tenido una intervención coronaria percutánea (ICP) previa y tiene muchas más comorbilidades.
A pesar de estos riesgos, la CABG sigue siendo una de las operaciones quirúrgicas más importantes en la historia de la medicina moderna, habiendo probablemente salvado más vidas y ofrecido un alivio sintomático más considerable que cualquier otra cirugía mayor. Los nuevos enfoques mínimamente invasivos, los avances en la anestesia y el manejo de la unidad de cuidados intensivos (UCI) y los avances tecnológicos están empujando los límites de esta operación a nuevas alturas.
En general, hay dos tipos de procedimientos quirúrgicos de CABG: en la bomba y fuera de la bomba, con la diferencia de que un CABG en la bomba utiliza un circuito de derivación cardiopulmonar y un corazón detenido para trabajar. La arteria mamaria interna izquierda (LIMA) y los injertos de vena safena (SVG) de las extremidades inferiores se emplean comúnmente como conductos de injerto de derivación.
La arteria mamaria interna derecha (RIMA), la arteria radial y la arteria gastroepiploica son algunos de los otros conductos que se pueden trasplantar. El tipo y la posición de los injertos están determinados por la anatomía del paciente y la ubicación de las arterias bloqueadas. El LIMA se injerta típicamente en la arteria descendente anterior izquierda (LAD), mientras que los otros conductos se utilizan para acceder a las otras arterias bloqueadas.
Anatomía y Fisiología
Dos arterias coronarias principales irrigan el miocardio del corazón: la arteria coronaria principal izquierda y la arteria coronaria derecha (ACR). La arteria coronaria principal izquierda es típicamente una sección corta que se divide en las arterias descendentes anteriores izquierdas (LAD) y circunflejas. El LAD se divide en ramas diagonales, mientras que la arteria circunfleja se divide en ramas marginales obtusas. El ACR se divide en dos ramas: la arteria descendente posterior (CAP) y las ramas marginales.
Dependiendo de qué arteria suministre el tabique interventricular y el CAP, la circulación coronaria se puede clasificar en sistemas dominantes izquierdos, dominantes derechos y codominantes. La arteria circunfleja suministra el CAP en un sistema dominante a la izquierda, mientras que el ACR suministra el CAP en un sistema dominante a la derecha. Con el suministro vascular codominante, el CAP es alimentado por las arterias RCA y circunfleja al mismo tiempo.
Las obstrucciones en cualquiera de las arterias coronarias resultan en una deficiencia correspondiente en la perfusión miocárdica, isquemia, y si no se trata pueden resultar en un infarto permanente o daño al corazón.
Información histórica
En 1912, Alexis Carrel fue galardonado con el Premio Nobel de Fisiología y Medicina por su trabajo. Su conocimiento de la relación entre la angina de pecho y la estenosis de la arteria coronaria le permitió anastomosear un segmento de la arteria carótida desde la aorta torácica descendente hasta la arteria coronaria izquierda en un modelo canino.
Arthur Vineberg, un notable cirujano canadiense, trasplantó la arteria torácica interna izquierda (mamaria) directamente en el miocardio del ventrículo anterior izquierdo en pacientes con angina de pecho grave a fines de la década de 1940. Sorprendentemente, algunas personas tuvieron una reducción considerable de los síntomas como resultado de esta cirugía.
Sabiston realizó el primer procedimiento planificado de derivación de venas safenas para la revascularización coronaria en la Universidad de Duke en 1962. Kolessov utilizó la arteria torácica interna izquierda (mamaria) para evitar la arteria descendente anterior izquierda sin derivación cardiopulmonar en 1964, y Carpentier fue pionero en el uso de injertos de arteria radial como conductos CABG en 1973.
CABG floreció como el único tratamiento para EAC a lo largo de la década de 1970 y principios de la década de 1980. El número de cirugías de CABG realizadas disminuyó con el desarrollo, la introducción y la adopción generalizada de stents percutáneos en la arteria coronaria en las décadas de 1980 y 1990. Sin embargo, varios ensayos multicéntricos que comparan la CABG con el tratamiento actual con stent han establecido claramente las ventajas de la CABG, particularmente cuando se incluyen características específicas del paciente, como diabetes, EAC multivaso y miocardiopatía isquémica.
Indicaciones para CABG
Cuando hay obstrucciones de alto grado en cualquiera de las arterias coronarias principales y/o la intervención coronaria percutánea (PCI) no ha logrado eliminar los bloqueos, a menudo se recomienda la CABG. Las siguientes son las recomendaciones de Clase 1 de las directrices de la ACCF/AHA de 2011:
- Enfermedad principal izquierda superior al 50%
- Enfermedad arterial coronaria de tres vasos de más del 70% con o sin afectación proximal de LAD
- Enfermedad de dos vasos: LAD más otra arteria principal
- Una estenosis severa de más del 70% en un paciente con síntomas anginosos considerables a pesar del tratamiento máximo con medicamentos
- En un sobreviviente de muerte súbita cardíaca con taquicardia ventricular relacionada con isquemia, una enfermedad vascular fue más del 70%.
Otras indicaciones para CABG incluyen las siguientes:
- Angina incapacitante (Clase I)
- Isquemia que persiste en el contexto de un infarto de miocardio sin elevación del segmento ST (IMSEST) que es refractario al tratamiento medicinal (Clase I)
- Función ventricular izquierda deficiente, pero viable, miocardio no funcional por encima del defecto anatómico que se puede revascularizar.
- EAC clínicamente grave con estenosis del 70 por ciento o más en uno o más vasos, así como angina refractaria a pesar del tratamiento con medicamentos y la PCI
- EAC clínicamente grave de 70% o más estenosis en 1 o más vasos en sobrevivientes de paro cardíaco repentino que se cree que es causado por arritmia ventricular isquémica
- EAC clínicamente grave con 50% o más de estenosis en 1 o más vasos en pacientes sometidos a cirugía cardíaca por otras razones (por ejemplo, reemplazo de válvula o cirugía aórtica)
La CABG se puede realizar como tratamiento de emergencia en el contexto de un IM con elevación del segmento ST (IAMCEST) si la intervención coronaria percutánea (ICP) no fue posible o si la ICP falló y hay dolor e isquemia prolongados que afectan a una parte importante del miocardio a pesar de la terapia medicinal.
Los factores que aumentan el beneficio de supervivencia de la CABG incluyen los siguientes:
- Fracción de eyección del ventrículo izquierdo del 45% o menos
- Diabetes mellitus
- Regurgitación mitral isquémica
- Fallo de PCI, con o sin IM agudo (IAM)
Contraindicaciones
La CABG no se recomienda para personas asintomáticas que tienen un bajo riesgo de infarto de miocardio o muerte. Los pacientes que se beneficiarán poco de la revascularización coronaria también están excluidos.
Aunque la edad de la tercera edad no es una contraindicación, la CABG debe abordarse con precaución en los ancianos, particularmente en los mayores de 85 años. Estos individuos también son más propensos a tener problemas perioperatorios después de la CABG. En pacientes con EAC complicada, un enfoque de equipo cardíaco multidisciplinario que haga hincapié en la toma de decisiones compartida es fundamental para proporcionar al paciente la mejor oportunidad de un plan de revascularización exitoso.
Procedimiento CABG
Además de la angiografía coronaria que detectó la enfermedad de la arteria coronaria, el paciente requerirá varias pruebas realizadas en preparación para la cirugía. Se requerirán pruebas de laboratorio como un hemograma completo (CBC), paneles metabólicos que incluyen pruebas de función hepática, paneles de coagulación y hemoglobina A1c. Otras pruebas, incluso como un electrocardiograma (ECG), ecocardiografía, ecografía carotídea, radiografía de tórax y tal vez un mapeo de tórax o vena de las extremidades inferiores por tomografía computarizada, pueden ser necesarias.
Para evitar arritmias como la fibrilación auricular, con frecuencia se administran medicamentos preoperatorios como los betabloqueantes durante el período perioperatorio. Anteriormente, la aspirina se retenía de 5 a 7 días antes de la cirugía, pero ahora se sugiere comenzar o continuar antes de la operación.
Cuando el paciente llegue al hospital, se establecerá el acceso intravenoso y se examinarán sus medicamentos y pruebas preoperatorias. Se eliminará el vello de los lugares de la cirugía y se le dará al paciente un baño de clorhexidina.
Equipo
Esta cirugía quirúrgica significativa requiere no solo el equipo requerido para la mayoría de las otras operaciones quirúrgicas, sino también varias piezas especializadas de equipo, como una máquina de derivación cardiopulmonar con un dispositivo calentador-enfriador para calentar y enfriar la sangre.
Personal
La operación es realizada por un equipo quirúrgico cardiovascular especializado con amplia formación y experiencia en el cuidado de estos pacientes complejos. El equipo está formado por el cirujano cardiotorácico y sus asistentes, anestesiólogos, enfermeras, técnicos quirúrgicos y perfusionistas.
Evaluación de riesgos
Se están desarrollando modelos de riesgo para predecir la mortalidad a los 30 días después de la CABG aislada. Los predictores más utilizados en cirugía cardíaca son el sistema Euroscore y el Modelo de Riesgo de Cirugía Cardíaca 2008 de la Sociedad de Cirujanos Torácicos (STS). La edad, el IM previo, la PVD, la insuficiencia renal, el estado hemodinámico y la FE son factores compartidos en estos dos modelos sobresalientes. Ocho de los factores más relevantes, incluyendo la edad, la agudeza quirúrgica, el estado reoperatorio, el nivel de creatinina, la diálisis, el shock, la enfermedad pulmonar crónica y la FE, explican el 78 por ciento de la variación en el modelo STS.
Premedicación
La premedicación busca reducir las necesidades de oxígeno miocárdico mediante la reducción de la frecuencia cardíaca y la presión arterial sistémica, así como aumentar el flujo sanguíneo miocárdico utilizando vasodilatadores. Los siguientes medicamentos deben tomarse hasta el momento de la cirugía:
- Betabloqueantes, bloqueadores de los canales de calcio y nitratos
- Aspirina
Los agentes administrados son los siguientes:
- Temazepam inmediatamente preoperatorio
- Midazolam, una pequeña dosis intravenosa (IV) en el quirófano antes de la inserción de la vía arterial
Cada paciente debe recibir 2 unidades de sangre (para casos leves) o 6 unidades de sangre, plasma fresco congelado y plaquetas combinadas (para casos complejos). Se puede considerar que el ácido tranexámico (bolo de 1 g antes de la incisión quirúrgica, seguido de una infusión de 400 mg / h durante la cirugía) minimiza la hemorragia mediastínica postoperatoria y la cantidad de productos sanguíneos necesarios (es decir, glóbulos rojos y plasma fresco congelado)
Anestesia
La cirugía cardíaca generalmente se realiza bajo anestesia general profunda con entubación endotraqueal. Los siguientes dos tipos de bloqueo neuroaxial se utilizan raramente como complementos:
- Infusión intratecal de opioides
- Anestesia epidural torácica (generalmente una infusión de anestésico/opioide local en dosis bajas)
Técnica
El proceso comienza después de que el paciente está en la sala de operaciones y se conecta a los monitores estándar. Antes de inducir la anestesia general, un anestesiólogo puede insertar una línea arterial para controlar la presión arterial del paciente de forma invasiva. Tras la inducción de la anestesia general y la intubación del paciente, se puede insertar una línea central para el acceso venoso y un catéter de la arteria pulmonar, seguido de la inserción de un transductor de ecocardiografía transesofágica.
Antes de la incisión quirúrgica, el paciente se prepara y cubre estérilmente, y se administra un tiempo de espera. El cirujano realiza una esternotomía medial para prepararse para la extracción del LIMA para su uso como conducto. Un asistente capacitado, generalmente un asistente médico, un primer asistente de enfermería u otro cirujano, utiliza procedimientos abiertos o asistidos por video para extirpar la vena safena de una o ambas piernas al mismo tiempo.
Después de la adquisición de conductos adecuados, el cirujano prescribe anticoagulación, con mayor frecuencia heparina, para ser administrada en preparación para el bypass cardiopulmonar (CPB). La aorta y el corazón del paciente se canulan centralmente, y el tubo está conectado al circuito de derivación cardiopulmonar. Después del inicio de la CPB, el corazón se detiene con cardioplejia alta en potasio para que el cirujano pueda anastomosear los conductos cosechados a las arterias coronarias distantes a las obstrucciones.
Como conductos para el injerto de derivación de la arteria coronaria, se pueden emplear arterias o venas (CABG). Una publicación clave de la Clínica Cleveland demostró las ventajas de supervivencia de injertar la arteria torácica interna izquierda (mamaria) en la arteria coronaria descendente anterior izquierda hace muchos años. Esto sigue siendo cierto; de hecho, si es posible, el injerto bilateral de arteria torácica interna (mamaria) ofrece un beneficio considerable de supervivencia a largo plazo. La evidencia sólida muestra que el uso de un injerto de arteria adicional en lugar de un injerto venoso se relaciona con mejores resultados a largo plazo.
La vena safena más grande y, en raras ocasiones, la vena safena corta son los injertos de vena más utilizados regularmente, mientras que la arteria torácica interna (mamaria) es el trasplante de arteria más utilizado. El injerto de arteria radial se reintrodujo en la práctica clínica en la década de 1990 y continúa demostrando altas tasas de permeabilidad del 80% o más después de 10 años de seguimiento, particularmente si la estenosis vascular objetivo era superior al 90%.
La desventaja de los injertos de venas safenas es que su permeabilidad disminuye con el tiempo: 10-20% se bloquean 1 año después de la cirugía debido a errores técnicos, trombosis e hiperplasia íntima. Otro 1-2 por ciento de los injertos de venas se ocluyen cada año de 1 a 5 años después de la cirugía, y otro 4-5 por ciento ocluyen cada año de 6 a 10 años. La oclusión del injerto de vena que ocurre uno o más años después de la CABG es causada por aterosclerosis del injerto de vena, que se acompaña del desarrollo de hiperplasia neointimal.
Solo el 50-60% de los injertos de venas safenas son patentes 10 años después de la cirugía, y solo la mitad de ellos están libres de aterosclerosis angiográfica. Los pacientes deben tomar medicamentos antiplaquetarios de por vida, generalmente en forma de aspirina diaria en dosis bajas (81 mg), como parte de la profilaxis secundaria adecuada.
Los injertos de arteria torácica interna (mamaria), a diferencia de los injertos de venas safenas, mantienen la permeabilidad a lo largo del tiempo. Más del 90% de los injertos de arteria torácica interna (mamaria) todavía están patentes después de 10 años. Cuando se pasa por alto la arteria coronaria anterior izquierda, se debe utilizar la arteria torácica interna izquierda (mamaria) como conducto.
Los conductos están vinculados a una nueva ostia generada en la aorta proximal después de que el cirujano anastomosa las partes distales. La cardioplejia se enjuaga, el corazón comienza a contraerse y el cirujano puede examinar los injertos para determinar el flujo sanguíneo y la competencia, así como el sangrado de los sitios de anastomosis. Luego, el tórax se cierra con cables esternales y el paciente se traslada a la unidad de cuidados críticos para el monitoreo de la estabilidad hemodinámica y la extubación.
Complicaciones
El accidente cerebrovascular, la infección de la herida, la insuficiencia del injerto, la insuficiencia renal, la fibrilación auricular postoperatoria y la mortalidad son todas las posibles consecuencias de la CABG. Se ha informado que la tasa de accidente cerebrovascular después de la CABG oscila entre el 1% y el 2%, dependiendo de las características del paciente y los factores de riesgo para el accidente cerebrovascular, que incluyen edad avanzada, accidente cerebrovascular previo, aterosclerosis aórtica, enfermedad arterial periférica, fibrilación auricular perioperatoria y diabetes.
Las tasas de infección de la herida esternal son de alrededor del 1% y se ven afectadas por variables de riesgo como la obesidad, la diabetes, la enfermedad pulmonar obstructiva crónica (EPOC) y la duración de la operación.
El fracaso de un injerto de vena safena (SVG) es más probable dentro de los 30 días posteriores a la cirugía y es causado por numerosas razones, como el tamaño de la vena y la longitud excesiva, la escorrentía distal y el flujo deficiente, y la hipercoagulabilidad y trombosis. Con la angiografía repetida después de la CABG, se han observado tasas de fracaso de SVG de hasta el 25%. Alternativamente, los injertos arteriales como la arteria mamaria interna izquierda (LIMA) y los injertos arteriales radiales duran más tiempo y tienen tasas de permeabilidad que alcanzan el 90% después de 10 años.
Las tasas de insuficiencia renal postoperatoria después de la CABG varían del 2% al 3%, y el 1% necesita diálisis. La enfermedad renal preoperatoria, la vejez, la diabetes, el tipo de cirugía, la disfunción del VI y el shock son factores de riesgo. Aunque definitivamente no se ha demostrado que ningún medicamento disminuya las tasas de insuficiencia renal inducida por CABG, la CABG fuera de la bomba puede ofrecer un beneficio sobre la CABG en la bomba.
La fibrilación auricular dentro de los primeros 5 días después de la CABG es bastante frecuente, con tasas que oscilan entre el 20% y el 50%, y se relaciona con una mayor morbilidad, incluido un mayor riesgo de accidente cerebrovascular embólico y muerte. Se ha demostrado que la estrategia más efectiva para minimizar la incidencia de fibrilación auricular postoperatoria es la terapia preoperatoria con betabloqueantes y tal vez amiodarona.
El riesgo de mortalidad perioperatoria después de la CABG varía según las comorbilidades, la urgencia de la cirugía y el volumen de casos de la instalación donde se realiza el procedimiento, que oscila entre el 1% y el 2%.
Resultados
Según un metanálisis de seis ensayos clínicos aleatorizados en los que participaron 6055 pacientes de la era del injerto arterial y la colocación de stents, el injerto de derivación de la arteria coronaria (CABG) conduce a una reducción de la mortalidad a largo plazo y los infartos de miocardio (IM), así como a reducciones en las revascularizaciones repetidas en pacientes con enfermedad coronaria multivasina, independientemente de si los pacientes son diabéticos o no.
Un metanálisis de ocho ensayos aleatorizados que involucraron a 3612 pacientes adultos con diabetes y enfermedad arterial coronaria multivaso (EAC) encontró que la CABG redujo el riesgo de muerte por todas las causas en un 33% después de 5 años en comparación con la ICP. Cuando los pacientes que tenían CABG se compararon con subgrupos de pacientes que recibieron stents de metal desnudo o stents liberadores de fármacos, la disminución del riesgo relativo no varió sustancialmente.
A los pacientes de 51 a 70 años y a los mayores de 70 años que recibieron CABG en el mismo período de tiempo les fue considerablemente peor en términos de supervivencia. La enfermedad renal crónica, una fracción de eyección ventricular izquierda baja, la enfermedad vascular periférica o la enfermedad pulmonar obstructiva crónica fueron los principales factores de riesgo de muerte por todas las causas.
El Estudio de Extensión del Tratamiento Quirúrgico para la Insuficiencia Cardíaca Isquémica (STICH) (STICHES) concluyó que las tasas de muerte por cualquier causa, muerte por causas cardiovasculares y muerte por cualquier causa u hospitalización por causas cardiovasculares fueron significativamente más bajas en los pacientes que se sometieron a CABG y recibieron medicare.
Además, hubo una variación considerable a nivel hospitalario en las tasas de CABG de STEMI, y la CABG se realizó con frecuencia dentro de los 1-3 días posteriores a la angiografía. Pacientes que recibieron CABG y aquellos que no tuvieron tasas de mortalidad hospitalaria similares.
Un metanálisis de 6637 pacientes con EAC principal izquierda sin protección de nueve ensayos durante un período de 14 años (2003-2016) encontró que la ICP con stents liberadores de fármacos se asoció con una mortalidad cardíaca y por todas las causas comparable, pero tasas reducidas de accidente cerebrovascular y mayores tasas de revascularización repetida. Para los eventos cardíacos y cerebrovasculares adversos significativos, una tendencia a favor de la CABG frente a la PCI no alcanzó significación estadística.
En cuanto a la calidad de vida después de la CABG versus pci para la EAC multivaso, ambos procedimientos mejoran la frecuencia de la angina de pecho. Sin embargo, a 1 mes después del procedimiento, los pacientes con PCI tienden a recuperarse más rápido y tienen un mejor estado de salud a corto plazo que los pacientes con CABG, sin embargo, a los 6 meses y más tiempo después del procedimiento, los pacientes con CABG parecen tener un mejor alivio de la angina y calidad de vida que los pacientes con PCI.
Conclusión
Un injerto de derivación de la arteria coronaria (CABG) es una técnica quirúrgica utilizada para tratar la enfermedad coronaria con el objetivo de mejorar la calidad de vida y reducir la mortalidad relacionada con el corazón. Redirige la sangre alrededor de secciones constreñidas u obstruidas de las arterias principales, aumentando el flujo sanguíneo y el suministro de oxígeno al corazón.