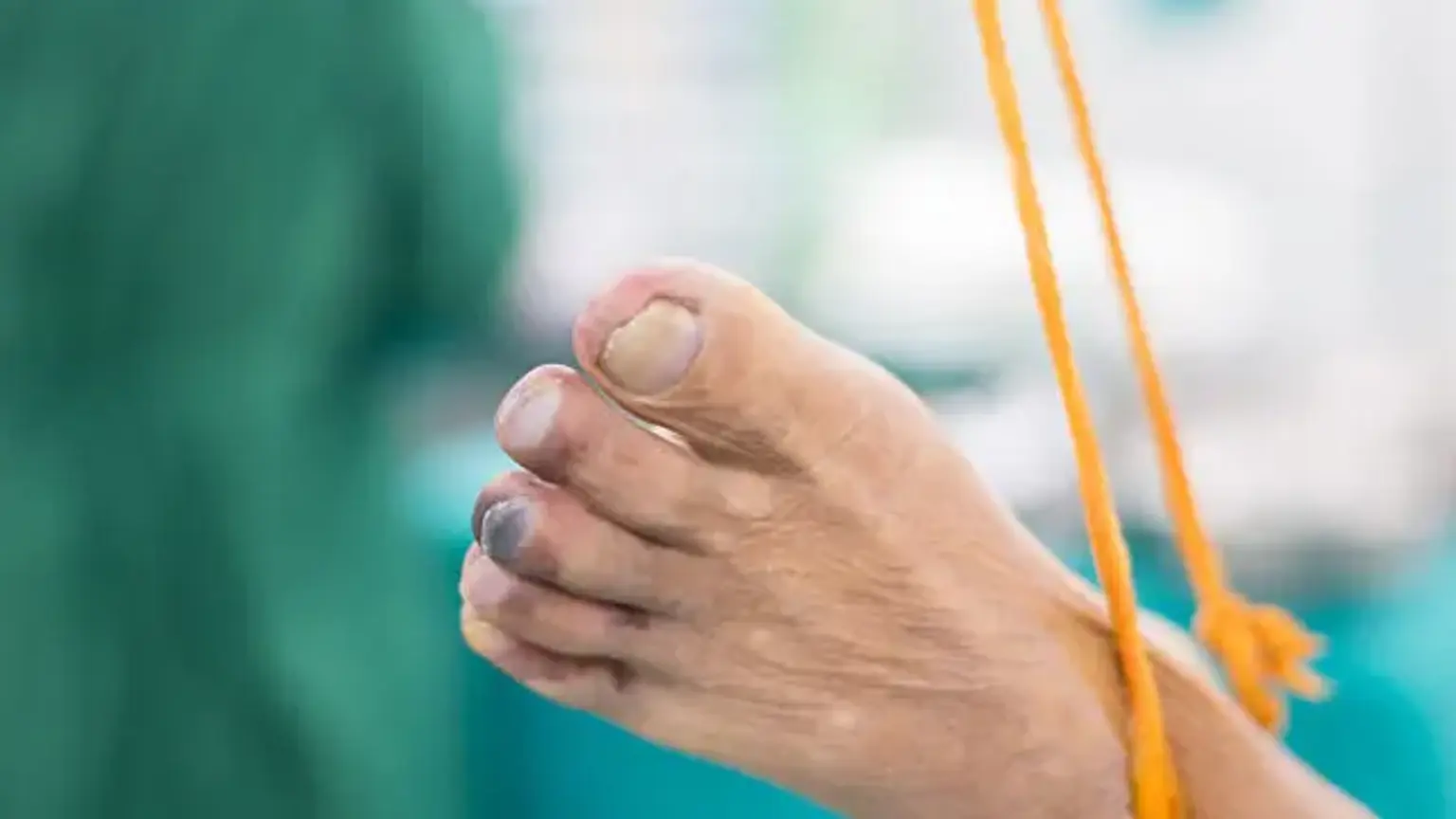
Isquemia crítica de extremidades (CLI)
Descripción general
Algunas personas con enfermedad arterial periférica pueden desarrollar isquemia crítica de las extremidades, una afección con una tasa de morbilidad y mortalidad significativa. Para evitar la amputación y disminuir la muerte, se recomienda el diagnóstico precoz, el manejo médico adecuado y la revascularización.
Para estos pacientes, es ideal una estrategia multidisciplinaria que involucre intervencionistas endovasculares, cirujanos vasculares, podólogos, especialistas en enfermedades infecciosas y especialistas en el cuidado de heridas.
Definición de isquemia crítica de extremidades (CLI)
La isquemia crítica de las extremidades (CLI) es una enfermedad clínica caracterizada por molestias isquémicas en reposo o pérdida de tejido causada por disfunción arterial periférica, como úlceras que no cicatrizan o gangrena. CLI conlleva un riesgo sustancial de pérdida de extremidades y complicaciones cardiovasculares a corto plazo. La angiografía, ya sea no invasiva o invasiva, ayuda a determinar la viabilidad y el método de revascularización arterial.
La ICE se describe tradicionalmente como malestar en reposo o pérdida de tejido (úlceras o gangrena) acompañada de isquemia, caracterizada por parámetros hemodinámicos como presiones bajas en los tobillos o los dedos de los pies o lecturas bajas de oxígeno transcutáneo (TcO2). Los requisitos de presión del tobillo varían de 40 a 70 mm Hg, las presiones de los dedos de los pies de 30 a 50 mm Hg y los niveles de TcO2 de 20 a 40 mm Hg. Los puntos de corte más altos para la pérdida de tejido se utilizan con frecuencia bajo la idea de que se necesita una perfusión más alta para la cicatrización de heridas; sin embargo, el consenso de los expertos sobre estos criterios hemodinámicos varía entre los estándares.
Los estándares iniciales estaban destinados a estandarizar los requisitos de entrada para los ensayos clínicos de CLI en pacientes sin diabetes mellitus, lo que permitía realizar comparaciones entre estudios o evaluar la probabilidad de cicatrización de heridas. 8 Sin embargo, su uso como pruebas diagnósticas CLI en la práctica clínica es cuestionable.
Debido a la superposición significativa en las lecturas entre los pacientes con CLI que progresan o no continúan con amputaciones graves o eventos cardiovasculares, es problemático definir puntos de corte particulares para la presión del dedo del pie o TcO2 para el diagnóstico clínico de CLI. Según un estudio, no tuvieron ningún efecto sobre la elección de someterse a una revascularización. 12 Además de isquemia, otras definiciones de CLI incluyen infección de heridas y osteomielitis.
Factores de riesgo de isquemia crítica de extremidades
Los factores de riesgo de la isquemia crónica de las extremidades son los mismos que los de la aterosclerosis, que es el endurecimiento y constricción de las arterias causado por la acumulación de depósitos grasos conocidos como placa. Este síndrome se ve exacerbado por los siguientes factores:
- Edad
- De fumar
- Diabetes
- Sobrepeso u obesidad
- Estilo de vida sedentario
- Colesterol alto
- Hipertensión
- Antecedentes familiares de aterosclerosis o claudicación.
Fisiopatología
La CLI es causada más comúnmente por EAP multisegmentaria con disminución del flujo sanguíneo en los tejidos periféricos. En raras situaciones, la presencia de un gasto cardíaco reducido al mismo tiempo puede empeorar la perfusión periférica en pacientes con CLI.
Aunque este síntoma común de la EAP está disminuido o ausente en las personas diabéticas con neuropatía, la disminución de la oxigenación y la nutrición de los tejidos periféricos puede producir claudicación o malestar durante el descanso. Además, los pacientes diabéticos con CLI suelen tener lesiones arteriales distales caracterizadas por la afectación de la arteria por debajo de la rodilla (BTK), y la ulceración, la necrosis o la gangrena son con frecuencia las indicaciones iniciales de la EAP.
Síntomas de isquemia crítica de extremidades
Los síntomas más notables de la isquemia crítica de las extremidades son el dolor isquémico en reposo, que es un dolor agudo en las piernas y los pies mientras la persona no se mueve, o llagas que no cicatrizan en los pies o las piernas. Otros signos y síntomas incluyen:
- Dolor o entumecimiento en los pies
- Piel brillante, suave y seca de las piernas o los pies.
- Engrosamiento de las uñas de los pies
- Pulso ausente o disminuido en las piernas o los pies
- Llagas abiertas, infecciones de la piel o úlceras que no cicatrizan
- Gangrena seca (piel negra y seca) de las piernas o los pies
Diagnóstico
La manifestación clínica de la CLI está determinada por el grado de isquemia, la presencia de infección y la existencia de neuropatía coexistente. El dolor isquémico suele empeorar cuando el paciente está en decúbito supino y con frecuencia requiere el uso de fármacos para la analgesia. Tiene el potencial de despertar a las personas de su sueño y evitar que deambulen. Incluso en ausencia de isquemia importante, la infección puede exacerbar el malestar. La neuropatía puede causar daño a los tejidos o disfrazar la incomodidad de una úlcera.
Las recomendaciones actuales exigen medir la presión del tobillo o el índice tobillo-brazo. A pesar de que la calcinosis medial puede proporcionar resultados falsamente altos, las presiones en los dedos del pie pueden sugerir un bloqueo arterial. Los niveles de TcO2 o las presiones de perfusión de la piel pueden usarse para predecir la probabilidad de cicatrización de heridas.
El objetivo principal es mantener intacta la función de las extremidades. La revascularización es una técnica crítica para la preservación de la extremidad, sin embargo, no mejora la función y la movilidad de la extremidad en todos los pacientes. El deterioro cognitivo, el estado no ambulatorio antes de la CLI y las comorbilidades significativas, por ejemplo, predicen un mal resultado incluso con la revascularización. Al considerar la revascularización, las imágenes arteriales determinan los objetivos y la forma de revascularización.
La angiografía no invasiva que utiliza la angiografía por tomografía computarizada (CTA) o la angiografía por resonancia magnética, así como la ecografía dúplex, pueden detectar el bloqueo arterial. La ecografía dúplex no requiere contraste, aunque requiere una habilidad especializada y puede tener dificultades para escanear las arterias tibiales. El mapeo de venas es esencial en la enfermedad infrainguinal para establecer la factibilidad de un bypass quirúrgico con vena autógena.
La CTA requiere la administración de contraste yodado, lo que puede provocar nefropatía por contraste en personas con función renal reducida. Los artefactos causados por arterias muy calcificadas pueden restringir la ATC, especialmente en la enfermedad distal. La angiografía por resonancia magnética de tiempo de vuelo sin contraste es propensa a artefactos con flujo no laminar típico de la placa aterosclerótica, y los problemas de contraste con gadolinio restringen su utilidad en la enfermedad renal avanzada.
En ocasiones, la ATC y la angiografía por resonancia magnética son insuficientes para evaluar las arterias tibiales más pequeñas. No obstante, la ATC y la angiografía por resonancia magnética pueden ayudar en la localización de los objetivos de la enfermedad, así como en la planificación de la técnica y la estrategia de revascularización.
Debido a que las imágenes no invasivas de las arterias distales son limitadas, la angiografía invasiva se realiza con frecuencia para determinar la posibilidad de revascularización y debe evaluarse antes de una amputación grave. El contraste yodado se utiliza en la angiografía invasiva, que tiene la resolución espacial más alta. Con la angiografía por sustracción convencional y digital, los casos de diagnóstico pueden necesitar tan solo 30 ml de contraste para ambas piernas.
Controlar el dolor, que puede incluir medicamentos, aliviar la presión sobre las úlceras, usar botas de piel de oveja para promover el suministro colateral superficial e inclinar la cama hacia abajo para aumentar la confianza y la perfusión de las extremidades son algunas de las primeras terapias. 2 El tratamiento del dolor tiene el potencial de revertir la vasoconstricción mediada por el sistema simpático. Aunque algunos de estos métodos solo mejoran ligeramente la perfusión, pueden aliviar el dolor asociado con CLI mientras se planifica la terapia final.
Gestión
El objetivo de la terapia CLI es aliviar el dolor, promover la cicatrización de heridas, mejorar la función del paciente, evitar la amputación de extremidades y minimizar la muerte. La revascularización de miembros inferiores es la terapia de primera línea para los pacientes con ICE que pueden tolerarla. Los pacientes con CLI con muchas comorbilidades o una posibilidad limitada de revascularización efectiva pueden necesitar una amputación primaria en algunas circunstancias. El manejo del dolor, el control de los factores de riesgo cardiovascular y el control de la glucemia requieren intervención médica simultánea.
Tratamiento médico
Dolor
El tratamiento del dolor es fundamental para mejorar la calidad de vida y la función. En la mayoría de las situaciones, una revascularización periférica suficiente alivia las molestias periféricas. Se requiere tratamiento médico en pacientes sin opción-CLI, que han sido reconocidos como aquellos que no son curables mediante revascularización.
Aunque los opioides son necesarios con frecuencia, el paracetamol y los medicamentos antiinflamatorios no esteroideos suelen ser los tratamientos de primera línea. La terapia analgésica administrada de forma regular suele ser más eficaz que la terapia analgésica administrada a demanda. En algunas circunstancias, el dolor puede ser neuropático debido a la existencia de neuropatía periférica. Debido a que el dolor neuropático puede requerir una estrategia de tratamiento distinta, se debe realizar un diagnóstico diferencial completo.
De fumar
Para disminuir la progresión de la EAP y el riesgo de amputaciones mayores y eventos cardiovasculares, los fumadores deben dejar de fumar. Además, fumar aumenta la probabilidad de fracaso de la revascularización. Además, dejar de fumar reduce la mortalidad y aumenta la supervivencia libre de amputaciones en pacientes en comparación con aquellos que continúan fumando.
dislipidemia
El colesterol total, el LDL-C, los triglicéridos y las lipoproteínas son factores de riesgo para el desarrollo y la progresión de la EAP. Se sugiere el uso de estatinas en pacientes con EAP. Se ha demostrado que niveles bajos de LDL-C minimizan los eventos cardiovasculares (infarto de miocardio, eventos cerebrovasculares), y el objetivo para todos los pacientes con EAP es LDL-C 70 mg/dL.
Hipertensión
La presión arterial debe mantenerse bajo control en 140/90 mmHg en todos los pacientes y 130/80 mmHg en diabéticos o con proteinuria, según las guías. Los diuréticos tiazídicos, las enzimas convertidoras de angiotensina (ACE), los bloqueadores de los receptores de angiotensina (ARB), los bloqueadores de los canales de calcio (CCB) y los bloqueadores beta-adrenérgicos son medicamentos útiles para la presión arterial. ACE y ARB se consideran tratamientos de primera línea en personas diabéticas.
Diabetes
La diabetes ha sido identificada como un factor de riesgo significativo para la EAP. Aunque la EAP se asocia frecuentemente con numerosos factores de riesgo cardiovascular, se debe considerar un control glucémico estricto para retardar la aparición de problemas micro y macrovasculares.
La diabetes aumenta el riesgo de EAP entre tres y cuatro veces y el riesgo de claudicación dos veces. La mayoría de los pacientes diabéticos tienen otros factores de riesgo cardiovascular (tabaquismo, hipertensión y dislipemia) que contribuyen al desarrollo de la EAP. La diabetes también está relacionada con la neuropatía periférica y la disminución de la resistencia a las infecciones, lo que aumenta el riesgo de úlceras e infecciones en los pies.
Además, existe la creencia generalizada de que un control glucémico deficiente aumenta el riesgo de que las úlceras del pie diabético no cicatricen, a pesar de que no se han realizado estudios para evaluar la influencia de la HbA1c en los resultados de las úlceras del pie diabético. La HbA1c, por otro lado, se cree que es un predictor de amputación mayor, y la hiperglucemia es un factor de riesgo independiente de muerte en pacientes hospitalizados con pie diabético. El nivel objetivo de HbA1c es 7,0 por ciento para reducir el riesgo de complicaciones macrovasculares y el desarrollo de PAD.
Terapia antiplaquetaria
Se recomienda la profilaxis secundaria con aspirina/ácido acetilsalicílico (AAS) o clopidogrel en personas con EAP y/u otros trastornos cardiovasculares. Durante problemas asociados, como hemorragia gastrointestinal, una dosis baja de aspirina/AAS (75 a 160 mg) es beneficiosa y segura. Se recomienda la medicación antiplaquetaria doble (ASA+clopidogrel) durante al menos 1 mes después de la operación endovascular en pacientes diabéticos; más allá de 1 mes, se debe mantener AAS o clopidogrel de por vida.
Manejo quirúrgico de CLI
Revascularización Endovascular
La revascularización endovascular es el tratamiento preferido para la CLI en muchos lugares debido a que reduce la morbilidad y la mortalidad en comparación con la cirugía abierta. La mejor técnica de tratamiento (cirugía endovascular o abierta) estará determinada por las consideraciones anatómicas, las comorbilidades, el deseo del paciente y la experiencia y capacidad del operador.
Aunque la revascularización del flujo de entrada (aorto-ilíaca y femoral) puede curar la claudicación, la CLI se acompaña con frecuencia de enfermedad multinivel y, por lo general, requiere revascularización del flujo de salida (tibial) además de tratar la enfermedad del flujo de entrada. La mayoría de los datos para la terapia endovascular de la enfermedad por flujo sanguíneo proviene de ensayos de personas que tenían claudicación o una combinación de claudicación y CLI.
Revascularización quirúrgica abierta
Los objetivos de la revascularización quirúrgica son proporcionar flujo en línea recta hacia el pie, facilitar la cicatrización de heridas y restringir el nivel de amputación. La revascularización endovascular se asocia con un menor riesgo de infarto de miocardio perioperatorio, mortalidad y accidente cerebrovascular que la cirugía abierta. Sin embargo, en el caso de CLI, la pérdida potencial de la extremidad y la función puede favorecer la cirugía si el tratamiento endovascular no es viable o efectivo y los pacientes tienen una supervivencia respetable de 2 años.
Los tratamientos endovasculares para la enfermedad del flujo de entrada (p. ej., colocación de endoprótesis ilíaca) y la revascularización quirúrgica para la enfermedad femoral o infrainguinal se utilizan con frecuencia para tratar la enfermedad multinivel (p. ej., endarterectomía femoral común y derivación femoropoplítea). La oclusión aórtica distal y la enfermedad ilíaca pueden necesitar una derivación aorto-bifemoral, una derivación femoral a femoral contralateral o una derivación axilar-femoral.
La SFA proximal o arteria profunda puede alcanzarse durante una endarterectomía femoral común. Para disminuir la reestenosis, el cierre se realiza normalmente con un parche bovino o sintético, sin embargo, también se usa el cierre primario sin parche. Las complicaciones incluyen infección de la herida (especialmente en personas obesas), hematoma y fuga linfática. Este procedimiento ofrece una alta tasa de permeabilidad a largo plazo (> 90 por ciento) y se considera superior al tratamiento endovascular, particularmente para la enfermedad muy calcificada que afecta la SFA y los orígenes profundos.
El bypass infrainguinal, como la terapia endovascular, depende de una entrada y salida adecuadas. Los tres tipos de derivación de la vena safena incluyen la vena invertida (translocada), la vena no invertida y la derivación in situ, que implica la ligadura de las ramas de la vena y la movilización y anastomosis de los extremos distales a la arteria. Las dos últimas configuraciones requieren la escisión de las válvulas mediante valvulotomía, lo que en ocasiones puede dañar el conducto venoso. Los estudios observacionales indican que los tres diseños tienen resultados similares.
Comparaciones de revascularización quirúrgica abierta versus endovascular
La investigación Bypass Versus Angioplastia in Severe Ischaemia of the Leg (BASIL) es el primer ensayo aleatorizado que compara la terapia endovascular versus cirugía abierta de pacientes con ICE. Este experimento, que se publicó hace una década, no encontró diferencias en la amputación mayor o la mortalidad después de 5 años. El grupo quirúrgico tuvo una mayor tasa de infarto de miocardio, infección de la herida y problemas pulmonares, mientras que el grupo endovascular tuvo una mayor tasa de revascularización repetida.
Sin embargo, la mortalidad perioperatoria de la cirugía abierta ha disminuido en los últimos 10 a 15 años y existen más alternativas para el rescate del injerto con procedimientos endovasculares. Las soluciones endovasculares desarrolladas durante el estudio BASIL incluyen stents de metal desnudo, balones y stents recubiertos de fármacos y una variedad de cables y dispositivos para ayudar a atravesar oclusiones prolongadas.
Recientemente, varias ideas para los objetivos finales clave de CLI se han centrado en salvar la extremidad (evitar la amputación grave) y el requisito de una reintervención extensa (un nuevo injerto de derivación o trombólisis del injerto o segmento tratado). Como resultado de estos hallazgos, los Institutos Nacionales de Salud financiaron la investigación Best Endovascular Vs Best Surgical Therapy inpatients with Critical Limb Ischemia (BEST-CLI), una nueva evaluación aleatoria que compara la cirugía abierta versus la revascularización endovascular en CLI.
Amputación
Las amputaciones menores, como las amputaciones de dedos, radios (dedos y metatarsianos) o transmetatarsianos, requieren un suministro de sangre suficiente en el pie para promover la recuperación y, por lo general, forman parte del plan de tratamiento para la gangrena o la pérdida de tejido después de una revascularización exitosa. En general, la amputación pequeña no impide la independencia funcional ni necesita el uso de prótesis.
Las amputaciones mayores (por debajo o por encima de la rodilla) reducen la independencia funcional y necesitan el uso de una prótesis para caminar. Aunque evitar una amputación significativa es una prioridad, la amputación puede ser necesaria en las siguientes situaciones: revascularización fallida, pacientes con pérdida sustancial de tejido o infección, pacientes no aptos para la revascularización quirúrgica sin opciones endovasculares y pacientes potencialmente no ambulatorios. Hasta un tercio de todas las amputaciones por debajo de la rodilla pueden requerir una cirugía adicional o una amputación por encima de la rodilla debido a una mala recuperación.
Un pulso poplíteo permeable reduce la tasa de fallas en la cicatrización al 10%. Las amputaciones por encima de la rodilla se recuperan a una tasa de más del 90 %, pero solo el 20 % de los amputados logran una movilidad completa con una prótesis, en comparación con el 60 % con una prótesis por debajo de la rodilla. La edad, las amputaciones bilaterales o por encima de la rodilla, la demencia y el funcionamiento deficiente antes de la amputación se asocian con el uso y el funcionamiento deficientes de la prótesis después de una amputación mayor.
Cuidado de heridas
Mejorar la perfusión en la extremidad, abordar la infección, minimizar la presión sobre una herida, el desbridamiento y la nutrición adecuada son conceptos de cuidado de heridas. La cicatrización de heridas se ve favorecida por la eliminación de tejido desvitalizado o enfermo con un bisturí, colagenasas o incluso gusanos. Para evitar la osteomielitis, pueden ser necesarios antibióticos para tratar la infección.
Evitar la presión sobre la herida (por ejemplo, descargar el pie) también ayuda en la cicatrización de heridas. Usando botas de piel de oveja (Rooke), se puede elevar la temperatura local de la extremidad, lo que puede promover el flujo colateral superficial y ayudar a perfundir una extremidad. Los vendajes de presión negativa (por ejemplo, asistidos por vacío) mejoran el flujo capilar y ayudan en el drenaje de heridas. Aunque el tratamiento con oxígeno hiperbárico no ofrece beneficios para la prevención de amputaciones, puede mejorar el punto final más subjetivo de cicatrización de heridas en la diabetes mellitus.
La compresión neumática intermitente puede ayudar a la cicatrización de heridas y prevenir amputaciones catastróficas en personas que no tienen alternativas de revascularización. Los tratamientos basados en células, como la inyección de células mononucleares derivadas de la médula ósea, aún no han evitado amputaciones significativas en pacientes que no tienen alternativas de revascularización.
Terapia médica y vigilancia después de la revascularización
El fracaso de la terapia endovascular y quirúrgica de CLI causado por trombosis, proliferación neointimal o desarrollo de aterosclerosis requiere un monitoreo continuo de los pacientes por parte de especialistas vasculares. La vigilancia también implica abordar agresivamente los factores de riesgo ateroscleróticos para reducir el alto riesgo de eventos cardiovasculares.
La incomodidad de la isquemia recurrente en la pierna, la falta de progresión de la cicatrización de la herida o una caída en los índices tobillo-brazo son signos de reestenosis u oclusión. El uso de ultrasonografía dúplex en injertos de derivación es frecuente para descubrir estenosis de injertos para reparar y mantener la permeabilidad a largo plazo. Sin embargo, en un experimento aleatorizado, este procedimiento no se relacionó con una amputación reducida o una mayor permeabilidad, y no existen investigaciones aleatorias de su eficacia después del tratamiento endovascular.
Después de la terapia endovascular, proporcionamos un historial y un examen físico, además de emplear una ecografía dúplex en la arteria femoral, especialmente después de tratar la enfermedad de un segmento largo o cuando los síntomas o la cicatrización deficiente de la herida plantean dudas sobre la permeabilidad.
La evidencia de la terapia para prevenir la trombosis o la reestenosis después de los procedimientos endovasculares es limitada y, con frecuencia, se extrapola de las intervenciones de las arterias coronarias. La aspirina en dosis bajas a menudo se toma por el resto de la vida para evitar no solo la trombosis de un segmento tratado sino también otros problemas cardiovasculares. Se desconoce la duración de la acción de clopidogrel para prevenir la oclusión de los segmentos tratados por vía endovascular.
La mayoría de los ensayos clínicos de colocación de stents simples utilizan medicación antiplaquetaria dual durante 1 a 3 meses; sin embargo, los hallazgos de los estudios médicos de pacientes con EAP pueden justificar un tratamiento prolongado. Los ensayos clínicos en Japón muestran que el cilostazol puede minimizar la reestenosis instantánea; sin embargo, esto aún no se ha integrado en las últimas recomendaciones de revascularización del CLI.
La utilidad de la anticoagulación para la derivación de las extremidades inferiores es contradictoria; algunos ensayos demostraron un beneficio sobre la aspirina para la vena autógena frente al conducto protésico y viceversa. La mayoría de los cirujanos reservan la anticoagulación para la trombosis del injerto o las condiciones de hipercoagulabilidad debido al mayor riesgo de hemorragia. No hay ninguna ventaja en combinar clopidogrel y aspirina para la permeabilidad del injerto.
Conclusión
Para la población que envejece, la isquemia crítica de las extremidades (CLI) sigue siendo un proceso patológico prominente. Las recomendaciones rígidas para el cuidado de los pacientes con CLI son ineficaces debido a las dificultades que implica tratar adecuadamente a estos individuos.
El examen vascular, el índice tobillo-brazo (ABI) y una serie de modalidades de imágenes hacen que el diagnóstico de CLI sea simple, pero la mejor manera de tratar a las personas con CLI, ya sea quirúrgica o médicamente, es menos evidente. Esta revisión investigará estas inquietudes y brindará información sobre la mejor atención clínica de los pacientes con CLI.
La revascularización, incluida la cirugía de derivación con o sin tromboendarterectomía, así como los tratamientos endovasculares, brinda la mayor posibilidad de salvar la extremidad para los pacientes que pueden soportar las operaciones quirúrgicas.