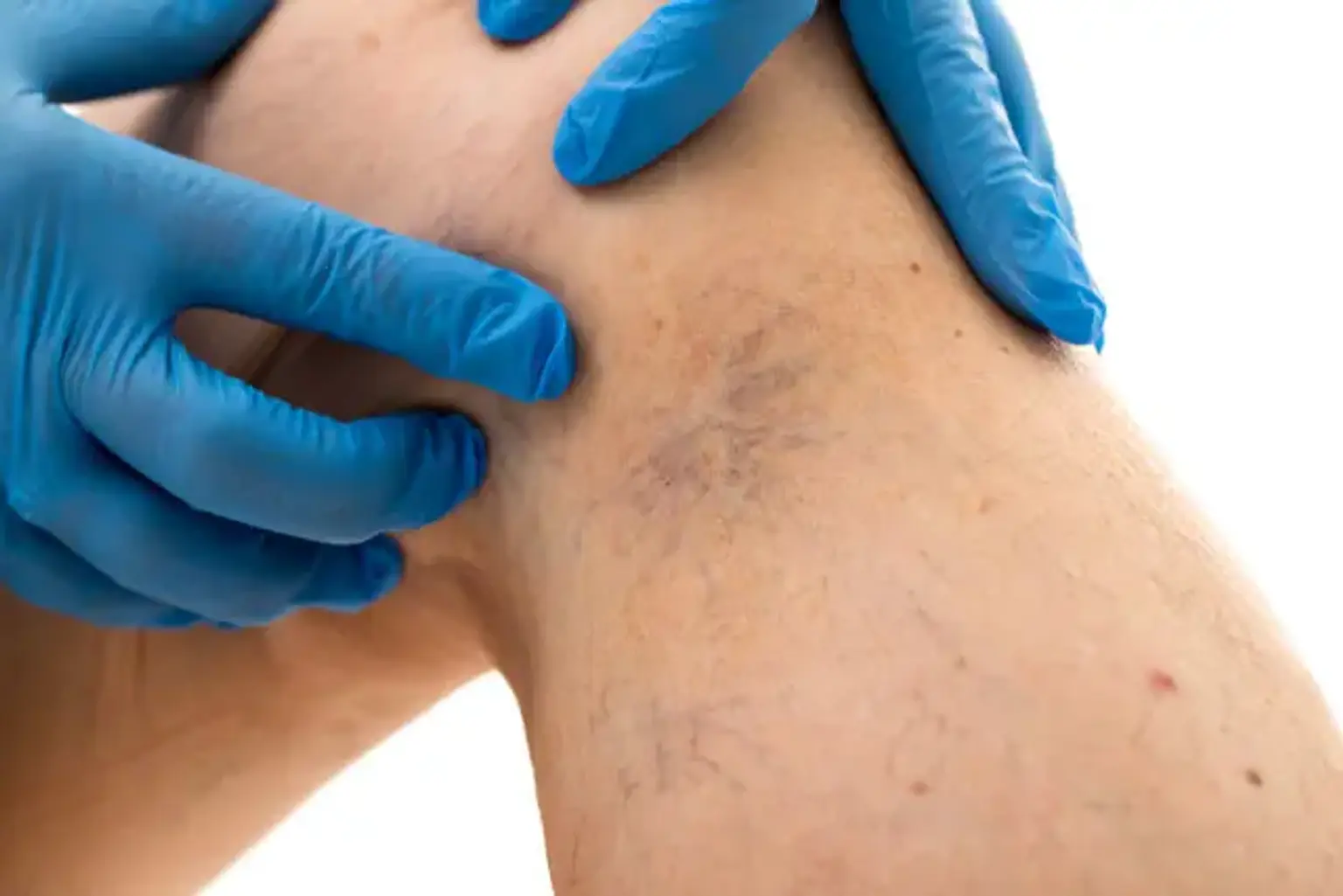
Insuficiencia Venosa Crónica
La insuficiencia venosa crónica (IVC) de las extremidades inferiores puede causar una amplia gama de síntomas, desde problemas estéticos asintomáticos hasta molestias graves. Telangiectasias, venas reticulares, venas varicosas, edema, hiperpigmentación y/o dermatitis, lipodermatoesclerosis, atrofia blanca y ulceración venosa son ejemplos de esto.
Debido a la subestimación de la magnitud y la importancia de la afección, así como al reconocimiento insuficiente de los muchos signos de presentación de problemas venosos primarios y secundarios, la IVC es un problema médico bastante común que los profesionales de la salud a menudo descuidan. Hasta el 55% de las personas tienen circulación venosa anormal en las extremidades inferiores, mientras que la prevalencia informada de CVI depende completamente de los estudios demográficos.
La CVI se asocia con el aumento de la edad, antecedentes familiares, bipedestación prolongada, obesidad, tabaquismo, estilo de vida sedentario, lesiones en las extremidades inferiores, trombosis venosa anterior, existencia de una derivación arteriovenosa, situaciones de niveles elevados de estrógeno y embarazo. De acuerdo con un estudio transversal multiétnico, la prevalencia de CVI en la población asiática es mucho más baja que en los blancos no hispanos, pero se proyecta que la prevalencia de CVI en Corea del Sur aumente debido a la probabilidad de diagnóstico insuficiente de CVI, un aumento en la obesidad. , y una población de mayor edad.
Epidemiología de la insuficiencia venosa crónica
En los Estados Unidos, la CVI es un importante problema de salud pública. Se estima que entre el 3 y el 5 por ciento de todos los estadounidenses sufren síntomas relacionados con la CVI. Se ha estimado que la prevalencia de venas varicosas en la población adulta oscila entre el 9 % y el 62 %, y la mayoría de los estudios muestran reflujo varicoso clínico en aproximadamente el 45 % de la población. Aproximadamente 500.000 personas están afectadas por úlceras por estasis venosa. La tasa media de hospitalización por IVC es de 92 por cada 100.000 pacientes.
Se cree que la insuficiencia venosa es más común en los países occidentalizados e industrializados que en los países subdesarrollados, debido a las variaciones en el estilo de vida y la actividad.
Se estima que entre el 2 y el 3 por ciento de la población adulta sufre ulceración en las extremidades inferiores, y entre el 75 y el 90 por ciento de estas úlceras tienen CVI.
Fisiopatología de la insuficiencia venosa crónica
La hipertensión venosa ambulatoria, que se produce por el reflujo de la válvula venosa, el bloqueo del flujo venoso o ambos, es la causa fisiopatológica más común de la IVC de las extremidades inferiores. En una postura estacionaria sin contracción del músculo esquelético, la presión venosa en la vena del pie puede llegar a 85 a 90 mmHg. Durante la deambulación, esta presión cae a menos de 30 mmHg en un paciente con válvulas venosas sanas. La caída de la presión venosa con los movimientos de las piernas se reduce en un paciente con CVI. Las altas presiones creadas en las venas profundas por la contracción de los músculos de la pantorrilla pueden transmitirse al sistema superficial y a la microcirculación de la piel si las válvulas de las venas perforantes son ineficaces. La hipertensión venosa ambulatoria es el término médico para esta condición. Debido al bloqueo persistente del flujo venoso y al reflujo valvular debido al daño de la válvula,
Causas de insuficiencia venosa crónica
Una válvula puede resultar dañada por un coágulo de sangre en una vena profunda de la pierna (trombosis venosa profunda). La CVI también puede ser causada por falta de actividad. Los períodos largos de estar sentado o de pie también pueden ser dañinos. Esto aumenta la presión en las venas, quizás debilitando las válvulas.
La IVC es más frecuente en mujeres que en hombres. También puede tener una mayor probabilidad si usted es:
- Obeso
- Más de 50 años
- Embarazada o ha estado embarazada anteriormente
- Proveniente de una familia con antecedentes de CVI
- Alguien que ha tenido coágulos de sangre en el pasado
- Una persona que fuma
Síntomas de insuficiencia venosa crónica
La incomodidad, el edema, las venas varicosas y los problemas o ulceraciones de la piel son síntomas de la CVI. Después de estar de pie por mucho tiempo, la incomodidad venosa de la pierna se describe comúnmente como un dolor sordo, palpitaciones o pesadez, o una sensación de presión que se alivia con cualquier tratamiento que reduzca la presión venosa, como elevar la pierna, usar medias de compresión o caminar. La incomodidad en las piernas, por otro lado, está ausente en aproximadamente el 25 % de los pacientes con otros síntomas clínicos de CVI, mientras que es la única característica clínica en aproximadamente el 12 % de los pacientes. Se puede observar sensibilidad en personas con venas varicosas debido a la distensión venosa. La claudicación venosa puede ocurrir en personas que tienen una obstrucción venosa profunda.
La CVI se caracteriza por edema en las piernas. Por lo general, es un pitting y varía mucho según la hora del día y si tiene ortostasis o no. Comienza en el área perimaleolar y sube por la pierna. La insuficiencia cardíaca congestiva, la hipoalbuminemia por síndrome nefrótico o insuficiencia hepática grave, el mixedema por hipotiroidismo y los medicamentos como los bloqueadores de los canales de calcio y las tiazolidinedionas pueden producir edema bilateral en las piernas. También se debe evaluar el lipedema, o edema de las piernas sin fóvea producido por la acumulación de grasa. El lipedema no incluye los pies. Clínicamente, puede ser difícil distinguirlo del linfedema. Uno de los síntomas clínicos del linfedema es el signo de Stemmer. Además, hasta un tercio de los casos de CVI resultan en linfedema secundario; sin embargo, si se trata la CVI subyacente,
Las venas varicosas son venas distendidas, abultadas y superficiales que se vuelven complicadas y más grandes con el tiempo. Los pacientes con venas varicosas suelen estar asintomáticos pero les preocupa el aspecto de sus piernas. Si se produce una tromboflebitis superficial, causan dolor y pueden provocar un sangrado continuo.
El oscurecimiento de la piel, la dermatitis por estasis y la ulceración son ejemplos de alteraciones de la piel. El depósito de hemosiderina provoca hiperpigmentación. La hiperpigmentación no venosa, como la acantosis nigricans o la hemosiderosis, está más extendida y afecta a diversas partes del cuerpo. La psoriasis, la periarteritis nodosa y la dermatitis alérgica deben distinguirse de la dermatitis por estasis. La lipodermatoesclerosis es un tipo de inflamación de la grasa subcutánea. Una úlcera venosa se diferencia de una úlcera isquémica en que las úlceras isquémicas son más profundas y a menudo contienen márgenes gangrenosos o un centro gangrenoso.
Diagnóstico de insuficiencia venosa crónica
Para un diagnóstico preciso de CVI, se requiere un historial médico completo y un examen físico. El examen físico debe realizarse de pie para permitir la máxima distensión de la vena. Se requieren pruebas de diagnóstico, tanto no invasivas como invasivas, para ayudar en el diagnóstico.
Prueba de Brodie-Trendelenburg
La prueba de Brodie-Trendelenburg es útil para determinar si el reflujo es profundo o superficial. Para drenar las venas, el paciente se acuesta con la pierna elevada. Después de indicarle al paciente que se ponga de pie, se aplica un torniquete o compresión manual sobre las venas superficiales y se examinan las venas. Si las varices se llenan en menos de 20 segundos, se producen por insuficiencia venosa superficial. En presencia de insuficiencia venosa profunda (o mixta), por otro lado, las venas varicosas se ensanchan rápidamente.
pletismografía
La pletismografía es una prueba venosa no invasiva que evalúa cada componente probable de la fisiopatología de la CVI, como el reflujo, el bloqueo y la disfunción de la bomba muscular. Es posible determinar el volumen venoso, los tiempos de llenado venoso, el flujo de salida venoso máximo, la capacitancia venosa segmentaria y la fracción de eyección. La pletismografía de impedancia, la pletismografía de galgas extensiométricas, la fotopletismografía y la pletismografía de aire son los cuatro tipos principales de pletismografía. Esta técnica solo se utiliza en entornos académicos u hospitalarios cuando el DHE no proporciona información clara sobre la patogenia de la DVC debido a su complejidad.
Tomografía Computarizada y Venografía por Resonancia Magnética
Aunque los avances en la tomografía computarizada (TC) y la resonancia magnética (RM) han mejorado el examen de la patología venosa, estas técnicas rara vez se utilizan para diagnosticar la CVI y planificar el tratamiento. Para obtener imágenes excelentes y eliminar los artefactos en un sistema venoso específico, es esencial el tiempo adecuado de adquisición de imágenes basado en el tiempo de llenado venoso. Además, estos métodos no dan datos funcionales. Estos enfoques, por otro lado, son particularmente beneficiosos para evaluar lesiones aisladas o complejas en las venas proximales y sus estructuras circundantes, así como para determinar si existe o no una obstrucción intrínseca o extrínseca.
Ultrasonografía venosa dúplex
DUS es el método de diagnóstico más utilizado y eficaz para la IVC, que proporciona información tanto etiológica como anatómica. DUS detecta el bloqueo venoso y el reflujo venoso en venas superficiales y profundas mediante una combinación de imágenes en modo B y Doppler espectral. El uso de DHE asistido por color para visualizar patrones de flujo venoso es beneficioso.
Diagnóstico de obstrucción venosa
La ausencia de flujo, la disminución del aumento, la presencia de un trombo ecogénico dentro de la vena o la incapacidad de la vena para colapsar después de la compresión pueden ser signos de oclusión venosa. En reposo, las venas grandes, incluida la vena cava inferior, los vasos ilíacos, femorales y poplíteos, exhiben un flujo sanguíneo espontáneo. Los cambios respiratorios se reflejan en este flujo. Debido al aumento de la presión intraabdominal durante la inspiración, el flujo normal se detiene durante la inspiración y se reanuda después de la espiración. Debido a su pequeño tamaño, las venas pequeñas, como las venas de la pantorrilla, rara vez muestran un flujo espontáneo. Una restricción proximal o distal al área de evaluación puede causar una falta de flujo espontáneo. Además, una estenosis proximal está indicada por un flujo de alta velocidad esencialmente constante sin variaciones respiratorias. No en una posición de pie, pero en decúbito supino o en una modesta posición de Trendelenburg invertida, debe evaluarse el flujo espontáneo. En las venas normales, el aumento se puede examinar ejerciendo una presión relativamente fuerte sobre la pantorrilla para aumentar el flujo central. Es ideal para apretar y sostener durante alrededor de 0,3 segundos antes de soltar mientras realiza una compresión. Este procedimiento se realiza para confirmar la permeabilidad del segmento de la vena. El aumento se ha atenuado, lo que indica oclusión. La fluctuación de la fuerza de compresión, por otro lado, es una desventaja clave de esta operación. El método más confiable para detectar un trombo intraluminal es la compresibilidad, que se realiza en una vista de eje corto. La mayor velocidad de la sangre de DUS en la vena ilíaca indica estenosis no trombótica. debe evaluarse el flujo espontáneo. En las venas normales, el aumento se puede examinar ejerciendo una presión relativamente fuerte sobre la pantorrilla para aumentar el flujo central. Es ideal para apretar y sostener durante alrededor de 0,3 segundos antes de soltar mientras realiza una compresión. Este procedimiento se realiza para confirmar la permeabilidad del segmento de la vena. El aumento se ha atenuado, lo que indica oclusión. La fluctuación de la fuerza de compresión, por otro lado, es una desventaja clave de esta operación. El método más confiable para detectar un trombo intraluminal es la compresibilidad, que se realiza en una vista de eje corto. La mayor velocidad de la sangre de DUS en la vena ilíaca indica estenosis no trombótica. debe evaluarse el flujo espontáneo. En las venas normales, el aumento se puede examinar ejerciendo una presión relativamente fuerte sobre la pantorrilla para aumentar el flujo central. Es ideal para apretar y sostener durante alrededor de 0,3 segundos antes de soltar mientras realiza una compresión. Este procedimiento se realiza para confirmar la permeabilidad del segmento de la vena. El aumento se ha atenuado, lo que indica oclusión. La fluctuación de la fuerza de compresión, por otro lado, es una desventaja clave de esta operación. El método más confiable para detectar un trombo intraluminal es la compresibilidad, que se realiza en una vista de eje corto. La mayor velocidad de la sangre de DUS en la vena ilíaca indica estenosis no trombótica. Es ideal para apretar y sostener alrededor de 0,3 segundos antes de soltar mientras se realiza una compresión. Este procedimiento se realiza para confirmar la permeabilidad del segmento de la vena. El aumento se ha atenuado, lo que indica oclusión. La fluctuación de la fuerza de compresión, por otro lado, es una desventaja clave de esta operación. El método más confiable para detectar un trombo intraluminal es la compresibilidad, que se realiza en una vista de eje corto. La mayor velocidad de la sangre de DUS en la vena ilíaca indica estenosis no trombótica. Es ideal para apretar y sostener alrededor de 0,3 segundos antes de soltar mientras se realiza una compresión. Este procedimiento se realiza para confirmar la permeabilidad del segmento de la vena. El aumento se ha atenuado, lo que indica oclusión. La fluctuación de la fuerza de compresión, por otro lado, es una desventaja clave de esta operación. El método más confiable para detectar un trombo intraluminal es la compresibilidad, que se realiza en una vista de eje corto. La mayor velocidad de la sangre de DUS en la vena ilíaca indica estenosis no trombótica. es una desventaja clave de esta operación. El método más confiable para detectar un trombo intraluminal es la compresibilidad, que se realiza en una vista de eje corto. La mayor velocidad de la sangre de DUS en la vena ilíaca indica estenosis no trombótica. es una desventaja clave de esta operación. El método más confiable para detectar un trombo intraluminal es la compresibilidad, que se realiza en una vista de eje corto. La mayor velocidad de la sangre de DUS en la vena ilíaca indica estenosis no trombótica.
Diagnóstico de reflujo venoso
La dirección del flujo se utiliza para detectar el reflujo venoso. El reflujo venoso se define como cualquier flujo inverso considerable hacia el pie. En la postura de Trendelenburg inversa, se mide el reflujo venoso. Aunque el flujo inverso se puede ver sin la maniobra de provocación, el reflujo venoso se puede confirmar mediante la maniobra de Valsalva o el aumento comprimiendo la pantorrilla. La presión intraabdominal se eleva mediante la técnica de Valsalva. El objetivo principal de esta prueba es evaluar las características de flujo de los vasos centrales y el funcionamiento de la válvula. La presión hacia abajo se lleva hacia abajo y a través de las válvulas defectuosas hasta que llega a la válvula de trabajo. El reflujo venoso está indicado por el flujo inverso prolongado después del aumento. Sin embargo, el procedimiento de provocación preferible es utilizar un enfoque de inflado y desinflado del manguito con un desinflado rápido del manguito en la postura de pie. Para detectar el reflujo en las venas superficiales y profundas de la pierna, este enfoque brinda datos medibles más uniformes. El término "tiempo de reflujo" se refiere al tiempo que dura el reflujo. Se considera normal tener mucho reflujo venoso. El reflujo patológico se define como un intervalo de tiempo de más de 1,0 segundo en las venas femoral o poplítea, más de 0,5 segundos en los sistemas safenos y más de 0,35 en las perforantes. La duración del reflujo no se corresponde con los signos clínicos, a pesar de que representa la gravedad de la enfermedad. El reflujo patológico se define como un intervalo de tiempo de más de 1,0 segundo en las venas femoral o poplítea, más de 0,5 segundos en los sistemas safenos y más de 0,35 en las perforantes. La duración del reflujo no se corresponde con los signos clínicos, a pesar de que representa la gravedad de la enfermedad. El reflujo patológico se define como un intervalo de tiempo de más de 1,0 segundo en las venas femoral o poplítea, más de 0,5 segundos en los sistemas safenos y más de 0,35 en las perforantes. La duración del reflujo no se corresponde con los signos clínicos, a pesar de que representa la gravedad de la enfermedad.
En individuos con CVI, una evaluación DHE debe revelar patrones estructurales de las venas y anomalías en el flujo sanguíneo venoso en las extremidades. Se debe recopilar la siguiente información: (1) el número, sitio, diámetro y función de las venas perforantes incompetentes; (2) el grado de reflujo en las venas safenas de los muslos y las piernas; (3) otras venas relacionadas que muestran reflujo; (4) el origen del relleno de todas las várices superficiales si no es de las venas ya descritas; (5) venas hipoplásicas, atrésicas, faltantes o extirpadas; y (6) la condición de las uniones safenas.
Ultrasonido Intravascular
Debido a que la ecografía intravascular venosa (IVUS) es mejor que la venografía convencional para las pruebas de diagnóstico morfológico del bloqueo del flujo venoso ilíaco y proporciona una gran ayuda en la colocación precisa de stents venosos, IVUS está ganando rápidamente aceptación en el tratamiento de la enfermedad iliofemoral venosa crónica.
Tratamiento de insuficiencia venosa crónica
Todos los pacientes con signos y/o síntomas de CVI deben recibir un tratamiento conservador al principio. El manejo conservador se basa principalmente en el uso de medias de compresión. La reducción del riesgo, como la pérdida de peso en un paciente obeso, la actividad frecuente de caminar y el abandono del hábito de fumar, debe apoyarse como un manejo conservador en el paciente. Eberhardt y Raffetto brindan un resumen completo del diagnóstico y tratamiento de la CVI.
Medias de compresión
Las medias de compresión están diseñadas para brindar compresión externa gradual a la pierna y contrarrestar las presiones hidrostáticas que causan la hipertensión venosa. Las medias de compresión gradualmente graduadas son preferibles a las medias de compresión sin graduar. Para la profilaxis de la TVP en pacientes quirúrgicos, no hay diferencia entre las medias de compresión graduada hasta la rodilla y hasta el muslo. La mayoría de los pacientes, especialmente los ancianos, toleran mejor las medias hasta la rodilla.
Los pacientes con venas varicosas con o sin edema deben usar medias de compresión con una presión de compresión de 20 a 30 mmHg. Los pacientes con cambios extensos en la piel venosa o una úlcera deben usar medias con una presión de 30 a 40 mmHg. Se recomiendan medias con una presión de 40 a 50 mmHg para personas con úlceras recurrentes.
La terapia de compresión con presión moderada (20 a 30 mmHg) se recomienda para personas con venas varicosas sintomáticas que no son aptas para la ablación de la vena safena, de acuerdo con los estándares de práctica clínica actuales. Además, la terapia de compresión está indicada como tratamiento estándar para la cicatrización de úlceras venosas y como complemento de la ablación de venas superficiales para la prevención de la recurrencia de úlceras.
A pesar de la eficacia clínica de las medias de compresión, tienen una serie de inconvenientes, que incluyen dificultad de aplicación, limitaciones físicas (obesidad) e insuficiencia vascular concurrente. Muchos informes indican que aproximadamente la mitad de los pacientes no pueden mantener la terapia de compresión por una variedad de razones, que incluyen tensión y calor.
Tratamiento médico
Las venas varicosas sintomáticas, el edema del tobillo y las úlceras venosas pueden tratarse con medicamentos venoactivos. Las saponinas (p. ej., extracto de semilla de castaño de indias), gamma-benzopirenos (flavonoides), la fracción de flavonoides purificada micronizada (MPFF) y otros extractos de plantas se han probado con diversos grados de éxito. Aunque el objetivo de utilizar estos medicamentos venoactivos es aumentar el tono venoso y la permeabilidad capilar, el mecanismo de acción exacto es incierto. Según un metanálisis de Cochrane, no hay evidencia adecuada para justificar el uso generalizado de medicamentos venoactivos para tratar la CVI.
La pentoxifilina es un medicamento microcirculatorio que inhibe la liberación de citocinas inflamatorias, la estimulación de los leucocitos y la agregación plaquetaria. La pentoxifilina en combinación con la compresión se relacionó con mayores tasas de curación de las úlceras venosas en un metanálisis de cinco ensayos en relación con la compresión sola, aunque la magnitud del beneficio parece ser pequeña y su importancia en el tratamiento del paciente es incierta. La pentoxifilina en una dosis mayor fue más beneficiosa que en una dosis más baja, sin embargo, la cantidad más alta causó más molestias gastrointestinales.
Para ayudar a aliviar el dolor y la hinchazón causados por la IVC, las guías de práctica clínica actuales recomiendan el uso de fármacos venoactivos como flavonoides, MPFF y extracto de semilla de castaño de Indias, así como el uso de pentoxifilina o MPFF en combinación con compresión para acelerar la cicatrización de las úlceras venosas.
Tratamiento quirúrgico
La terapia quirúrgica abierta de venas varicosas con ligadura alta y extirpación de la VSM combinada con la escisión de venas varicosas grandes ha sido el estándar de atención durante más de un siglo. Esta terapia se realiza en la siguiente secuencia: se realizan incisiones en la ingle y la parte superior de la pantorrilla; la GSV se liga (ligadura alta) por debajo de la SFJ, y se inserta un alambre en la GSV y se avanza distalmente; la parte proximal de la GSV se asegura al alambre y se recupera (desnudando) a través de la incisión de la pantorrilla. La extracción de la GSV por debajo de la rodilla y la extracción de la SSV generalmente no se realizan debido al alto riesgo de lesión nerviosa. Las complicaciones de la ligadura y la extracción incluyen TVP, sangrado, hematoma, infección y lesión nerviosa.
La terapia de ablación endovenosa ha reemplazado principalmente a la ligadura y la extracción tradicionales durante la última década. Pacientes con una gran vena safena distendida y tortuosa ubicada inmediatamente debajo de la piel o agrandamiento aneurismático en la SFJ, pacientes con tromboflebitis previa de la GSV o SSV donde la colocación percutánea de la fibra láser o el catéter de radiofrecuencia puede no ser factible, y pacientes para quienes la cirugía abierta Las técnicas que deben utilizarse para la extracción de venas han sido las únicas indicaciones para este procedimiento.
La flebectomía por punción implica la extirpación o avulsión de las venas varicosas mediante heridas punzantes menores o un orificio de punción producido con una aguja más grande. En el pasado, esta técnica se realizaba de acuerdo con la ligadura y extirpación de la vena safena.
Escleroterapia
La escleroterapia es el procedimiento percutáneo menos intrusivo para cerrar venas indeseables con irritantes químicos. Detergentes (p. ej., morruato de sodio), agentes osmóticos (p. ej., solución salina hipertónica) y agentes químicos (p. ej., tetradecilsulfato de sodio, tetrada de sodio (p. ej., yodo poliyodado). La sustancia esclerosante se administra en forma líquida o en forma de espuma. mezclándolo con aire o CO2/O2.En individuos con CVI, la escleroterapia se puede hacer sola o en combinación con una operación quirúrgica.La escleroterapia se puede usar para tratar telangiectasias, venas reticulares, venas varicosas menores y segmentos venosos con reflujo.
Terapia de ablación térmica endovenosa
La terapia de ablación térmica se divide en dos tipos: EVLA y RFA. Ambos son ultrasonidos guiados. Un generador de calor induce daño térmico local a la pared de la vena, lo que resulta en trombosis y fibrosis, según el mecanismo.
Ambos se usan comúnmente para el reflujo de GSV y han reemplazado a la cirugía debido a una convalecencia y un dolor más breves, a la vez que brindan una eficacia similar. Un metanálisis encontró que EVLA y RFA eran igualmente seguros y efectivos en términos de calidad de vida, bloqueo, tromboflebitis, hematoma y recanalización después de un año. Esta operación requiere el uso de anestesia tumescente. La anestesia tumescente es una técnica para administrar una gran cantidad de anestésico con una dosis baja.
Los hematomas son la consecuencia más común y ocurren en hasta el 80 % de los pacientes que se someten a una terapia de ablación. La trombosis venosa leve, la TVP, las quemaduras en la piel, la pigmentación y el daño a los nervios son efectos posibles pero raros. Después de la ablación de las perforantes, se ha documentado una fístula arteriovenosa.
Implantación de Stent y Valvuloplastia
Algunos pacientes con oclusiones crónicas de la vena ilíaca que tienen síntomas significativos de CVI y que no han respondido a los tratamientos convencionales pueden ser candidatos para procedimientos basados en catéter, como la colocación de stents o el bypass quirúrgico.
La incompetencia valvular se trata con la reconstrucción quirúrgica de las válvulas, que consiste en apretar la válvula por aposición comisural de las venas profundas, y procedimientos de transferencia de válvula, que consisten en insertar un segmento de la válvula permeable de la vena braquial o axilar en la vena con una vena incompetente. válvula.
Conclusión
La IVC de miembros inferiores es una condición médica bastante común que suele estar infradiagnosticada. Es crucial acercarse a los pacientes con sospecha de la enfermedad porque está relacionada con una amplia gama de síntomas. Para evaluar y diagnosticar adecuadamente la fisiopatología de la CVI, se requiere una comprensión profunda de la arquitectura y función venosa normal. Aunque las imágenes estructurales con tomografía computarizada o resonancia magnética pueden ser adecuadas para diagnosticar a un paciente con enfermedad arterial de las extremidades inferiores, se requieren imágenes funcionales con DUS para diagnosticar pacientes con CVI. Las medias de compresión son el estándar de oro para el tratamiento conservador, pero el bajo cumplimiento es un desafío serio. En pacientes sintomáticos, la terapia de ablación venosa se recomienda antes.