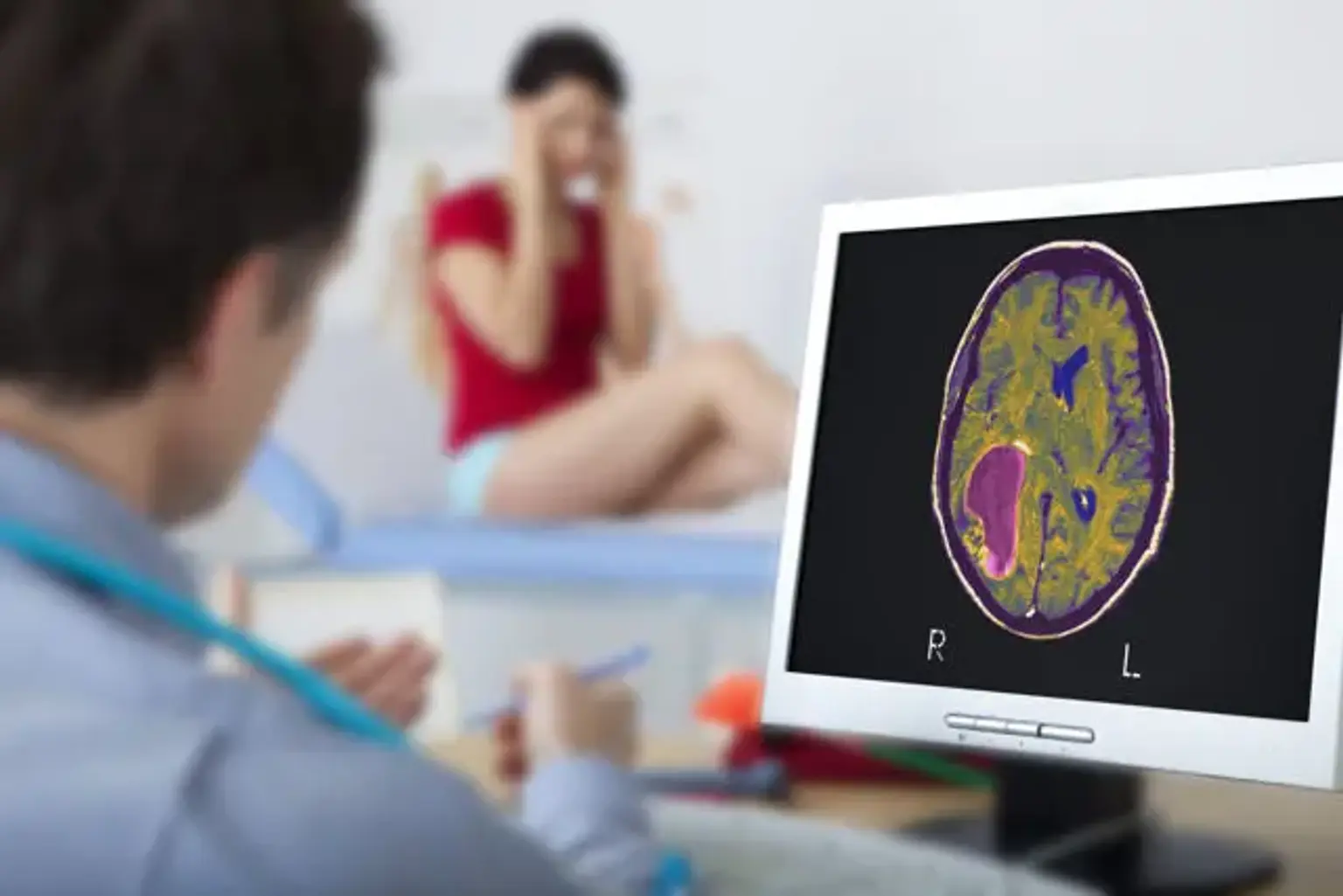
Gliome
Aperçu
Le gliome est le type le plus répandu de tumeur du système nerveux central (SNC) dérivée des cellules gliales. Chaque année, six cas de gliomes sont identifiés pour 100 000 personnes aux États-Unis. Les gliomes sont des tumeurs qui s’infiltrent dans le tissu cérébral environnant de manière très diffuse. Le glioblastome est le type de tumeur cérébrale le plus dangereux, tandis que les astrocytomes pilocytiques sont les moins dangereux.
Auparavant, les gliomes diffus étaient divisés en sous-groupes et grades basés sur l’histopathologie, tels que les astrocytomes diffus, les oligodendrogliomes ou les gliomes / oligoastrocytomes mixtes.
Les gliomes ont récemment été classés à l’aide de marqueurs moléculaires et génétiques. Ces avancées ont des effets pronostiques et thérapeutiques plus spécifiques pour les patients atteints de gliome. Les gliomes sont classés de I à IV en fonction du degré de prolifération indiqué par l’indice mitotique et la présence ou l’absence de nécrose, en plus des marqueurs moléculaires et génétiques.
La thérapie optimale pour un certain patient prend en compte l’emplacement de la tumeur, les symptômes potentiels et les avantages par rapport aux dangers de diverses approches de traitement.
Le traitement du gliome est adapté à chaque patient et peut inclure la chirurgie, la radiothérapie, la chimiothérapie ou l’observation. Une équipe multidisciplinaire est la plus adaptée au traitement des personnes atteintes de tumeurs cérébrales. Les neurochirurgiens, les neuro-oncologues médicaux, les radiothérapeutes et les pathologistes font partie de ceux qui entrent dans cette catégorie.
Incidence et prévalence globale des gliomes cérébraux
Chaque année, environ 80 000 nouveaux cas de tumeur cérébrale primaire sont détectés aux États-Unis. Les gliomes représentent environ un quart de tous les cancers (soit 20 000). Chaque année, environ 12 000 cas de glioblastome sont diagnostiqués (environ 15 % du total des tumeurs cérébrales nouvellement diagnostiquées).
Physiopathologie des gliomes
Les céphalées sont le symptôme initial le plus répandu chez les patients atteints de gliome. On pense que la physiopathologie des céphalées est causée par le développement de tumeurs, ce qui provoque un impact de masse sur les tissus environnants. L’effet de masse, à son tour, provoque une pression dans la microvascularisation, ce qui provoque un œdème. L’effet de masse provoque des signes d’une tumeur cérébrale en fonction de l’emplacement de la tumeur dans le cerveau.
Les tumeurs du lobe frontal, par exemple, peuvent causer des troubles du comportement, tandis que les tumeurs dominantes du lobe temporal peuvent causer des troubles de la parole réceptive. D’autres symptômes d’effets de masse comprennent des nausées, des vomissements et des changements visuels. Les convulsions sont le deuxième symptôme le plus répandu. Les crises sont causées par une irritation tumorale du cortex cérébral, ce qui entraîne des crises localisées ou généralisées.
D’autres symptômes des gliomes comprennent des picotements, une faiblesse et des difficultés à se déplacer. Dans de rares circonstances, les patients peuvent apparaître dans un état comateux en raison de saignements à l’intérieur de la tumeur, entraînant un syndrome d’engagement aigu.
Il a été révélé que les gliomes présentaient un certain nombre d’altérations génétiques acquises (plutôt que héréditaires). Au début de la maladie, la protéine suppresseur de tumeur p53 (p53) est mutée. p53 est le « gardien du génome », assurant que l’ADN est répliqué correctement lors de la duplication de l’ADN et des cellules et détruisant la cellule (apoptose) si l’ADN est altéré et ne peut pas être réparé. D’autres mutations peuvent persister lorsque p53 est modifié.
Un autre gène suppresseur de tumeur, l’homologue de la phosphatase et de la tensine (PTEN), est supprimé ou modifié. Le récepteur du facteur de croissance épidermique, un facteur de croissance qui encourage généralement la division cellulaire, est augmenté et provoque une division excessive des cellules. Ces mutations, lorsqu’elles sont combinées, provoquent une division cellulaire incontrôlable, caractéristique du cancer. On a découvert que les mutations de l'IDH 1 et de l'IDH 2 faisaient partie du processus et étaient associées à un mauvais pronostic.
Qui risque d’avoir un gliome?
N’importe qui peut développer un gliome, mais les facteurs suivants peuvent augmenter votre risque:
- Âge : Les gliomes sont plus fréquents chez les personnes âgées (plus de 65 ans) et les enfants (moins de 12 ans).
- Ethnicité: Les Blancs peuvent être plus susceptibles de développer des gliomes que les autres races.
- Antécédents familiaux : Certains troubles génétiques héréditaires peuvent augmenter le risque de gliomes.
- Genre: Les gliomes sont légèrement plus fréquents chez les hommes que chez les femmes.
- Exposition aux rayonnements ou aux toxines : Une exposition répétée ou prolongée à des rayonnements ou à certains produits chimiques peut augmenter le risque.
Causes des gliomes cérébraux
Troubles héréditaires :
Les causes précises des gliomes sont inconnues. Des troubles héréditaires tels que les neurofibromatoses (types 1 et 2) et le complexe de la sclérose tubéreuse ont été liés à leur développement. Différents oncogènes peuvent travailler ensemble pour causer des gliomes.
Régime:
Certaines études sur les compléments alimentaires et vitaminiques semblent suggérer que les composés alimentaires N-nitrosamine peuvent avoir un impact sur le risque de cancers du cerveau chez l’enfant et chez l’adulte. Dans certaines enquêtes, les chercheurs ont découvert que les patients atteints de tumeurs cérébrales (ou leurs mères) ingéré plus d’aliments de guérison (également connus sous le nom de Curing) que les groupes témoins. Les adultes atteints de gliome étaient plus susceptibles de manger un régime riche en aliments salés et faible en fruits et légumes riches en vitamine C, ainsi qu’un régime riche en nitrites et faible en vitamine C. L’impact a été plus fort chez les hommes que chez les femmes.
Cependant, le schéma de risque accru avec une consommation accrue d’aliments salés et un risque réduit avec une consommation accrue de fruits, de légumes et de vitamines antioxydantes est cohérent avec d’autres études sur le cancer qui montrent qu’une consommation accrue de légumes et éventuellement de fruits est associée à une diminution du risque de cancer.
Radiation:
Il n’y a aucune preuve claire d’une relation entre les gliomes et le rayonnement électromagnétique des téléphones cellulaires. On pensait que c’était concevable, malgré le fait que diverses grandes études n’ont trouvé aucune preuve concluante, comme l’a déclaré l’Institut national du cancer des NIH.
Cependant, d’autres recherches sont menées pour obtenir des preuves plus solides et confirmer qu’il n’y a pas de relation (le plus récent communiqué de presse de l’Institut national des sciences de la santé environnementale des NIH a discuté d’une étude en cours avec des résultats légèrement positifs, bien qu’il semble qu’il puisse y avoir eu des problèmes avec le groupe témoin mourant prématurément).
Infection par le cytomégalovirus:
Certaines recherches ont montré que les patients ayant des glioblastomes sont infectés par le CMV, ce qui soulève la possibilité que cela puisse accélérer la formation de tumeurs. Cependant, il s’agit d’un point de vue controversé, car les enquêtes approfondies ultérieures n’ont pas réussi à démontrer un lien entre l’infection virale et le développement du gliome. Des recherches antérieures pourraient avoir été influencées par des artefacts de coloration d’anticorps faussement positifs, selon des preuves.
Polymorphismes héréditaires des gènes de réparation de l’ADN:
Le risque de gliome est augmenté par les polymorphismes germinaux (héréditaires) dans les gènes de réparation de l’ADN ERCC1, ERCC2 (XPD) et XRCC1. Cela suggère que les gliomes se forment à la suite d’une réparation altérée ou inadéquate des dommages à l’ADN. Les dommages à l’ADN sont probablement une cause primaire importante du développement du cancer en général.
Des dommages excessifs à l’ADN peuvent entraîner des mutations par synthèse de translésion. Une réparation incomplète de l’ADN peut également entraîner des changements épigénétiques ou des épimutations. De telles mutations et épimutations peuvent fournir à une cellule un avantage prolifératif, qui peut éventuellement conduire à la croissance du cancer par sélection naturelle.
Autres causes
Bien que certaines études aient montré que les agriculteurs présentaient un risque plus élevé de gliome que la population générale, l’exposition aux animaux d’élevage ou au fumier n’est pas liée au gliome. Des études ultérieures n’ont pas montré de lien entre l’agriculture et les gliomes; de même, il existe des données contradictoires entre les enseignants et le gliome. Les architectes, les géomètres, les employés du commerce de détail, les bouchers et les ingénieurs ont une plus grande incidence de gliomes, selon des statistiques plus cohérentes. La majorité des enquêtes ont conclu qu’il est peu probable que l’exposition aux pesticides soit une cause de gliome, tandis qu’un petit nombre d’études ont identifié un lien.
Classifications des gliomes
Les gliomes sont classés en trois catégories en fonction des caractéristiques des cellules phénotypiques : les astrocytomes, les épendymomes et les oligodendrogliomes. Sur la base de la forme cellulaire, de l’activité mitotique et du marqueur moléculaire, ces gliomes cellulaires sont en outre classés comme des tumeurs de bas grade, atypiques et de haut grade. Le système de notation de l’Organisation mondiale de la santé (OMS) utilise des marqueurs moléculaires dont les conséquences prédictives et thérapeutiques ont été trouvées. Les gliomes sont classés par type de cellule, par grade et par emplacement :
Par type de cellule :
Les gliomes sont nommés en fonction du type spécifique de cellule avec lequel ils partagent des caractéristiques histologiques, mais pas nécessairement d’où ils proviennent. Les principaux types de gliome sont:
- Épendymomes : Provient de cellules épendymaires qui tapissent les cavités ventriculaires et le canal central de la moelle épinière. Ceux-ci sont assez répandus chez les patients pédiatriques.
- Astrocytomes: Il est dérivé des astrocytes et peut être encapsulé, en conservant des limites distinctes entre les cellules normales et malignes, ou infiltrant, indiquant un grade avancé. Les enfants ont tendance à avoir de faibles scores, mais les jeunes adultes et les patients plus âgés ont tendance à avoir des scores élevés.
- Oligodendrogliomes : Développé à partir de cellules oligodendrocytes. Les adultes sont plus susceptibles de les avoir parce qu’ils sont moins infiltrants que les astrocytomes.
- Gliome du tronc cérébral : se développer dans le tronc cérébral
- Gliome du nerf optique : se développe dans ou autour du nerf optique
- Gliomes mixtes: tels que les oligoastrocytomes, contiennent des cellules de différents types de glie
Par le score:
Les gliomes sont en outre classés en fonction de leur grade, qui est déterminé par une analyse pathologique de la tumeur. La classification OMS des tumeurs du système nerveux central est utilisée pour l’examen neuropathologique et le diagnostic des échantillons de tumeurs cérébrales.
- Gliomes biologiquement bénins [grade I de l’OMS]: ils présentent un risque relativement faible et peuvent être enlevés chirurgicalement en fonction de leur emplacement.
- Gliomes de bas grade [grade II de l’OMS]: ils sont bien différenciés (non anaplasiques); ceux-ci ont tendance à présenter des tendances bénignes et à présager un meilleur pronostic pour le patient. Cependant, ils ont un taux uniforme de récidive et d’augmentation de grade au fil du temps et doivent donc être classés comme malins.
- Haut grade [grades III à IV de l’OMS] : les gliomes sont indifférenciés ou anaplasiques ; ceux-ci sont malins et portent un pronostic plus sombre.
Le système de classement de l’Organisation mondiale de la santé (OMS) pour l’astrocytome est le plus fréquent, avec des tumeurs notées de I (maladie la moins avancée - meilleur pronostic) à IV (maladie la plus avancée - pronostic sombre).
Par emplacement :
Les gliomes sont classés selon qu’ils sont situés au-dessus ou au-dessous de la tente du cerveau, une membrane du cerveau. La tente du cerveau est l’espace qui sépare le cerveau (ci-dessus) du cervelet (en bas).
- Le supratentorial est au-dessus de la tente, dans le cerveau, et se trouve principalement chez les adultes (70%).
- L’infratentorial est en dessous de la tente, dans le cervelet, et se trouve principalement chez les enfants (70%).
- Les tumeurs pontines se trouvent dans les ponts du tronc cérébral. Le tronc cérébral est divisé en trois sections (pons, mésencéphale et moelle allongée); les ponts régulent les processus clés, y compris la respiration, ce qui rend la chirurgie extrêmement dangereuse.
Signes et symptômes des gliomes
Les symptômes les plus fréquents des gliomes cérébraux comprennent des maux de tête, des nausées, des vomissements, des convulsions et, dans des cas plus avancés, une faiblesse ou une altération de l’état mental. L’examen neurologique de ces personnes peut être normal ou peut montrer divers degrés de faiblesse focale, des déficiences sensorielles ou, dans un cas grave, un état mental modifié en raison d’un effet de masse aigu causé par l’élargissement de la tumeur.
Évaluation des patients atteints de gliomes cérébraux
Dans le cadre d’un examen historique et physique impliquant des tumeurs cérébrales, les tests d’imagerie suivants sont appropriés:
- Tomodensitométrie (TDM) de la tête: Une enquête appropriée doit être effectuée pour évaluer les anomalies intracrâniennes aiguës telles que les saignements, l’œdème et l’asymétrie dans le tissu cérébral.
- Résonance magnétique cérébrale (IRM) : Les caractéristiques des tumeurs cérébrales sont déterminées dans cette enquête sensible. Les cancers de bas grade ne se réhaussent pas normalement, mais les tumeurs de haut grade le font. De plus, l’IRM est une excellente technique pour déterminer l’étendue de l’œdème cérébral. Une IRM du cerveau aide à la planification du traitement et à la réponse aux traitements chirurgicaux, de radiothérapie et de chimiothérapie.
- Radiographie du thorax: Les patients qui viennent d’être diagnostiqués avec une tumeur au cerveau ont besoin d’un bilan métastatique approprié en fonction de leurs antécédents et de leur examen physique. Les patients ayant de longs antécédents de tabagisme, par exemple, peuvent avoir besoin d’une radiographie pulmonaire. Si une masse est observée sur une radiographie pulmonaire, elle doit être étudiée plus avant à l’aide d’une tomodensitométrie du corps ou d’une tomographie par émission de positons (TEP) pour déterminer le site principal probable de la maladie métastatique.
Comment les gliomes cérébraux sont-ils traités?
Le traitement des gliomes cérébraux est déterminé en fonction de l’emplacement, du type de cellule et du degré de malignité. Le traitement est souvent une combinaison de chirurgie, de radiothérapie et de chimiothérapie. Le traitement par radiothérapie et témozolomide concomitant a entraîné un temps de survie plus long.
La radiothérapie a été administrée 5 jours par semaine pendant 6 semaines, totalisant 60 Gy. Le témozolomide a été administré quotidiennement tout au long de la radiothérapie à une dose de 75 mg par mètre carré de surface corporelle par jour. À la fin du traitement, six cycles de témozolomide ont été administrés pendant cinq jours tout au long de chaque cycle de 28 jours.
La radiothérapie peut prendre la forme d’un rayonnement externe ou d’une méthode de radiochirurgie stéréotaxique. Les tumeurs de la moelle épinière peuvent être traitées chirurgicalement et par radiothérapie. Le témozolomide est un médicament chimiothérapeutique qui peut être facilement administré en ambulatoire et qui traverse avec succès la barrière hémato-encéphalique. Certains gliomes peuvent bénéficier d’un traitement d’immunothérapie.
Des essais récents ont utilisé des bloqueurs angiogéniques tels que le bévacizumab en conjonction avec la chimiothérapie conventionnelle pour traiter le gliome récurrent de haut grade, avec des résultats prometteurs.
Pronostic des gliomes
Le pronostic des gliomes est déterminé par le grade (tel que déterminé par la classification de l’Organisation mondiale de la santé) de la tumeur avec laquelle le patient se présente. Toute tumeur qui est au-delà du grade I de l’OMS (c’est-à-dire une tumeur maligne par opposition à une tumeur bénigne) a généralement un pronostic de mortalité qui varie de plusieurs années (grade II / III de l’OMS) à des mois (grade IV de l’OMS). Le pronostic peut également être proposé en fonction du sous-type cellulaire, ce qui peut avoir un effet sur le pronostic.
Faible grade:
Le pronostic des cancers de bas grade est légèrement meilleur. Les patients atteints de gliome de bas grade sont 17 fois plus susceptibles de mourir que les individus comparables dans la population générale. Le taux de survie relative à 10 ans ajusté selon l’âge était de 47 %. Une recherche a révélé que les personnes atteintes d’oligodendrogliome de bas grade ont une durée de vie médiane de 11,6 ans, tandis qu’une autre a trouvé une survie médiane de 16,7 ans. Malheureusement, 70% des tumeurs de bas grade (grade II de l’OMS) se développeront en tumeurs de haut grade d’ici 5 à 10 ans.
Haut grade:
Les astrocytomes anaplasiques et le glioblastome multiforme sont inclus dans cette catégorie. Alors que les gliomes anaplasiques (grade III de l’OMS) ont une survie globale médiane d’environ 3 ans, le glioblastome multiforme a une survie globale médiane lugubre de 15 mois.
Par rapport à l’absence de radiothérapie postopératoire, la radiothérapie quotidienne conventionnelle postopératoire améliore la survie chez les personnes présentant un excellent bien-être fonctionnel et un gliome de haut grade. Par rapport à la radiothérapie conventionnelle, la radiothérapie hypofractionnée a une efficacité similaire pour la survie, en particulier chez les personnes âgées de 60 ans et plus atteintes de glioblastome.
Gliome pontique intrinsèque diffus :
Le gliome pontique intrinsèque diffus affecte principalement les enfants, dont la plupart ont entre cinq et sept ans. Le GPID a une durée de survie médiane de moins de 12 mois. La chirurgie pour enlever la tumeur n’est généralement pas possible ou conseillée dans le cas du GPID. Ces tumeurs, par définition, s’infiltrent dans le tronc cérébral de manière diffuse, se développant entre les cellules nerveuses normales. Une chirurgie agressive peut nuire gravement aux structures neurologiques nécessaires au mouvement des bras et des jambes, au mouvement des yeux, à l’alimentation, à la respiration et même à la conscience.
Conclusion
Les gliomes sont des tumeurs qui commencent dans les cellules gliales du cerveau ou de la colonne vertébrale. Les gliomes représentent environ 30% de tous les cancers du cerveau et du système nerveux central et 80% de toutes les tumeurs cérébrales malignes.
Selon la recherche, les altérations de l’ADN provoquent le développement de tumeurs malignes du cerveau et de la moelle épinière telles que les gliomes. Les cellules reçoivent des instructions sur la façon de se développer et de se reproduire. Les mutations, ou les altérations de l’ADN dans nos gènes, peuvent provoquer une prolifération incontrôlable des cellules.
Les patients souffrant de cette condition peuvent présenter des symptômes et des signes non spécifiques tels que l’aphasie, des problèmes cognitifs, des difficultés à marcher, des étourdissements, des maux de tête, une faiblesse ou un engourdissement d’un côté du corps), des nausées et des vomissements, des anomalies de la personnalité ou du comportement, et même des convulsions.
En présence d’une anamnèse et d’un examen physique évocateurs de tumeurs cérébrales, la tomodensitométrie et l’IRM sont les modalités d’imagerie de choix.
Pour la majorité des individus, la chirurgie est la première ligne de traitement pour un gliome. Si la tumeur est facilement accessible, un chirurgien peut être en mesure de l’enlever complètement. Les gliomes, d’autre part, peuvent être difficiles à éliminer complètement, en particulier dans les parties difficiles à atteindre ou fragiles du cerveau.
Après la chirurgie, d’autres thérapies telles que la chimiothérapie et la radiothérapie doivent être administrées. Ce sont des traitements adjuvants, ce qui signifie qu’ils éliminent toutes les cellules cancéreuses résiduelles ou les morceaux de tumeur après la chirurgie. Cependant, si la tumeur est inopérable, les médecins peuvent recommander la chimiothérapie ou la radiothérapie comme thérapies primaires.