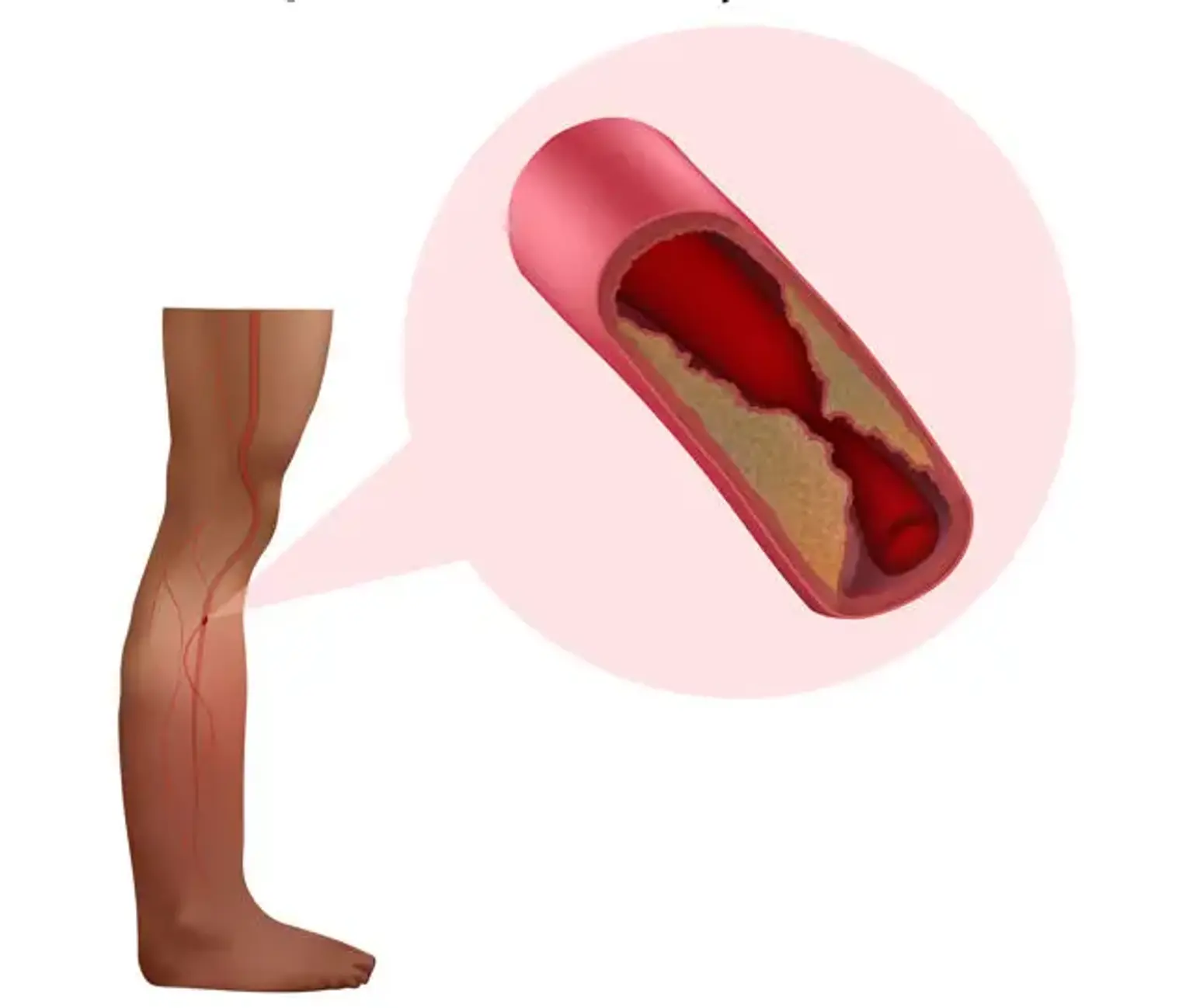
Maladie artérielle périphérique
Aperçu
La maladie artérielle périphérique (MAP) est une affection athéroscléreuse chronique et progressive qui entraîne un blocage partiel ou complet du système vasculaire périphérique. L’AOMI affecte habituellement l’aorte abdominale, les artères iliaques, les membres inférieurs et, en de rares occasions, les membres supérieurs. L’AOMI touche plus de 200 millions de personnes dans le monde, et son importance mondiale augmente à mesure que les gens vivent plus longtemps et sont exposés à davantage de facteurs de risque.
Les patients atteints de MAP ont une présentation et des antécédents variés de la maladie, certains restant asymptomatiques et d’autres évoluant vers une ulcération artérielle, une claudication, une ischémie des membres au repos et une amputation des membres.
L’AOMI est une maladie cardiovasculaire comparable, avec des événements cardiovasculaires mortels et non mortels à haut risque tels que l’infarctus du myocarde et les accidents vasculaires cérébraux qui se produisent souvent. La MAP est une maladie systémique grave et progressive qui nécessite une collaboration interprofessionnelle pour améliorer les résultats des patients.