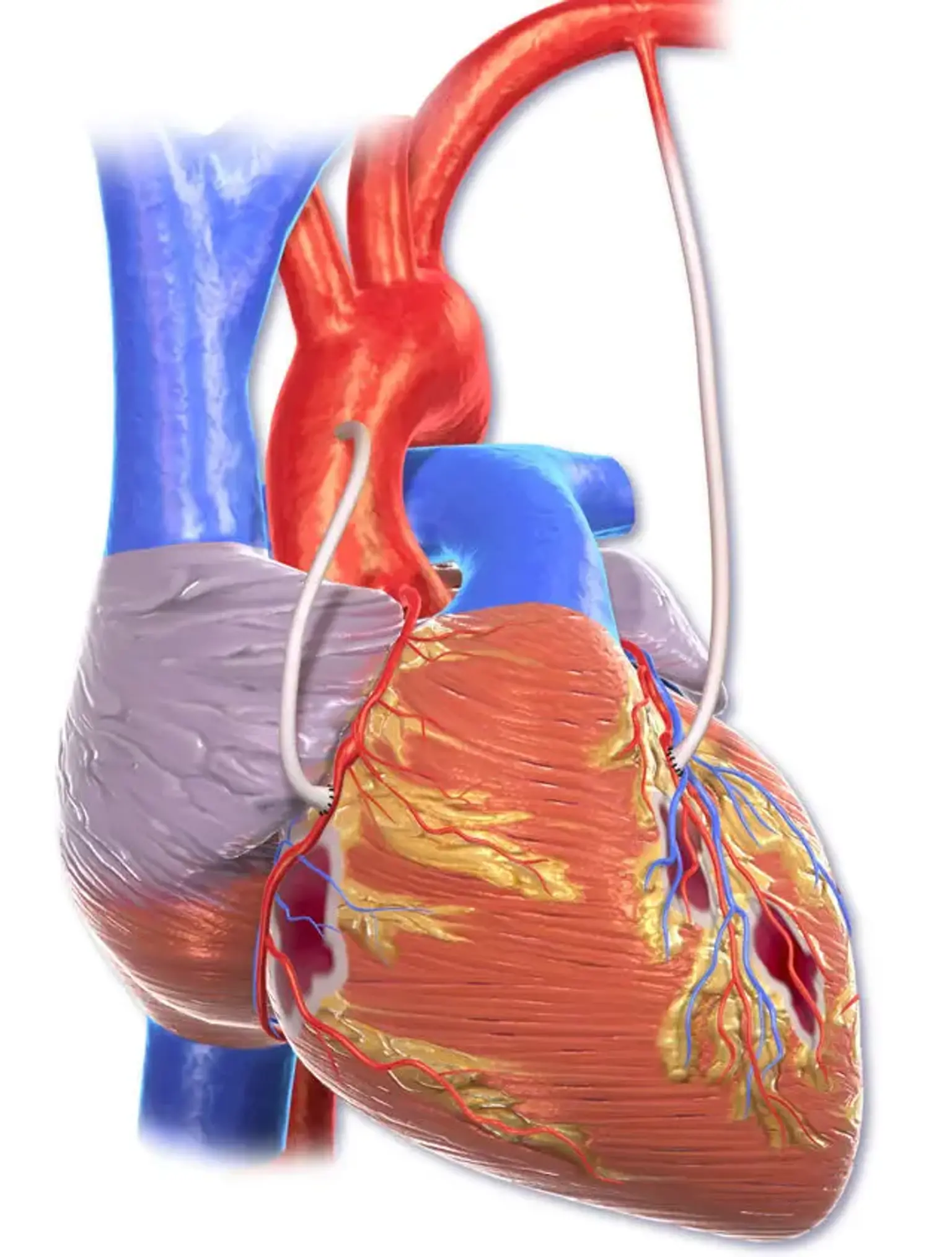
Koszorúér-bypass graft (CABG)
Áttekintés
A CABG egy jelentős sebészeti eljárás, amelynek során a beteg koszorúerében lévő atheromatosus elzáródásokat megkerülik a betakarított vénás vagy artériás csatornák segítségével. A bypass helyreállítja az ischaemiás szívizom véráramlását, helyreállítja a funkciót és az életképességet, és enyhíti az anginás tüneteket.
Évente közel 400 000 CABG-műveletet végeznek, így ez a leggyakrabban elvégzett nagy sebészeti műtét; a műtéti trendek azonban eltolódtak, mivel az alternatív választások, például az orvosi terápia és a perkután koszorúér-beavatkozás (PCI) népszerűbbé váltak.
CABG műtét
A koszorúér-bypass oltás (CABG) egy olyan eljárás, amelyet az életminőség javítására és a szívvel kapcsolatos halálozás minimalizálására használnak a koszorúér-betegségben (CAD) szenvedő egyéneknél. A CAD a legnagyobb halálok az Egyesült Államokban és az iparosodott világban, évente 16,5 millió (20 éves) amerikai felnőttet érint.
Az Egyesült Államokban évente 530 989 halálesetért felelős, és a CAD hosszú távú következményei, beleértve a bal kamrai diszfunkciót és a szívelégtelenséget, 2030-ra várhatóan közel 8 millió 18 év feletti személyt érintenek.
A CABG műtétet először az 1960-as években hajtották végre azzal a céllal, hogy tüneti enyhülést, jobb életminőséget és jobb várható élettartamot biztosítsanak a CAD-betegek számára. Az orvosi kezeléshez képest a CABG az 1970-es évekre növelte a túlélési arányt a multivessel betegségben szenvedő és a bal oldali fő betegségben szenvedőknél.
Az új CAD kezelési paradigma olyan szívcsapat megközelítést igényel, amelyben a kardiológus és a szívsebész együtt értékeli a koszorúér-angiográfiát, és a beteg számára a legjobb elérhető alternatívát nyújtja a koszorúér-revascularizációhoz, legyen szó perkután koszorúér-sztent vagy CABG beültetéséről. Jelenleg az átlagos CABG-beteg idősebb, korábban perkután koszorúér-beavatkozáson (PCI) esett át, és sokkal több társbetegsége van.
E kockázatok ellenére a CABG továbbra is a modern orvostudomány történetének egyik legfontosabb sebészeti művelete, amely valószínűleg több életet mentett meg, és jelentősebb tüneti enyhülést kínált, mint bármely más nagy műtét. Az új, minimálisan invazív megközelítések, az anesztézia és az intenzív osztályok (ICU) kezelésének áttörései, valamint a technológiai fejlődés új magasságokba emelik ennek a műveletnek a határait.
Általánosságban elmondható, hogy kétféle CABG sebészeti eljárás létezik: a szivattyún és a szivattyún kívül, azzal a különbséggel, hogy a szivattyún lévő CABG kardiopulmonális bypass áramkört és letartóztatott szívet használ a munkához. A bal belső emlőartériát (LIMA) és az alsó végtagokból származó saphenous vénás graftokat (SVG) általában bypass graft csatornákként alkalmazzák.
A jobb belső emlőartéria (RIMA), a radiális artéria és a gastroepiploic artéria néhány további átültethető csatorna. A graftok fajtáját és helyzetét a beteg anatómiája és az elzáródott artériák elhelyezkedése határozza meg. A LIMA-t általában a bal elülső csökkenő (LAD) artériába oltják, míg a többi vezetéket a többi elzáródott artériához való hozzáférésre használják.
Anatómia és fiziológia
Két fő koszorúér látja el a szív szívizomát: a bal fő koszorúér és a jobb koszorúér (RCA). A bal fő koszorúér jellemzően egy rövid szakasz, amely a bal elülső csökkenő (LAD) és a circumflex artériákra oszlik. A LAD átlós ágakra oszlik, míg a circumflex artéria tompa marginális ágakra oszlik. Az RCA két ágra oszlik: a hátsó csökkenő artériára (PDA) és a marginális ágakra.
Attól függően, hogy melyik artéria látja el az interventricularis septumot és a PDA-t, a koszorúér-keringés bal-domináns, jobb-domináns és társ-domináns rendszerekbe sorolható. A circumflex artéria bal-domináns rendszerben látja el a PDA-t, míg az RCA a PDA-t jobb-domináns rendszerben látja el. A domináns vaszkuláris ellátás mellett a PDA-t egyszerre táplálja az RCA és a circumflex artériák.
A koszorúér-artériák bármelyikének elzáródása a szívizom-perfúzió megfelelő hiányát, az ischaemiát eredményezi, és ha nem kezelik, tartós infarktust vagy szívkárosodást okozhat.
Történelmi információk
1912-ben Alexis Carrel munkájáért fiziológiai és orvostudományi Nobel-díjat kapott. Az angina pectoris és a koszorúér-szűkület közötti kapcsolat ismerete lehetővé tette számára, hogy kutyamodellben anasztomózzon egy nyaki artériás szegmenst a csökkenő mellkasi aortától a bal koszorúérig.
Arthur Vineberg, egy figyelemre méltó kanadai sebész, az 1940-es évek végén súlyos angina pectoralisban szenvedő betegeknél a bal belső mellkasi (emlő) artériát közvetlenül az elülső bal kamra szívizomába ültette át. Meglepő módon néhány személynek jelentős tünetcsökkenése volt a műtét eredményeként.
Sabiston 1962-ben a Duke Egyetemen végezte el az első tervezett saphenous vénás bypass eljárást a koszorúér-revascularizációhoz. Kolessov 1964-ben a bal belső mellkasi (emlős) artériát használta a bal elülső leszálló artéria megkerülésére kardiopulmonális bypass nélkül, Carpentier pedig 1973-ban úttörő szerepet játszott a radiális artériás oltványok CABG csatornaként történő használatában.
A CABG az 1970-es években és az 1980-as évek elején virágzott a CAD egyedüli kezeléseként. Az elvégzett CABG-műtétek száma az 1980-as és 1990-es években a perkután koszorúér-stentelés kialakulásával, bevezetésével és széles körű elterjedésével csökkent. Számos multicentrikus vizsgálat, amely összehasonlította a CABG-t a jelenlegi stentkezeléssel, egyértelműen megállapította a CABG előnyeit, különösen akkor, ha olyan speciális betegjellemzőket is magukban foglalnak, mint a cukorbetegség, a multikuláris CAD és az ischaemiás kardiomiopátia.
A CABG indikációi
Ha a fő koszorúerek bármelyikében magas fokú elzáródások vannak, és / vagy a perkután koszorúér-beavatkozás (PCI) nem tudta megszüntetni az elzáródásokat, a CABG-t gyakran javasolják. A 2011-es ACCF/AHA irányelvek 1. osztályú ajánlásai a következők:
- A bal oldali fő betegség nagyobb, mint 50%
- 70% -ot meghaladó háromerű koszorúér-betegség proximális LAD érintettséggel vagy anélkül
- Kéthajós betegség: LAD és egy másik fő artéria
- Súlyos, több mint 70% -os szűkület egy olyan betegnél, akinek jelentős anginás tünetei vannak a maximális gyógyszeres kezelés ellenére
- Az ischaemiával összefüggő kamrai tachycardiával járó hirtelen szívhalál túlélőjében az egyik érrendszeri betegség több mint 70% volt.
A CABG egyéb indikációi a következők:
- Angina letiltása (I. osztály)
- Ischaemia, amely a gyógykezelésre refrakter nem-ST szegmensemelkedésű miokardiális infarktus (NSTEMI) összefüggésében áll fenn (I. osztály)
- Rossz bal kamrai funkció, de életképes, nem működő szívizom az anatómiai defektus felett, amely revascularizálható.
- Klinikailag súlyos CAD 70 százalékos vagy annál nagyobb szűkülettel egy vagy több érben, valamint refrakter angina a gyógyszeres kezelés és a PCI ellenére
- Klinikailag súlyos, 70% -os vagy annál nagyobb szűkület 1 vagy több erben a hirtelen szívmegállás túlélőinél, akikről azt gondolják, hogy ischaemiás kamrai aritmia okozta
- Klinikailag súlyos CAD 50% vagy annál több szűkülettel 1 vagy több érben olyan betegeknél, akik más okokból szívműtéten esnek át (pl. Szelepcsere vagy aortaműtét)
A CABG sürgősségi kezelésként végezhető ST-szegmens emelkedési MI (STEMI) beállításában, ha a perkután koszorúér-beavatkozás (PCI) nem volt lehetséges, vagy ha a PCI sikertelen volt, és a gyógyszeres kezelés ellenére a szívizom jelentős részét érintő, hosszan tartó fájdalom és ischaemia áll fenn.
A CABG túlélési előnyét növelő tényezők a következők:
- A bal kamrai ejekciós frakció legfeljebb 45%
- Cukorbetegség
- Ischaemiás mitralis regurgitáció
- PCI-hiba, akut MI-vel vagy anélkül (AMI)
Ellenjavallatok
A CABG nem ajánlott tünetmentes egyéneknek, akiknél alacsony az MI vagy a halál kockázata. Azok a betegek, akiknek kevés haszna származik a koszorúér-revascularizációból, szintén ki vannak zárva.
Bár az idősebb kor nem ellenjavallat, a CABG-t óvatosan kell megközelíteni az időseknél, különösen a 85 év felettieknél. Ezek az egyének hajlamosabbak a CABG-t követő perioperatív problémákra is. A bonyolult CAD-ben szenvedő betegeknél a multidiszciplináris kardiális csapat megközelítése, amely hangsúlyozza a megosztott döntéshozatalt, kritikus fontosságú ahhoz, hogy a beteg a lehető legnagyobb esélyt kapja a sikeres revascularizációs tervre.
CABG eljárás
A koszorúér-betegséget észlelő koszorúér-angiográfia mellett a betegnek különböző vizsgálatokat kell végeznie a műtét előkészítéséhez. Laboratóriumi vizsgálatokra, például teljes vérképre (CBC), metabolikus panelekre, beleértve a májfunkciós teszteket, véralvadási panelekre és hemoglobin A1c-re lesz szükség. Más vizsgálatokra is szükség lehet, beleértve az elektrokardiogramot (EKG), az echokardiográfiát, a carotis ultrahangvizsgálatot, a mellkasi röntgenfelvételt és esetleg az alsó végtagok CT mellkasát vagy vénás feltérképezését.
Az aritmiák, például a pitvarfibrilláció elkerülése érdekében a perioperatív időszakban gyakran adnak preoperatív gyógyszereket, például béta-blokkolókat. Korábban az aszpirint a műtét előtt 5-7 nappal visszatartották, de most azt javasolják, hogy kezdjék el vagy folytassák a műtét előtt.
Amikor a beteg megérkezik a kórházba, intravénás hozzáférést hoznak létre, és megvizsgálják gyógyszereiket és preoperatív tesztjeiket. A hajat eltávolítják a műtéti helyekről, és a beteg klórhexidin-fürdőt kap.
Berendezés
Ez a jelentős sebészeti műtét nemcsak a legtöbb más sebészeti beavatkozáshoz szükséges felszerelést teszi szükségessé, hanem számos speciális berendezést is, például egy kardiopulmonális bypass gépet melegítő-hűtő eszközzel a vér melegítésére és hűtésére.
Személyzet
A műtétet egy speciális szív- és érrendszeri sebészeti csapat végzi, amely kiterjedt képzéssel és tapasztalattal rendelkezik ezeknek a komplex betegeknek a gondozásában. A csapat a kardiothoracikus sebészből és asszisztenseikből, aneszteziológusokból, ápolókból, sebészeti technikusokból és perfúziós szakemberekből áll
Kockázatértékelés
Kockázati modelleket dolgoznak ki az izolált CABG utáni 30 napos halálozás előrejelzésére. A szívsebészetben leggyakrabban használt előrejelzők az Euroscore rendszer és a Mellkassebészek Társasága (STS) 2008-as szívsebészeti kockázati modellje. Az életkor, a korábbi MI, a PVD, a veseelégtelenség, a hemodinamikai állapot és az EF mind közös tényezők ebben a két kiemelkedő modellben. A nyolc legfontosabb tényező, köztük az életkor, a műtéti élesség, a reoperatív állapot, a kreatininszint, a dialízis, a sokk, a krónikus tüdőbetegség és az EF, magyarázza az STS modell variációjának 78 százalékát.
Premedikáció
A premedikáció célja a szívizom oxigénigényének csökkentése a szívfrekvencia és a szisztémás artériás nyomás csökkentésével, valamint a szívizom véráramlásának növelése értágítók segítségével. A következő gyógyszereket kell szedni a műtét időpontjáig:
- Béta-blokkolók, kalciumcsatorna-blokkolók és nitrátok
- Aszpirin
A beadott szerek a következők:
- Temazepam azonnal preoperatív
- Midazolám, egy kis intravénás (IV) adag a műtőben az artériás vonal behelyezése előtt
Minden betegnek 2 egység vért (enyhe esetekben) vagy 6 egység vért, friss fagyasztott plazmát és vérlemezkéket kell kapnia egymással (összetett esetekben). A tranexaminsav (1 g bolus a műtéti bemetszés előtt, majd 400 mg/óra infúzió a műtét alatt) megfontolható a posztoperatív mediastinalis vérzés és a szükséges vérkészítmények mennyiségének (azaz vörösvértestek és friss fagyasztott plazma) minimalizálása érdekében.
Érzéstelenítés
A szívműtétet leggyakrabban mély általános érzéstelenítéssel, endotracheális csővel végzik. A neuraxiális blokád következő két típusát ritkán használják kiegészítőként:
- Intratekális opioid infúzió
- Mellkasi epidurális érzéstelenítés (általában alacsony dózisú helyi érzéstelenítő/opioid infúzió)
Technika
A folyamat akkor kezdődik, amikor a beteg a műtőben van, és csatlakozik a szabványos monitorokhoz. Az általános érzéstelenítés kiváltása előtt az aneszteziológus beilleszthet egy artériás vonalat a beteg vérnyomásának invazív monitorozására. Az általános érzéstelenítés és a beteg intubálása után a vénás hozzáférés központi vonalát és egy pulmonalis artériás katétert lehet behelyezni, majd egy transzesophagealis echokardiográfiás jelátalakítót kell behelyezni.
A műtéti bemetszés előtt a pácienst sterilen előkészítik és behúzzák, és időtúllépést adnak be. A sebész mediális sternotomiát végez, hogy felkészüljön a LIMA eltávolítására csatornaként való felhasználásra. A képzett asszisztens, általában orvosasszisztens, nővér első asszisztens vagy más sebész, nyílt vagy videóval támogatott eljárásokat alkalmaz, hogy egyszerre távolítsa el a saphenous vénát az egyik vagy mindkét lábról.
A megfelelő csatornák megszerzését követően a sebész antikoagulációt, leggyakrabban heparint ír elő, amelyet a kardiopulmonális bypass (CPB) előkészítésére kell beadni. A beteg aortája és szíve központilag kannulált, és a csövek a kardiopulmonális bypass áramkörhöz vannak csatlakoztatva. A CPB beindulását követően a szívet magas káliumtartalmú kardioplegiával állítják le, hogy a sebész anasztomózhassa a betakarított vezetékeket a koszorúér-artériákhoz, távol az akadályoktól.
A koszorúér-bypass oltás csatornáiként artériák vagy vénák alkalmazhatók (CABG). A Cleveland Clinic egyik kulcsfontosságú publikációja bizonyította a bal belső mellkasi (emlős) artéria oltásának túlélési előnyeit a bal elülső csökkenő koszorúérbe sok évvel ezelőtt. Ez még mindig igaz; Valójában, ha lehetséges, a kétoldalú belső mellkasi (emlős) artériás oltás jelentős hosszú távú túlélési előnyt kínál. Erős bizonyítékok azt mutatják, hogy a vénás graft helyett egy extra artériás graft használata jobb hosszú távú eredményekkel jár.
A nagyobb saphenous véna és ritkán a rövid saphenous véna a leggyakrabban használt vénás graftok, míg a belső mellkasi (emlős) artéria a leggyakrabban használt artériás transzplantáció. A radiális artériás graftot az 1990-es években vezették be újra a klinikai gyakorlatba, és 10 éves követés után továbbra is magas, 80% -os vagy annál nagyobb átjárhatósági arányt mutat, különösen, ha a cél érrendszeri szűkület meghaladta a 90% -ot.
A saphenous vénás graftok hátránya, hogy átjárhatóságuk idővel csökken: 10-20% -uk a műtét után 1 évvel blokkolódik technikai hibák, trombózis és intimális hiperplázia miatt. A vénás graftok további 1-2 százaléka a műtétet követően 1-5 évvel, 6-10 évig pedig évente további 4-5 százalékkal. A vénás graft elzáródását, amely egy vagy több évvel a CABG után következik be, vénás graft ateroszklerózis okozza, amelyet neointimális hiperplázia kialakulása kísér.
A saphenous vénás graftoknak csak 50-60% -a szabadalmaztatott 10 évvel a műtét után, és csak a fele mentes az angiográfiás ateroszklerózistól. A betegeknek élethosszig tartó vérlemezke-ellenes gyógyszert kell szedniük, jellemzően napi alacsony dózisú (81 mg) aszpirin formájában, a megfelelő másodlagos profilaxis részeként.
A belső mellkasi (emlő) artériás graftok a saphenous vénás graftokkal ellentétben az idő múlásával fenntartják az átjárhatóságot. A belső mellkasi (emlős) artériás graftok több mint 90% -a 10 év után még mindig szabad. Amikor a bal elülső koszorúér-artériát megkerülik, a bal belső mellkasi (emlős) artériát kell használni csatornaként.
A vezetékek a proximális aortában keletkező új ostia-hoz kapcsolódnak, miután a sebész anasztomózist végzett a disztális részeken. A kardioplegiát ezután leöblítik, a szív elkezd összehúzódni, és a sebész megvizsgálhatja a graftokat a véráramlás és a kompetencia, valamint az anasztomózis helyeiről származó vérzés szempontjából. A mellkasot ezután szegycsonthuzalokkal zárják le, és a beteget a kritikus ellátási egységbe helyezik a hemodinamikai stabilitás monitorozására és extubálására.
Szövődmények
A stroke, a sebfertőzés, a graft elégtelenség, a veseelégtelenség, a posztoperatív pitvarfibrilláció és a mortalitás mind a CABG lehetséges következményei. A jelentések szerint a CABG utáni stroke aránya 1% és 2% között mozog, a beteg jellemzőitől és a stroke kockázati tényezőitől függően, amelyek magukban foglalják az előrehaladott életkort, a korábbi stroke-ot, az aorta ateroszklerózist, a perifériás artériás betegséget, a perioperatív pitvarfibrillációt és a cukorbetegséget.
A szegycsonti sebfertőzés aránya 1% körül van, és olyan kockázati változók befolyásolják, mint az elhízás, a cukorbetegség, a krónikus obstruktív tüdőbetegség (COPD) és a művelet hossza.
A saphenous vénás graft (SVG) sikertelensége valószínűleg a műtétet követő 30 napon belül következik be, és számos ok okozza, mint például a véna mérete és túlzott hossza, a disztális lefolyás és a rossz áramlás, valamint a hiperkoagulálhatóság és a trombózis. A CABG-t követő ismételt angiográfiával az SVG-meghibásodás aránya akár 25% is lehet. Alternatív megoldásként az artériás graftok, mint például a bal belső emlőartéria (LIMA) és a radiális artériás graftok hosszabb ideig tartanak, és átjárhatósági arányuk 10 év után eléri a 90% -ot.
A CABG-t követő posztoperatív veseelégtelenség aránya 2% és 3% között változik, 1% -uk dialízisre szorul. A preoperatív vesebetegség, az öregség, a cukorbetegség, a műtét típusa, az LV diszfunkció és a sokk mind kockázati tényezők. Bár egyetlen gyógyszerről sem bizonyították be határozottan, hogy csökkentené a CABG által kiváltott vesekárosodás arányát, a szivattyún kívüli CABG előnyt jelenthet a pumpán lévő CABG-vel szemben.
A pitvarfibrilláció a CABG-t követő első 5 napban meglehetősen gyakori, aránya 20% és 50% között mozog, és fokozott morbiditással jár, beleértve az embóliás stroke és a halál nagyobb kockázatát. A leghatékonyabb stratégia a posztoperatív pitvarfibrilláció előfordulásának minimalizálására bizonyítottan a béta-blokkolókkal és talán amiodaronnal végzett preoperatív terápia.
A CABG-t követő perioperatív mortalitás kockázata a komorbiditásoktól, a műtét sürgősségétől és az eljárás elvégzésének helyszínéül szolgáló intézmény esetszámától függően 1% és 2% között változik.
Eredmények
Az artériás oltás és stentelés korszakából származó 6055 beteg bevonásával végzett hat randomizált klinikai vizsgálat metaanalízise szerint a koszorúér-bypass oltás (CABG) a hosszú távú halálozás és a miokardiális infarktus (MI) csökkenéséhez, valamint az ismételt revascularizációk csökkenéséhez vezet multivessel koszorúér-betegségben szenvedő betegeknél, függetlenül attól, hogy a betegek cukorbetegek-e vagy sem.
Nyolc randomizált vizsgálat metaanalízise 3612 felnőtt cukorbeteg és multierekciós koszorúér-betegségben (CAD) szenvedett beteg bevonásával megállapította, hogy a CABG 5 év után 33% -kal csökkentette az összes okból bekövetkező halál kockázatát a PCI-hez képest. Amikor a CABG-ben szenvedő betegeket összehasonlították a csupasz fém sztenteket vagy gyógyszer-eluáló sztenteket kapó betegek alcsoportjaival, a relatív kockázatcsökkenés nem változott lényegesen.
Az 51 és 70 év közötti betegek és a 70 évnél idősebbek, akik ugyanabban az időszakban kaptak CABG-t, jelentősen rosszabbul teljesítettek a túlélés szempontjából. A krónikus vesebetegség, az alacsony bal kamrai ejekciós frakció, a perifériás érrendszeri betegség vagy a krónikus obstruktív tüdőbetegség voltak a vezető kockázati tényezők az összes okból bekövetkező halál szempontjából.
Az ischaemiás szívelégtelenség sebészeti kezelése (STICH) kiterjesztési tanulmány (STICHES) arra a következtetésre jutott, hogy a bármilyen okból bekövetkező halálozás, a szív- és érrendszeri okokból bekövetkező halál, valamint a szív- és érrendszeri okokból bármilyen okból vagy kórházi kezelésből eredő halálozás aránya szignifikánsan alacsonyabb volt azoknál a betegeknél, akik CABG-n estek át és medicare-ben részesültek.
Ezenkívül jelentős kórházi szintű eltérés volt a STEMI CABG arányokban, és a CABG-t gyakran az angiográfiát követő 1-3 napon belül végezték el. Azok a betegek, akik CABG-t kaptak, és azok, akiknek nem volt hasonló kórházi halálozási aránya.
6637 nem védett bal fő CAD-ben szenvedő beteg metaanalízise kilenc vizsgálatból 14 év alatt (2003-2016) megállapította, hogy a gyógyszer-eluáló sztentekkel rendelkező PCI összehasonlítható szív- és minden okból bekövetkező halálozással járt, de csökkent a stroke aránya és nagyobb az ismételt revascularizáció aránya. Jelentős kedvezőtlen szív- és cerebrovascularis események esetén a CABG vs PCI-t előnyben részesítő tendencia nem ért el statisztikai szignifikanciát.
A CABG utáni életminőség és a PCI szempontjából a multivessel CAD esetében mindkét eljárás javítja az angina gyakoriságát. Az eljárás után 1 hónappal azonban a PCI-betegek általában gyorsabban felépülnek és jobb rövid távú egészségi állapotuk van, mint a CABG-betegeknek, azonban 6 hónapos és hosszabb utókezeléskor a CABG-betegek jobb angina-enyhüléssel és életminőséggel rendelkeznek, mint a PCI-betegek.
Következtetés
A koszorúér-bypass graft (CABG) egy sebészeti technika, amelyet a szívkoszorúér-betegség kezelésére használnak az életminőség javítása és a szívvel kapcsolatos halálozás csökkentése céljából. Átirányítja a vért a fő artériák szűkített vagy elzárt szakaszai körül, növelve a véráramlást és az oxigénellátást a szívbe.