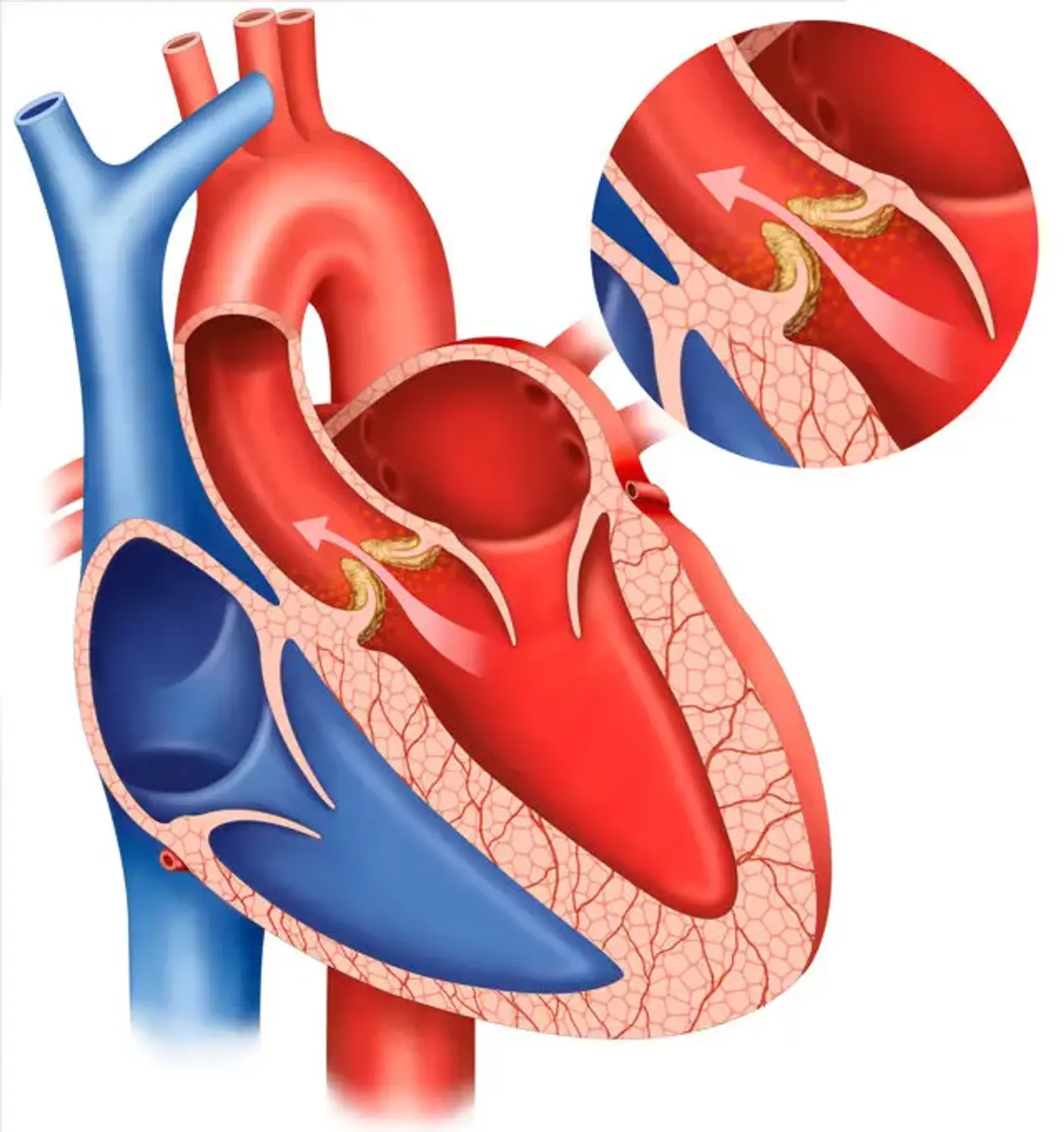
大動脈弁置換術(AVR)
概要
大動脈弁逆流症(AVR)は、左心室(LV)への拡張期大動脈血逆流として定義されます。急性ARは、重大な肺水腫と低血圧を特徴とし、外科的緊急事態と見なされます。慢性的な重度のAVRは、LV体積と圧力過負荷の組み合わせをもたらします。収縮期高血圧と広い脈圧を伴い、バウンディングパルスなどの末梢の身体的症状を説明します。
収縮期高血圧は後負荷の増加を引き起こし、進行性のLV拡張と収縮期機能障害につながります。心エコー検査はAVRの最も重要な診断テストです。これにより、AVRの発生源、ARの重症度、およびLVのサイズ、機能、血行動態への影響を特定できます。
慢性的な重度のAVRを持つ多くの個人は、正常なLV機能で症状なしで何年も生きることができます。これらの個人は手術を必要としませんが、症状の発症またはLV拡張/機能障害について注意深く監視する必要があります。LV駆出率が55%を下回るか、LV拡張末期の寸法が55mmに達する前に、手術を検討する必要があります。
重大な併存疾患または他の禁忌がない限り、症状のある人は手術を受けるべきです。血管拡張薬ベースの薬物治療の主な目標は、LV機能が正常な無症候性の患者の手術を延期するか、手術が不可能な患者を治療することです。
血管拡張薬治療の目的は、収縮期動脈圧を大幅に低下させることです。将来の治療法は、LVリモデリングと線維症を回避するために分子経路に集中する可能性があります。
AVRの疫学
慢性AVRの頻度と急性AVRの発生は不明のままです。健康な人でも、心エコー検査によるAVRの追跡は一般的な観察です。女性よりも男性に大きな影響を与えるようです(13%対8.5%)。AVRの有病率は年齢とともに上昇し、50歳以降に最も一般的です。米国におけるAVRの頻度は4.9〜10%と推定されています。
AVRはどのように発症し、臨床症状を引き起こしますか?
AVRは左心室の容積の増加を誘発する。LV拡張末期容積の増加は、LV拡張および偏心肥大をもたらす。これにより、より高いストロークボリュームを排出することができます。AVR患者のLVによって排出される総脳卒中量は、有効脳卒中量と逆流量の合計です。その結果、AVRはより大きなプリロードにリンクされています。ラプラスの法則によれば、LV拡張はLV収縮期緊張を上昇させる。これは、総前脳卒中量の増加によって引き起こされる収縮期血圧の上昇とともに、より大きな後負荷をもたらします。
LV拡張と肥大の組み合わせは、LV機能を補います。しかし、時間が経つにつれて、壁の肥厚は血行動態負荷に追いつかず、収縮機能と駆出率が低下します。
LVは非補償性であるため、コンプライアンスが低下し、LV拡張末期の圧力と体積が高くなります。左心房、肺動脈くさび、肺動脈、右心室(RV)、右心房圧は疾患の進行とともに上昇しますが、有効(前方)心拍出量は減少します。肺のうっ血により、呼吸困難、整形呼吸、発作性夜間呼吸困難などの心不全の症状が生じます。
LV質量が大きいほど、心筋酸素の使用を増やす必要があります。さらに、冠動脈灌流圧が低下する。この結果として心筋虚血および労作性胸部不快感が生じる。
LVの代償メカニズムは、急性重度のARの個人では、逆流性の体積負荷に対応するのに十分な速さで発達しません。LV拡張期血圧の急激な上昇は、突然の肺水腫と心原性ショックを引き起こす可能性があります。LV容積と圧力の急激な急激な上昇の結果として、拡張期僧帽弁閉鎖不全症でさえ発症する可能性があります。
AVRの考えられる原因は何ですか?
ARは、大動脈弁尖、大動脈根や輪などの支持構造、あるいはその両方の異常によって引き起こされる大動脈弁尖の異常によって引き起こされます。
原発性弁疾患:
一般的な原因には、石灰性大動脈弁疾患が含まれ、これは通常、大動脈弁狭窄症(AS)に関連していますが、ある程度のARに関連している可能性があります。チラシの解剖学的構造を変える感染性心内膜炎。上行大動脈の裂傷または裂傷は、交連支持の喪失による大動脈尖脱出につながる。
ARは、弁の不十分な閉鎖または脱出による先天性二尖大動脈弁(BAV)によって引き起こされる可能性がありますが、ASはBAVのより一般的な結果です。先天性ARのあまり一般的ではない原因には、単回交連弁および四肢弁、ならびに開窓弁破裂が含まれる。
大動脈尖脱は、心室中隔欠損症(VSD)の特定の人々に発症します。リウマチ性疾患はAV尖頭の線維性浸潤を引き起こし、それが収縮を引き起こし、収縮期中の正常な開放および拡張期中の閉鎖を妨げる。交連の融合により、ASとAVRが混在する可能性があります。リウマチ性僧帽弁疾患は、リウマチ性大動脈弁疾患を伴うことが多い。
進行性AVRは、粘液腫性大動脈弁変性症によっても引き起こされる可能性があります。二次AVRは、膜性大動脈下狭窄症によって引き起こされるAVリーフレットの肥厚および瘢痕化から生じる可能性がある。AVRは、経皮的大動脈バルーン弁切開術および経カテーテル大動脈弁置換術の合併症としても文書化されています。
弁膜AVRは、生体人工弁の構造劣化の結果としてより普及しつつあります。大動脈尖頭剥離または破裂は、急性AVRのまれな原因です。AVRの他のあまり一般的ではない原因には、全身性エリテマトーデス、高安病、ホイップル病、関節リウマチ、強直性脊椎炎、ジャコウド関節症、梅毒、クローン病、食欲抑制薬などがあります。
原発性大動脈根疾患:
大動脈環状拡張によりAV弁尖が分離し、AVRが発生します。加齢に伴う変化、マルファン症候群と頻繁に関連している嚢胞性内側壊死、または骨形成不全症はすべて、大動脈根に変性変化を引き起こす可能性があります。強直性脊椎炎、ベーチェット病、乾癬性関節炎、反応性関節炎に関連する関節炎、潰瘍性大腸炎、再発性多発性軟骨炎、巨細胞性動脈炎はすべて大動脈根拡張に関連しています。
重度の慢性全身性高血圧症は、大動脈輪を拡張し、AVRを進行させる可能性があります。逆行性大動脈解離は、大動脈輪を含み、乱し、AVRをもたらす可能性がある。
AVR患者の症状と身体的兆候は何ですか?
病歴別:
慢性AVRの症状は徐々に、時には数十年にわたって現れます。労作性呼吸困難、オルソプネア、発作性夜間呼吸困難、狭心症、動悸、頭のドキドキはすべて症状です。夜間狭心症は、睡眠中に心拍が遅くなり、動脈拡張期血圧が危険なほど低いレベルに低下すると発生します。
身体検査による:
収縮期高血圧と拡張期血圧の低下の結果として、AVRは脈圧の拡大に関連しています。頂端LVインパルスは超動的であり、横方向および下方向に変位する。強い収縮期のスリルは、心臓の付け根、胸骨上ノッチの近く、および頸動脈の上に感じられることがあります。巨大な前方ストローク量と低い大動脈拡張期圧がそれを誘発します。
S1は正常ですが、S2は隆起(大動脈根が拡張するため)または下降(大動脈弁尖が肥厚している場合)のいずれかです。高周波、吹き飛ばされた、デクレシェンド拡張期の雑音は、左胸骨境界の3番目の肋間ギャップで最もよく聞こえます。ARの雑音は、患者が前かがみになっているときの呼気の終わり近くに検出しやすくなります。
雑音は、しゃがむまたは等尺性の活動で増加し、血圧を下げる手順で減少します。中等度のAVRでは、この雑音は早期拡張期であり、重度のAVRを伴うホロ拡張期に進行します。
脈圧の拡大による重度の慢性AVR結果の末梢徴候を以下に説明します。
- オースティンフリントのつぶやき: 低音のゴロゴロとの中期拡張期の雑音は、頂点で最もよく聞こえました。ARの噴流による僧帽弁の早期閉鎖が原因と考えられています。
- ベッカーサイン: 検眼鏡を通した網膜動脈の目に見える脈動の存在
- ビスフェリエンスパルス: 早期拡張期の血液の逆流による二相性脈拍
- コリガンサイン: 突然の膨張と迅速な崩壊を伴うウォーターハンマーパルス。
- ド・ミュッセのサイン: 動脈脈動を伴うそれぞれで頭を揺らします。
- デュロジエのサイン: 収縮期雑音は、大腿動脈が近位に圧迫されると聞こえ、拡張期雑音は聴診器で遠位に圧迫されたときに聞こえます。
- ゲルハルトサイン: 脾臓の脈動は脾腫の存在下で検出されます。
- 丘の標識:下肢の血圧が上肢の血圧よりも高い
- メインサイン: 腕を上げると15mmHgを超える拡張期血圧の低下
- ミュラーサイン: 口蓋垂の収縮期脈動
- クインケサイン: 毛細管脈動(爪の先端に圧力がかかったときに爪の根元で最もよく見られる紅潮と漸色)。
- ローゼンバッハのサイン: 肝臓の脈動
- トラウベサイン: 大腿動脈で聞こえる「ピストルショット」収縮期および拡張期の音が急上昇
- これらの同名の兆候は、さまざまな感度と特異性を持っていることに注意する必要があります。これらの徴候の発現に対する大動脈弁閉鎖不全症の重症度の影響に関する証拠はまばらである。
急性AVRでは、症状と身体的所見は脳卒中量の減少に関連しています。患者は頻脈、頻呼吸、および肺水腫を呈します。急性ARの身体検査所見は慢性ARのそれよりも微妙であるため、患者が呼吸困難やショックを呈した場合の診断は困難です。迅速な診断には、高い疑いの指標が不可欠です。
AVRはどのように評価および診断されますか?
大動脈弁閉鎖不全症の精密検査には、以下の検査が含まれます。
- 心エコー検査
主な診断技術は心エコー検査であり、大動脈弁の構造、大動脈根の解剖学的構造、およびLVを正確に評価します。
慢性AVRは左心室拡張を特徴としています。後の段階まで、EFの低下または収縮末期次元の増加によって示されるように、収縮期機能は正常である。
重度のAVRでは、中心ジェット幅がLV流出路(LVOT)の65%を超え、逆流体積が60 mL /拍動、有効逆流開口部面積が0.30を超え、逆流率が50%、大静脈収縮が0.6 cmを超え、近位下行胸部大動脈に拡張期流の逆転があります。
重度のAVRの個人では、AVRジェットの連続波ドップラープロファイルは、急速な減速時間を示します。高い勾配は、大動脈とLVの間の圧力が拡張期中により早く等しくなることを意味します。
急性および慢性AVRの両方で、逆流ジェットの衝撃によって引き起こされる前僧帽弁尖の高周波拡張期羽ばたきが見られることがあります。
ベッドサイド経胸壁2次元およびMモード心エコー検査(TTE)および/または経食道心エコー図(TEE)を使用して、急性AR(TE)を診断できます。
- 心臓磁気共鳴
心臓MRI(CMR)は、音響窓が不十分なために心エコー検査にもかかわらず、さらなる評価を必要とする個人に特に有用な代替診断方法です。これは、LV収縮末期の容積、拡張期容積、および質量を決定するための最も正確な非侵襲的方法です。上行大動脈の順行性および逆行性の流量を使用して、AVRの重症度を正確に推定できます。
- 心臓カテーテル検査
臨床症状と非侵襲的画像との間に不一致がある場合、血管造影はAVR、血行動態、および冠状動脈構造の重症度に関する情報を提供できます。それは造影剤を大動脈根に素早く注入し、左右の前斜め突起を記録することを伴います。
AVRはどのように扱われますか?
急性AVR:
重度の急性AVRには緊急手術が推奨されます。治療は制限されており、患者を一時的に安定させるためにのみ利用されます。前方の流れを高めるために、静脈内利尿薬と血管拡張薬(ニトロプルシドナトリウムなど)を使用して後負荷を軽減します。心拍出量を改善するために、ドーパミンまたはドブタミンなどの変力剤が利用され得る。ベータ遮断薬は、COを低下させ、心拍数を遅くし、LVが拡張期充満する時間を増やすため、回避されます。大動脈内バルーンカウンターパルセーションは推奨されません。
抗生物質の開始後5〜7日間血行動態的に安定している活動性感染性心内膜炎によって引き起こされる急性AVRの患者では、手術が延期される場合があります。しかしながら、血行動態の不安定性または膿瘍の発生が起こるならば、処置は実行されなければならない。
慢性AVR:
疾患経過全体のモニタリング:軽度または中等度のAVRと正常な心臓サイズの無症候性の個人は、12か月または24か月ごとに臨床的および心エコー的に評価する必要があります。.持続的な重度のAVRおよび正常なLV機能を有する無症候性患者は、6ヶ月ごとに評価されるべきである。
医学療法: AVRでは治療の適応はほとんどありません。血管拡張薬治療は、慢性AVRに関連する全身性動脈性高血圧症の治療に使用する必要があります。.ジヒドロピリジンカルシウムチャネル遮断薬またはアンジオテンシン変換酵素阻害薬/アンジオテンシン受容体遮断薬(ACEI / ARB)を使用することが好ましい。
- 慢性ARの病期分類:慢性ARは、心臓弁膜症患者の管理に関する2020 ACC / AHAガイドラインに基づいて4つの段階に分類されます。
- ステージA: ARのリスクがある患者。これらの患者には血行力学的影響や症状はありません。.
- ステージB: 患者は軽度から中等度のARを持っていますが、LV収縮機能は正常であり、臨床症状はありません。
- ステージC: 無症候性の重度のAR。 患者はARジェット幅が65%以上になります 左心室流出路(LVOT)。ステージCは、LV収縮機能に応じてさらに次のように細分類されます。
- C1: 通常のLVEF(>50%)および軽度から中等度のLV拡張(LVESD <50 mm)。
- C2: 重度のLV拡張(LVESD >50 mm)でLVEF(<50%)が低下しました。
- ステージD: 症候性の重度のAR。 心エコー検査での重度のARジェットの所見。LVEF は正常または異常のいずれかです。症状には、労作性呼吸困難、狭心症、または心不全が含まれます。
外科的治療: ARの治療ガイドラインは、2020年の米国心臓協会/米国心臓病学会の推奨事項に基づいています。大動脈弁置換術(AVR)は、重度の症候性慢性ARおよびLV収縮不全を伴う重度の無症候性慢性AVR(LVEF 50%)の個人に好ましい治療法です。
AVRは、無症候性で正常なLV機能(LVEF 50%)を有するが、実質的なLV拡張(LVESD指数>25 mm / m2またはLVESD>50 mm)を有する重度のAVRを有する個人にとっても実行可能な選択肢である。
AVRは、無症候性で安静時のLV収縮機能が正常(LVEF 50%、ステージC1)であるが、手術の外科的リスクが最小限であることを考えると、LV拡張が有意に増加している(LV拡張末期寸法>65 mm)重度のAVR患者に対しても調査できます。
ガイドラインは、症状、左心室収縮機能障害、または左心室拡張が発症した場合に弁膜手術を推奨しているという事実にもかかわらず、慢性AR患者における無症候性心筋機能障害および不可逆性心筋線維症の証拠を示す新しい研究は、介入のタイミングに関する現在の推奨事項を疑問視しています。
AVRの予後
急性AVR:
急性重症大動脈閉鎖不全症のオペレーショナルリスクは、慢性重症大動脈閉鎖不全症よりも有意に高い。急性AVRの患者は、感染性心内膜炎や解離性動脈瘤などの悪化状態を示すことが多く、予後が低下します。
慢性AVR:
AVRが重症であっても、無症候性の慢性AVRは、一般的に長年にわたって一般的に陽性の予後と関連しています。AVR重症度、LVサイズおよび収縮機能の定量的測定は、臨床予後の優れた予測因子です。LV機能障害が早期に発見された場合、EFが大幅に低下する前、LV拡張の前、および症状が発生する前に、可逆的である可能性が高くなります。手術は高リスクの個人の心臓死亡率を改善するため、永久的な変化が起こる前に手術が必要です。
AVR患者が症状を呈すると、彼または彼女の状態は急速に悪化します。うっ血性心不全、急性肺水腫、突然死はすべて可能性です。NYHAクラスIIIまたはIVの症状を持つ個人のわずか30%が手術なしで4年間生存します。
AVRの合併症
慢性ARの初期段階は無症状であり、適応症や症状がない場合があります。しかし、病気が進行するにつれて、それは心臓の血行動態と機能に影響を与えます。進行性の左心室収縮機能障害、うっ血性心不全、虚血性心筋症、不整脈、および場合によっては突然の死を引き起こす可能性があります。うっ血症状または運動不耐性のある個人では、手術の利点は危険を上回ります。したがって、弁手術は問題を防ぐために十分に保証されています。
結論
大動脈弁逆流症(AVR)は、大動脈弁閉鎖が不十分であることを特徴とする心臓弁膜症であり、拡張期に大動脈から左心室(LV)に血液が逆流します。
大動脈弁閉鎖不全症は、急性(細菌性心内膜炎または大動脈解離による)または慢性(先天性二尖弁またはリウマチ熱による)であり、弁膜欠損または大動脈異常によって引き起こされる可能性があります。
急性AVRのほとんどの例は、LV機能の急速な低下をもたらし、続いて肺水腫と心臓代償不全が続きます。慢性ARは長期間補償することができ、左心不全が発生したときにのみ症状になります。
S3と甲高いデクレッシェンドの初期の拡張期雑音が聴診で聞こえます。拡大した脈圧は、もう一つの際立った診断機能です。診断の確立と病気の程度の評価の両方のための最も重要な診断ツールは心エコー検査です。
無症候性の個人に対する保存療法は、症状の制御と許容される身体活動で構成されます。.症候性またはLV機能が大幅に低下している患者は、外科的介入、最も典型的には大動脈弁置換術を必要とする。