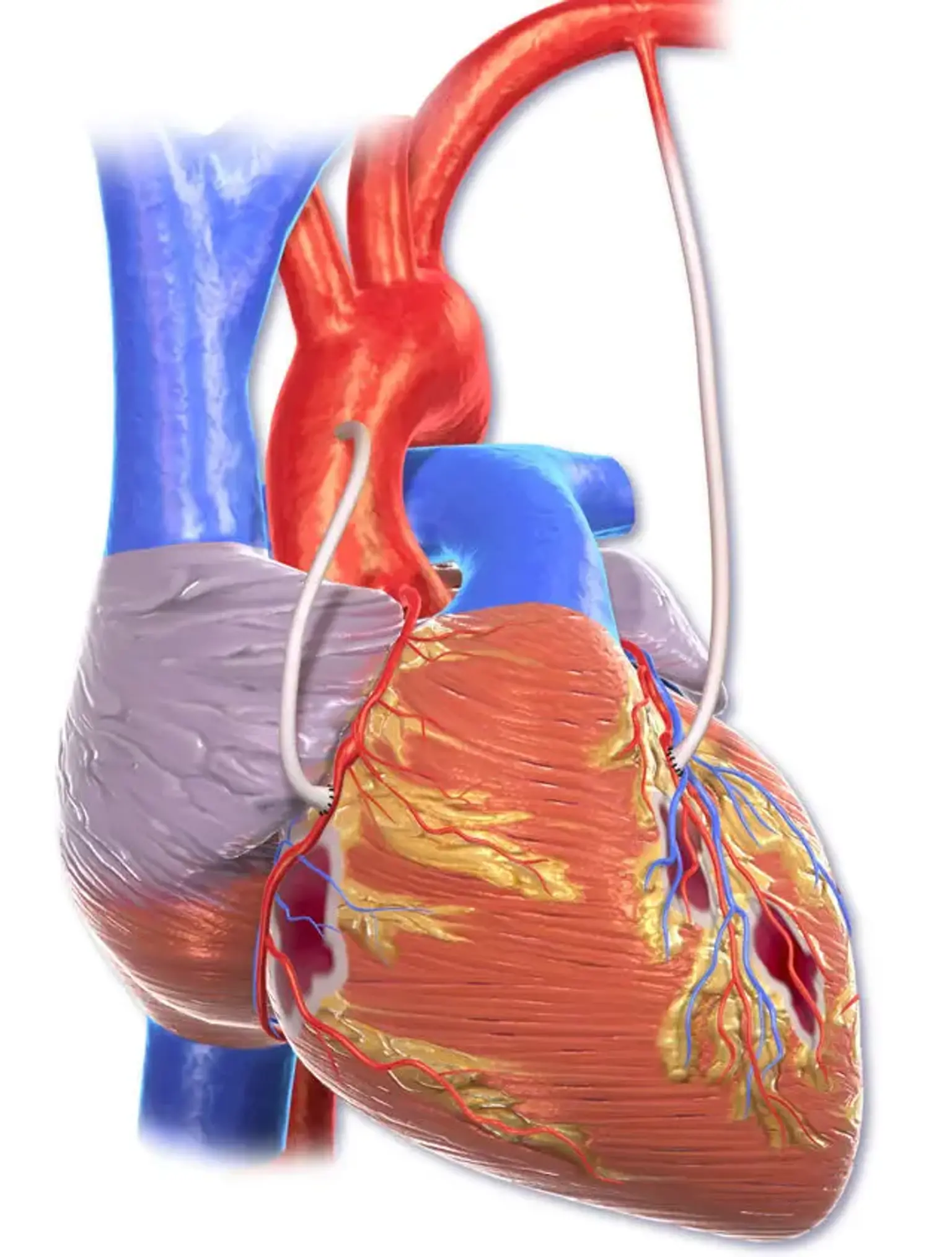
Enxerto de bypass da artéria coronária (CABG)
Visão geral
CABG é um procedimento cirúrgico significativo no qual obstruções ateromatosas nas artérias coronárias de um paciente são contornadas usando condutos venosos ou arteriais colhidos. O bypass restaura o fluxo sanguíneo para o miocárdio isquêmico, restaurando a função e a viabilidade e aliviando os sintomas anginosos.
Quase 400.000 operações de CABG são realizadas a cada ano, tornando-se a intervenção cirúrgica mais realizada regularmente; no entanto, as tendências cirúrgicas mudaram à medida que escolhas alternativas, como a terapia médica e a intervenção coronária percutânea (ICI) tornaram-se mais populares.
Cirurgia CABG
O enxerto de bypass da artéria coronária (CABG) é um procedimento utilizado para melhorar a qualidade de vida e minimizar a mortalidade cardíaca em indivíduos com doença arterial coronariana (CAD). A CAD é a maior causa de morte nos Estados Unidos e no mundo industrializado, afetando 16,5 milhões de adultos americanos (20 anos) a cada ano.
É responsável por 530.989 mortes nos Estados Unidos a cada ano, e as consequências a longo prazo da CAD, incluindo disfunção ventricular esquerda e insuficiência cardíaca, devem impactar cerca de 8 milhões de pessoas com mais de 18 anos até 2030.
A cirurgia CABG foi realizada pela primeira vez na década de 1960 com o objetivo de proporcionar alívio sintomático, melhor qualidade de vida e maior expectativa de vida aos pacientes com CAD. Quando comparado ao tratamento médico, o CABG aumentou as taxas de sobrevivência em indivíduos com doença multiarterial e deixou a doença principal na década de 1970.
O novo paradigma de tratamento da CAD pede uma abordagem da equipe cardíaca na qual o cardiologista e o cirurgião cardíaco avaliam a angiografia coronariana em conjunto e oferecem ao paciente a melhor alternativa disponível para a revascularização coronariana, seja implantação de um stent coronário percutâneo ou CABG. No momento, o paciente CABG médio é mais velho, teve intervenção coronária percutânea anterior (ICI), e tem muito mais comorbidades.
Apesar desses riscos, o CABG continua sendo uma das operações cirúrgicas mais importantes da história da medicina moderna, tendo provavelmente salvado mais vidas e oferecido um alívio sintomático mais considerável do que qualquer outra cirurgia importante. Novas abordagens minimamente invasivas, avanços na gestão de anestesia e unidade de terapia intensiva (UTI) e avanços tecnológicos estão empurrando os limites dessa operação para novos patamares.
Em geral, existem dois tipos de procedimentos cirúrgicos CABG: on-pump e off-pump, com a diferença sendo que um CABG on-pump usa um circuito de bypass cardiopulmonar e um coração preso para trabalhar. A artéria mamária interna esquerda (LIMA) e enxertos venosos safenos (SVG) das extremidades inferiores são comumente empregadas como condutores de enxerto de bypass.
A artéria mamária interna direita (RIMA), a artéria radial e a artéria gastroepiplóica são alguns dos outros condutores que podem ser transplantados. O tipo e a posição dos enxertos são determinados pela anatomia do paciente e pela localização das artérias bloqueadas. A LIMA é tipicamente enxertada na artéria descendente anterior esquerda (LAD), enquanto os outros condutores são utilizados para acessar as outras artérias bloqueadas.
Anatomia e Fisiologia
Duas artérias coronárias principais irrigam o miocárdio do coração: a artéria coronária principal esquerda e a artéria coronária direita (RCA). A artéria coronária principal esquerda é tipicamente uma seção curta que se divide nas artérias descendentes anteriores (LAD) e circunflexas esquerdas. A LAD se divide em ramos diagonais, enquanto a artéria circunflexa se divide em ramos marginais obtusos. A RCA se divide em dois ramos: a artéria descendente posterior (PDA) e os ramos marginais.
Dependendo de qual artéria fornece o septo interventricular e a PDA, a circulação coronária pode ser categorizada em sistemas dominantes à esquerda, dominantes à direita e codominantes. A artéria circunflexa supre a PDA em um sistema dominante à esquerda, enquanto a RCA supre a PDA em um sistema dominante à direita. Com a oferta vascular codominante, a PDA é alimentada tanto pela RCA quanto pelas artérias circunflexas ao mesmo tempo.
Bloqueios em qualquer uma das artérias coronárias resultam em uma deficiência correspondente na perfusão do miocárdio, isquemia, e se não tratada pode resultar em um infarto permanente ou danos ao coração.
Informações históricas
Em 1912, Alexis Carrel recebeu o Prêmio Nobel de Fisiologia e Medicina por seu trabalho. Seu conhecimento da relação entre angina pectoris e estenose da artéria coronária permitiu-lhe fazer a anastomose de um segmento da artéria carótida da aorta torácica descendente até a artéria coronária esquerda em um modelo canino.
Arthur Vineberg, um notável cirurgião canadense, transplantou a artéria torácica interna esquerda (mamária) diretamente no miocárdio do ventrículo esquerdo anterior em pacientes com angina peitoral grave no final da década de 1940. Surpreendentemente, alguns indivíduos apresentaram considerável redução de sintomas como resultado desta cirurgia.
Sabiston conduziu o primeiro procedimento planejado de bypass de veias safenas para revascularização coronária na Universidade Duke em 1962. Kolessov utilizou a artéria torácica interna esquerda (mamária) para contornar a artéria descendente anterior esquerda sem bypass cardiopulmonar em 1964, e Carpentier foi pioneiro no uso de enxertos de artéria radial como condutores CABG em 1973.
O CABG floresceu como o único tratamento para CAD durante a década de 1970 e início dos anos 1980. O número de cirurgias CABG realizadas diminuiu com o desenvolvimento, introdução e adoção generalizada de stents coronários percutâneos nas décadas de 1980 e 1990. Vários ensaios multicêntricos comparando CABG com o tratamento atual do stent, no entanto, estabeleceram claramente as vantagens do CABG, particularmente quando características específicas do paciente, como diabetes, CAD multiarterial e cardiomiopatia isquêmica são incluídas.
Indicações para CABG
Quando há bloqueios de alto grau em qualquer uma das principais artérias coronárias e/ou a intervenção coronária percutânea (PCI) não conseguiu eliminar os bloqueios, o CABG é frequentemente aconselhado. Seguem-se as recomendações classe 1 das diretrizes ACCF/AHA de 2011:
- Doença principal esquerda maior que 50%
- Doença arterial coronariana de três vasos superior a 70% com ou sem envolvimento proximal de LAD
- Doença de dois vasos: LAD mais uma outra artéria principal
- Uma estenose grave de mais de 70% em um paciente com sintomas anginal consideráveis, apesar do tratamento máximo de medicamentos
- Em um sobrevivente de morte cardíaca súbita com taquicardia ventricular relacionada à isquemia, uma doença vascular foi superior a 70%.
Outras indicações para CABG incluem as seguintes:
- Angina incapacitante (Classe I)
- Isquemia que persiste no contexto de um infarto do miocárdio de elevação do segmento não-ST (NSTEMI) que é refratário ao tratamento medicamentoso (Classe I)
- Má função ventricular esquerda, mas viável, de miocárdio não funcional acima do defeito anatômico que pode ser revascularizado.
- CAD clinicamente grave com 70% ou mais de estenose em um ou mais vasos, bem como angina refratária apesar do tratamento medicamentoso e PCI
- CAD clinicamente grave de 70% ou mais de estenose em 1 ou mais vasos em sobreviventes de parada cardíaca súbita que se acredita ser causada por arritmia ventricular isquêmica
- CAD clinicamente grave com 50% ou mais estenose em 1 ou mais vasos em pacientes submetidos à cirurgia cardíaca por outros motivos (por exemplo, substituição da válvula ou cirurgia aórtica)
O CABG pode ser realizado como um tratamento de emergência na configuração de um MI de elevação do segmento ST (STEMI) se a intervenção coronária percutânea (PCI) não for possível ou se a PCI falhou e há dor prolongada e isquemia afetando uma grande parte do miocárdio, apesar da terapia medicamentosa.
Os fatores que aumentam o benefício de sobrevivência do CABG incluem os seguintes:
- Fração de ejeção ventricular esquerda de 45% ou menos
- Diabetes mellitus
- Regurgitação mitral isquêmica
- Falha da PCI, com ou sem MI aguda (AMI)
Contra-indicações
O CABG não é recomendado para indivíduos assintomáticos que estejam em baixo risco de MI ou morte. Pacientes que se beneficiarão pouco da revascularização coronária também são excluídos.
Embora a idade do idoso não seja uma contraindicação, o CABG deve ser abordado com cautela nos idosos, particularmente aqueles com mais de 85 anos. Esses indivíduos também são mais propensos a ter problemas perioperatórios após o CABG. Em pacientes com CAD complicado, uma abordagem multidisciplinar da equipe cardíaca enfatizando a tomada de decisão compartilhada é fundamental para proporcionar ao paciente a melhor chance de um plano de revascularização bem-sucedido.
Procedimento CABG
Além da angiografia coronariana que detectou a doença arterial coronariana, o paciente exigirá vários exames realizados em preparação para a cirurgia. Testes laboratoriais como contagem sanguínea completa (CBC), painéis metabólicos, incluindo testes de função hepática, painéis de coagulação e hemoglobina A1c serão necessários. Outros testes, tais como eletrocardiograma (ECG), ecocardiografia, ultrassonografia carotídea, raio-x do tórax, e talvez uma tomografia do tórax ou um mapeamento venoso dos membros inferiores, podem ser necessários.
Para evitar arritmias como a fibrilação atrial, medicamentos pré-operatórios, como beta-bloqueadores, são frequentemente dados durante o período perioperatório. Anteriormente, a aspirina era retirada de 5 a 7 dias antes da cirurgia, mas agora é sugerido que comece ou continue no pré-operatório.
Quando o paciente chegar ao hospital, será estabelecido acesso intravenoso, e seus medicamentos e exames pré-operatórios serão examinados. O cabelo será removido dos locais da cirurgia, e o paciente receberá um banho de clorexidina.
Equipamento
Esta cirurgia cirúrgica significativa requer não apenas o equipamento necessário para a maioria das outras operações cirúrgicas, mas também vários equipamentos especializados, como uma máquina de bypass cardiopulmonar com um dispositivo de refrigeração aquecedor para aquecer e resfriar o sangue.
Pessoal
A operação é realizada por uma equipe especializada em cirurgia cardiovascular com extenso treinamento e experiência para cuidar desses pacientes complexos. A equipe é composta pelo cirurgião cardiotorácico e seus assistentes, anestesiologistas, enfermeiros, técnicos cirúrgicos e perfusionistas
Avaliação de Risco
Modelos de risco para prever mortalidade em 30 dias após CRM isolada estão sendo desenvolvidos. Os preditores mais usados em cirurgia cardíaca são o sistema Euroscore e o Society of Thoracic Surgeons (STS) 2008 Cardiac Surgery Risk Model. Idade, MI anterior, PVD, insuficiência renal, status hemodinâmico e EF são fatores compartilhados nesses dois modelos pendentes. Oito dos fatores mais relevantes, incluindo idade, acuidade cirúrgica, estado de reoperação, nível de creatinina, diálise, choque, doença pulmonar crônica e EF, explicam 78% da variação no modelo STS.
Pré medicação
A pré medicação busca reduzir as necessidades de oxigênio do miocárdio, reduzindo a frequência cardíaca e a pressão arterial sistêmica, bem como aumentar o fluxo sanguíneo do miocárdio usando vasodilatadores. Os seguintes medicamentos devem ser tomados até o momento da cirurgia:
- Beta-bloqueadores, bloqueadores de canais de cálcio e nitratos
- Aspirina
Os agentes administrados são os seguintes:
- Temazepam imediatamente pré-operatório
- Midazolam, uma pequena dose intravenosa (IV) na sala de cirurgia antes da inserção da linha arterial
Cada paciente deve receber 2 unidades de sangue (para casos leves) ou 6 unidades de sangue, plasma congelado fresco e plaquetas compatíveis (para casos complexos). O ácido tranexâmico (1 g de bolus antes da incisão cirúrgica, seguido de uma infusão de 400 mg/h durante a cirurgia) pode ser considerado para minimizar a hemorragia mediastinal pós-operatória e a quantidade de produtos sanguíneos necessários (ou seja, glóbulos vermelhos e plasma congelado fresco)
Anestesia
A cirurgia cardíaca é geralmente conduzida sob anestesia geral profunda com tubo endotraqueal. Os dois tipos seguintes de bloqueio neuraxial são usados raramente como adjuntos:
- Infusão de opioides intratecal
- Anestesia peridural torácica (geralmente uma infusão local de alta dose/ infusão de opioides)
Técnica
O processo começa depois que o paciente está na sala de cirurgia e é conectado a monitores padrão. Antes de induzir anestesia geral, um anestesista pode inserir uma linha arterial para monitorar a pressão arterial do paciente invasivamente. Após a indução da anestesia geral e da intubação do paciente, pode ser inserida uma linha central de acesso venoso e um cateter da artéria pulmonar, seguida pela inserção de um transdutor transesofágico de ecocardiografia.
Antes da incisão cirúrgica, o paciente é preparado e coberto de forma estéril, e o anestésico é administrado.. O cirurgião realiza uma esternotomia mediana para se preparar para a remoção do LIMA para uso como condutor. Um assistente treinado, geralmente um assistente médico, enfermeiro primeiro assistente ou outro cirurgião, usa procedimentos abertos ou assistidos por vídeo para remover a veia safena de uma ou ambas as pernas ao mesmo tempo.
Após a aquisição de condutores adequados, o cirurgião prescreve anticoagulação, na maioria das vezes heparina, a ser administrada em preparação para bypass cardiopulmonar (CPB). A aorta e o coração do paciente são centralmente canulados, e a tubulação está conectada ao circuito de bypass cardiopulmonar. Após o início do CPB, o coração é parado com cardioplegia de potássio elevado para que o cirurgião possa anastomosar os condutores colhidos às artérias coronárias distantes das obstruções.
Como condutores para enxerto de bypass da artéria coronária, podem ser empregadas artérias ou veias. Uma publicação-chave da Cleveland Clinic de muitos anos atrás provou as vantagens de sobrevivência ao enxertar a artéria torácica interna esquerda (mamária) na artéria coronária descendente anterior esquerda. Isso ainda é verdade; de fato, se possível, o enxerto de artéria torácica interna bilateral (mamária) oferece um considerável benefício de sobrevivência a longo prazo. Fortes evidências mostram que o uso de um enxerto de artéria extra em vez de um enxerto venoso está relacionado com melhores resultados a longo prazo.
A veia safena maior e, em raras ocasiões, a veia safena curta são os enxertos venosos mais utilizados com regularidade, enquanto a artéria torácica interna (mamária) é o transplante de artéria mais utilizado. O enxerto da artéria radial foi reintroduzido na prática clínica na década de 1990 e continua a demonstrar altas taxas de patência de 80% ou mais após 10 anos de seguimento, particularmente se a estenose vascular alvo fosse maior que 90%.
A desvantagem dos enxertos venosos safenos é que sua patência diminui com o tempo: 10-20% são bloqueados 1 ano após a cirurgia devido a erros técnicos, trombose e hiperplasia intimal. Outros 1-2% dos enxertos venosos ocluem todos os anos de 1 a 5 anos após a cirurgia, e outros 4-5% ocluem a cada ano de 6 a 10 anos. Oclusão do enxerto venoso que ocorre um ou mais anos após o CABG é causada pela aterosclerose do enxerto venoso, que é acompanhada pelo desenvolvimento da hiperplasia neointimal.
Apenas 50-60% dos enxertos de veias safenas estão patentes 10 anos após a cirurgia, e apenas metade deles estão livres de aterosclerose angiográfica. Os pacientes devem tomar medicamentos antiplaquetários ao longo da vida, mais tipicamente sob a forma de aspirina de baixa dose diária (81 mg), como parte da profilaxia secundária adequada.
Enxertos de artéria torácica interna (mamária), ao contrário dos enxertos venosos, mantêm a patência ao longo do tempo. Mais de 90% dos enxertos de artéria torácica interna (mamária) ainda são patenteados após 10 anos. Quando a artéria coronária anterior esquerda é contornada, a artéria torácica interna esquerda (mamária) deve ser utilizada como o condutor.
Os condutores estão ligados ao óstio gerado na aorta proximal após o cirurgião anastomosar as partes distais. A cardioplegia é então lavada, o coração começa a se contrair, e o cirurgião pode examinar os enxertos para fluxo sanguíneo e competência, bem como sangramento dos locais de anastomose. O tórax é então fechado com fios esternais, e o paciente é transferido para a unidade de cuidados críticos para monitoramento e estabilidade hemodinâmica e extubação.
Complicações
Acidente vascular cerebral, infecção por feridas, falha no enxerto, insuficiência renal, fibrilação atrial pós-operatória e mortalidade são todas as possíveis consequências do CABG. A taxa de derrame após o CABG foi relatada entre 1% e 2%, dependendo das características do paciente e dos fatores de risco para acidente vascular cerebral, que incluem idade avançada, derrame anterior, aterosclerose aórtica, doença arterial periférica, fibrilação atrial perioperatória e diabetes.
As taxas de infecção por feridas severas giram em torno de 1% e são afetadas por variáveis de risco como obesidade, diabetes, doença pulmonar obstrutiva crônica (DPOC) e tempo de operação.
A falha de um enxerto venoso safeno (SVG) é provavelmente dentro de 30 dias após a cirurgia e é causada por inúmeras razões como tamanho da veia e comprimento excessivo, escoamento distal e fluxo ruim, hipercoagulabilidade e trombose. Com a angiografia repetida após o CABG, foram observadas taxas de falha de SVG de até 25%. Alternativamente, enxertos arteriais como a artéria mamária interna esquerda (LIMA) e enxertos arteriais radiais duram mais tempo e têm taxas de patência que chegam a 90% após 10 anos.
As taxas de insuficiência renal pós-operatória após o CABG variam de 2% a 3%, com 1% precisando de diálise. Doença renal pré-operatória, velhice, diabetes, tipo de cirurgia, disfunção LV e choque são todos fatores de risco. Embora nenhum fármaco tenha definitivamente provado diminuir as taxas de comprometimento renal induzido pelo CABG, o CABG off-pump pode oferecer um benefício sobre o CABG on-pump.
A fibrilação atrial nos primeiros 5 dias após o CABG é bastante frequente, com taxas que variam de 20% a 50%, e está ligada ao aumento da morbidade, incluindo maior risco de acidente vascular cerebral e morte. A estratégia mais eficaz para minimizar a incidência de fibrilação atrial pós-operatória tem sido comprovadamente terapia pré-operatória com beta-bloqueadores e talvez amiodarona.
O risco de mortalidade perioperatória após o CABG varia de acordo com as co-morbidades, a urgência da cirurgia e o volume de caso da unidade onde o procedimento é realizado, variando de 1% a 2%.
Resultados
De acordo com uma meta-análise de seis ensaios clínicos randomizados envolvendo 6.055 pacientes da era do enxerto e stent arterial, o enxerto de bypass da artéria coronária (CABG) leva a uma redução da mortalidade de longo prazo e infartos do miocárdio (IM), bem como reduções nas revascularizações repetidas em pacientes com doença coronariana multiarterial, independentemente de os pacientes serem diabéticos ou não.
Uma meta-análise de oito ensaios randomizados envolvendo 3.612 pacientes adultos com diabetes e doença coronariana multiarterial (CAD) constatou que o CABG reduziu o risco de morte por todas as causas em 33% após 5 anos quando comparado ao PCI. Quando os pacientes que tinham CABG foram comparados com subgrupos de pacientes que tinham stents metálicos nus ou stents de eluição de drogas, a diminuição relativa do risco não variou substancialmente.
Os pacientes de 51 a 70 anos e aqueles com mais de 70 anos que receberam CABG no mesmo período de tempo se saíram consideravelmente piores em termos de sobrevivência. Doença renal crônica, baixa fração de ejeção ventricular esquerda, doença vascular periférica ou doença pulmonar obstrutiva crônica foram os principais fatores de risco para a morte por todas as causas.
O Estudo de Extensão do Tratamento Cirúrgico para Insuficiência Cardíaca Isquêmica (STICH) (STICHES) concluiu que as taxas de morte por qualquer causa, morte por causas cardiovasculares e morte por qualquer causa ou internação por causas cardiovasculares foram significativamente menores em pacientes submetidos ao CABG e receberam medicare.
Além disso, houve uma considerável variação hospitalar nas taxas de CABG STEMI, e o CABG foi frequentemente feito dentro de 1-3 dias de angiografia. Pacientes que receberam CABG e aqueles que não apresentaram taxas de mortalidade no hospital semelhantes.
Uma meta-análise de 6637 pacientes com CAD principal desprotegido de nove ensaios durante um período de 14 anos (2003-2016) constatou que o ICI com stents de eluição de drogas estava associado à mortalidade cardíaca e de todas as causas comparáveis, mas reduziu as taxas de derrame e maiores taxas de revascularização repetida. Para eventos cardíacos e cerebrovasculares adversos significativos, uma tendência favorável ao CABG vs PCI não alcançou significância estatística.
Em termos de qualidade de vida após CABG versus PCI para CAD multiarterial, ambos os procedimentos melhoram a frequência da angina. No entanto, com 1 mês de pós-procedimento, os pacientes com PCI tendem a se recuperar mais rapidamente e ter melhor estado de saúde de curto prazo do que os pacientes com CABG, porém com 6 meses e mais pós-procedimento, os pacientes cabg parecem ter melhor alívio de angina e qualidade de vida do que os pacientes com PCI.
Conclusão
Um enxerto de bypass da artéria coronária (CABG) é uma técnica cirúrgica usada para tratar doenças cardíacas coronárias com o objetivo de melhorar a qualidade de vida e reduzir a mortalidade cardíaca. Redireciona o sangue ao redor de seções restritas ou obstruídas das principais artérias, aumentando o fluxo sanguíneo e a entrega de oxigênio ao coração.