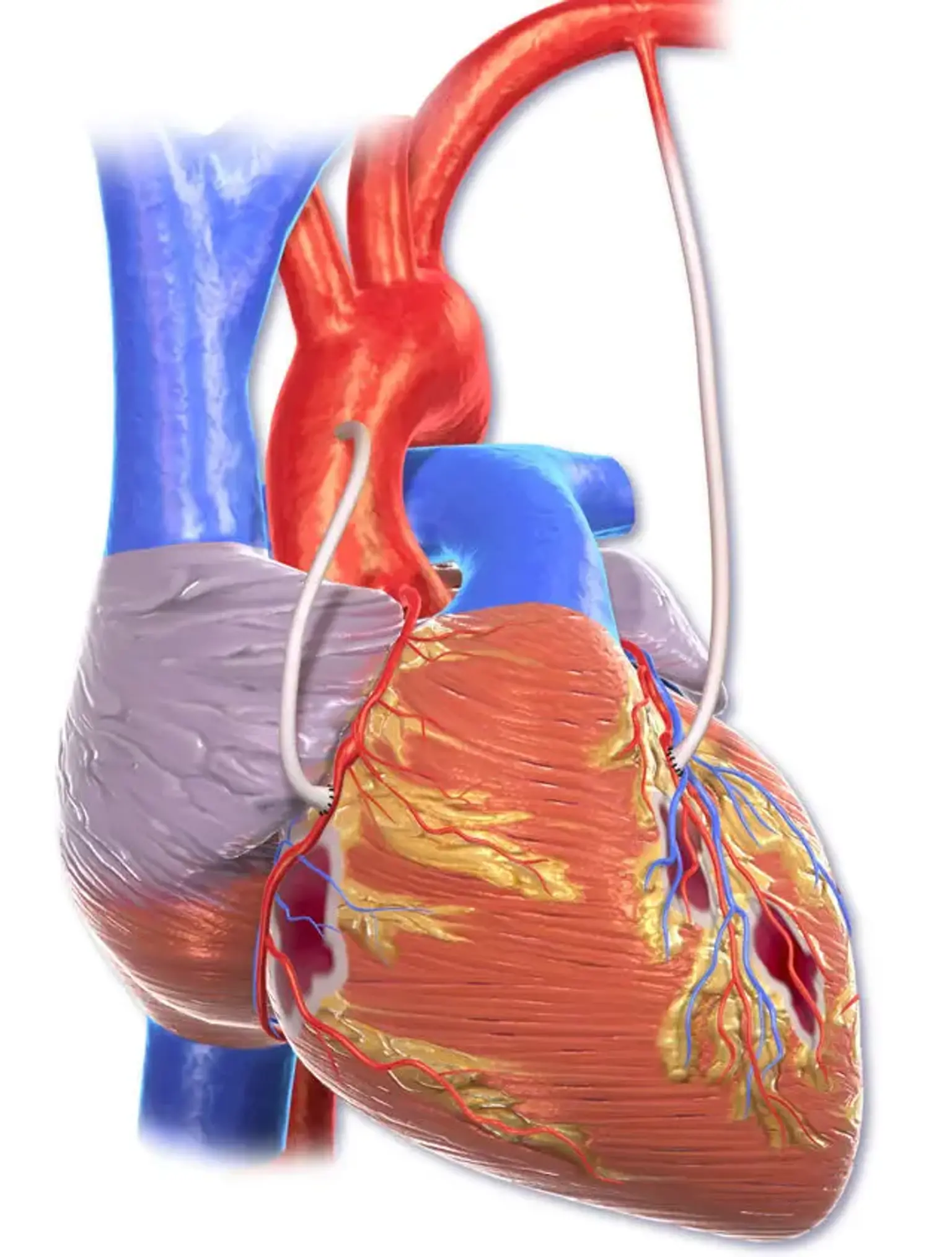
Аортокоронарное шунтирование (АКШ)
Обзор
АКШ - это важная хирургическая процедура, при которой атероматозные обструкции в коронарных артериях пациента обходятся с помощью венозных или артериальных кондуитов. Шунтирование восстанавливает кровоток в ишемизированном миокарде, восстанавливая его функцию и жизнеспособность и облегчая симптомы стенокардии.
Ежегодно проводится почти 400 000 операций АКШ, что делает ее наиболее регулярно выполняемой крупной хирургической операцией; однако тенденции в хирургии изменились, поскольку альтернативные варианты, такие как медикаментозная терапия и чрескожное коронарное вмешательство (ЧКВ), стали более популярными.
Хирургия АКШ
Аортокоронарное шунтирование (АКШ) - это процедура, используемая для повышения качества жизни и минимизации смертности, связанной с сердцем, у пациентов с ишемической болезнью сердца (ИБС). ИБС является самой большой причиной смерти в США и промышленно развитом мире, ежегодно поражая 16,5 миллионов взрослых жителей США (в возрасте 20 лет).
Ежегодно в США от нее умирают 530 989 человек, а долгосрочные последствия ИБС, в том числе как дисфункция левого желудочка и сердечная недостаточность, как ожидается, затронут почти 8 миллионов человек в возрасте старше 18 лет к 2030 году.
Операция АКШ была впервые выполнена в 1960-х годах с целью облегчения симптомов, улучшения качества жизни и увеличения продолжительности жизни пациентов с ИБС. По сравнению с медицинским лечением, АКШ увеличила выживаемость у пациентов с многососудистым заболеванием и оставила основное заболевание к 1970-м годам.
Новая парадигма лечения ИБС требует командного подхода, при котором кардиолог и кардиохирург вместе оценивают результаты коронарной ангиографии и предлагают пациенту наилучшую доступную альтернативу коронарной реваскуляризации, будь то имплантация чрескожного коронарного стента или АКШ. В настоящее время среднестатистический пациент, которому проводится АКШ, старше, у него ранее было чрескожное коронарное вмешательство (ЧКВ), и у него гораздо больше сопутствующих заболеваний.
Несмотря на эти риски, АКШ остается одной из самых важных хирургических операций в истории современной медицины, вероятно, она спасла больше жизней и обеспечила более значительное облегчение симптомов, чем любая другая крупная операция. Новые минимально инвазивные подходы, прорывы в анестезии и ведении пациентов в отделениях интенсивной терапии (ОИТ), а также технологические усовершенствования расширяют возможности этой операции.
В целом, существует два типа хирургических процедур АКШ: с использованием насоса и без него, с той разницей, что при АКШ с использованием насоса для работы используется контур сердечно-легочного шунтирования и остановленное сердце. В качестве трансплантатов для шунтирования обычно используются левая внутренняя грудная артерия (ЛВГА) и трансплантаты подкожных вен (ТПВ) из нижних конечностей.
Правая внутренняя грудная артерия (ПВГА), лучевая артерия и желудочно-сальниковая артерия - вот некоторые из других трансплантатов, которые могут быть пересажены. Вид и расположение трансплантатов определяются анатомией пациента и расположением заблокированных артерий. ЛВГА обычно пересаживается в левую переднюю нисходящую артерию (ЛПНА), а другие кондуиты используются для доступа к другим заблокированным артериям.
Анатомия и физиология
Миокард сердца снабжают две основные коронарные артерии: левая главная коронарная артерия и правая коронарная артерия (ПКА). Левая основная коронарная артерия обычно представляет собой короткий участок, который делится на левую переднюю нисходящую (ЛПН) и околосердечную артерии. ЛПН делится на диагональные ветви, в то время как окружная артерия делится на тупые краевые ветви. ПКА делится на две ветви: заднюю нисходящую артерию (ЗНА) и краевые ветви.
В зависимости от того, какая артерия снабжает межжелудочковую перегородку и ЗНА, коронарное кровообращение можно разделить на леводоминантную, праводоминантную и содоминантную системы. Околосердечная артерия снабжает ЗНА в леводоминантной системе, тогда как ПКА снабжает ЗНА в праводоминантной системе. При доминирующем сосудистом снабжении КПК снабжается одновременно и ПКА, и циркумфлекторной артерией.
Закупорка любой из коронарных артерий приводит к соответствующему дефициту перфузии миокарда, ишемии, и если ее не лечить, может привести к необратимому инфаркту или повреждению сердца.
Историческая справка
В 1912 году Алексис Каррель был удостоен Нобелевской премии по физиологии и медицине за свою работу. Его знания о взаимосвязи между стенокардией и стенозом коронарной артерии позволили ему анастомозировать сегмент сонной артерии из нисходящей грудной аорты с левой коронарной артерией на собачьей модели.
Артур Вайнберг, выдающийся канадский хирург, пересадил левую внутреннюю грудную (маммарную) артерию непосредственно в миокард передней стенки левого желудочка у пациентов с тяжелой стенокардией. Удивительно, но у нескольких человек в результате этой операции наблюдалось значительное уменьшение симптомов.
Сабистон провел первую запланированную процедуру шунтирования подкожной вены для коронарной реваскуляризации в Университете Дьюка в 1962 году. Колессов использовал левую внутреннюю грудную (маммарную) артерию для шунтирования левой передней нисходящей артерии без сердечно-легочного шунтирования в 1964 году, а Карпентье стал пионером в использовании трансплантатов лучевой артерии в качестве проводников для АКШ в 1973 году.
АКШ процветала как единственный метод лечения ИБС в течение 1970-х и начала 1980-х годов. Количество операций АКШ уменьшилось с развитием, внедрением и широким распространением чрескожного стентирования коронарной артерии в 1980-х и 1990-х годах. Однако несколько многоцентровых исследований, сравнивающих АКШ с современным стентированием, четко установили преимущества АКШ, особенно при учете специфических особенностей пациентов, таких как диабет, многососудистый ИБС и ишемическая кардиомиопатия.
Показания к применению АКШ
Если в одной из главных коронарных артерий имеется закупорка высокой степени и/или чрескожное коронарное вмешательство (ЧКВ) не помогло устранить закупорку, часто рекомендуется проведение АКШ. Ниже приведены рекомендации класса 1 из руководящих принципов ACCF/AHA 2011 года:
- Заболевание левой магистральной артерии более 50%
- Трехсосудистая ишемическая болезнь сердца более 70% с или без проксимального поражения ЛПН
- Двухсосудистое заболевание: ЛПН плюс еще одна крупная артерия
- Тяжелый стеноз более 70% у пациента со значительными ангинальными симптомами, несмотря на максимальное медикаментозное лечение
- У пациента, пережившего внезапную сердечную смерть с желудочковой тахикардией, связанной с ишемией, одно сосудистое заболевание составляло более 70%.
К другим показаниям для АКШ включают следующее:
- Инвалидизирующая стенокардия (класс I)
- Ишемия, сохраняющаяся на фоне инфаркта миокарда без подъема сегмента ST (NSTEMI), рефрактерная к медикаментозному лечению (класс I)
- Плохая функция левого желудочка, но жизнеспособный, нефункционирующий миокард над анатомическим дефектом, который может быть реваскуляризирован.
- Клинически тяжелая ИБС с 70-процентным или более стенозом в одном или нескольких сосудах, а также рефрактерная стенокардия, несмотря на медикаментозное лечение и ЧКВ
- Клинически тяжелая ИБС 70% или более стеноза в одном или нескольких сосудах у пациентов, переживших внезапную остановку сердца, причиной которой, как предполагается, была ишемическая желудочковая аритмия
- Клинически тяжелая ИБС с 50% и более стенозом в одном или нескольких сосудах у пациентов, перенесших кардиохирургию по другим причинам (например, замена клапана или операция на аорте)
АКШ может быть выполнена в качестве экстренного лечения в условиях им-подъема сегмента ST (STEMI), если чрескожное коронарное вмешательство (ЧКВ) было невозможно или если ЧКВ не помогло, а также при наличии продолжительной боли и ишемии, затрагивающей большую часть миокарда, несмотря на медикаментозную терапию.
К факторам, повышающим выживаемость после АКШ, включают следующее:
- Фракция выброса левого желудочка 45% или менее
- Сахарный диабет
- Ишемическая митральная регургитация
- Недостаточность ЧКВ, с острым ИМ (ОИМ) или без него
Противопоказания
АКШ не рекомендуется бессимптомным пациентам с низким риском МИ или смерти. Пациенты, которым коронарная реваскуляризация принесет незначительную пользу, также исключаются.
Хотя пожилой возраст не является противопоказанием, к АКШ следует подходить с осторожностью у пожилых людей, особенно старше 85 лет. Эти люди также более склонны к возникновению периоперационных проблем после АКШ. У пациентов с осложненной формой ИБС подход мультидисциплинарной кардиологической команды с акцентом на совместное принятие решений имеет решающее значение для обеспечения пациенту наилучших шансов на успешный план реваскуляризации.
Процедура АКШ
Помимо коронарной ангиографии, выявившей заболевание коронарных артерий, пациенту потребуются различные анализы, проводимые в рамках подготовки к операции. Потребуются такие лабораторные исследования, как полный анализ крови (CBC), метаболические панели, включая функциональные тесты печени, панели коагуляции и гемоглобин A1c. Могут потребоваться и другие исследования, в том числе электрокардиограмма (ЭКГ), эхокардиография, ультразвуковое исследование сонных артерий, рентгенография грудной клетки, возможно, компьютерная томография грудной клетки или картирование вен нижних конечностей.
Чтобы избежать аритмий, таких как фибрилляция предсердий, в периоперационный период часто назначаются предоперационные препараты, такие как бета-блокаторы. Раньше от аспирина воздерживались за 5-7 дней до операции, но сейчас предлагается начать или продолжить его прием до операции.
Когда пациент прибывает в больницу, ему устанавливают внутривенный доступ, проверяют его лекарства и предоперационные анализы. Волосы из мест проведения операции будут удалены, а пациенту сделают ванночку с хлоргексидином.
Оборудование
Для проведения этой важной хирургической операции требуется не только оборудование, необходимое для большинства других хирургических операций, но и несколько специальных приборов, таких как аппарат для сердечно-легочного шунтирования с нагревателем-охладителем для подогрева и охлаждения крови.
Персонал
Операция проводится специализированной сердечно-сосудистой хирургической бригадой с большой подготовкой и опытом ухода за этими сложными пациентами. В бригаду входят кардиоторакальный хирург и его ассистенты, анестезиологи, медсестры, хирургические техники и перфузиологи.
Оценка риска
В настоящее время разрабатываются модели риска для прогнозирования 30-дневной смертности после изолированной АКШ. Наиболее часто используемыми предикторами в кардиохирургии являются система Euroscore и модель риска кардиохирургии Общества торакальных хирургов (ОТХ) 2008 года. Возраст, предшествующий ИМ, ПВД, почечная недостаточность, гемодинамический статус и КВ являются общими факторами в этих двух выдающихся моделях. Восемь наиболее значимых факторов, включая возраст, остроту хирургического вмешательства, статус повторной операции, уровень креатинина, диализ, шок, хронические заболевания легких и КВ, объясняют 78% вариаций в модели ОТХ.
Премедикация
Премедикация направлена на снижение потребности миокарда в кислороде путем снижения частоты сердечных сокращений и системного артериального давления, а также на увеличение миокардиального кровотока с помощью вазодилататоров. Следующие препараты следует принимать до момента операции:
- Бета-блокаторы, блокаторы кальциевых каналов и нитраты
- Аспирин
Препараты назначаются следующим образом:
- Темазепам непосредственно перед операцией
- Мидазолам, небольшая внутривенная (IV) доза в операционной перед введением артериальной линии
Каждый пациент должен получить 2 единицы крови (для легких случаев) или 6 единиц крови, свежезамороженной плазмы и перекрестно подобранных тромбоцитов (для сложных случаев). Транексамовая кислота (1 г болюса перед хирургическим разрезом, затем инфузия 400 мг/ч во время операции) может быть рассмотрена для минимизации послеоперационного средостенного кровотечения и количества необходимых препаратов крови (т.е. эритроцитов и свежезамороженной плазмы).
Анестезия
Кардиохирургия чаще всего проводится под глубоким общим наркозом с эндотрахеальной трубкой. Следующие два типа нейронаксиальной блокады редко используются в качестве вспомогательных средств:
- Интратекальная инфузия опиоидов
- Торакальная эпидуральная анестезия (как правило, низкая доза местного анестетика / опиоидной инфузии)
Техника
Процесс начинается после того, как пациент находится в операционной и подключается к стандартным мониторам. Перед введением общего наркоза, анестезиолог может установить артериальную линию для инвазивного мониторинга артериального давления пациента. После введения общей анестезии и интубации пациента может быть установлена центральная линия для венозного доступа и катетер легочной артерии, а затем введен датчик для чреспищеводной эхокардиографии.
Перед хирургическим разрезом пациента стерильно подготавливают и драпируют, назначают тайм-аут. Хирург выполняет срединную стернотомию, чтобы подготовиться к удалению ЛВГА для использования в качестве кондуита. Обученный ассистент, как правило, помощник врача, первый помощник медсестры или другой хирург, использует открытые или видеоассистированные процедуры для удаления подкожной вены на одной или обеих ногах одновременно.
После получения адекватных кондуитов хирург назначает антикоагуляцию, чаще всего гепарин, для подготовки к сердечно-легочному шунтированию (СЛШ). Аорта и сердце пациента канюлируются по центру, и трубки подключаются к контуру сердечно-легочного шунтирования. После начала СЛШ сердце останавливают с помощью высококалиевой кардиоплегии, чтобы хирург мог анастомозировать собранные кондуиты с коронарными артериями, удаленными от обструкции.
В качестве кондуитов для шунтирования коронарных артерий могут использоваться артерии или вены (АКШ). Ключевая публикация Кливлендской клиники много лет назад доказала преимущества для выживания при трансплантации левой внутренней грудной (маммарной) артерии в левую переднюю нисходящую коронарную артерию. Это по-прежнему актуально; более того, если это возможно, двусторонняя пересадка внутренней грудной (маммарной) артерии дает значительное преимущество в долгосрочной выживаемости. Убедительные доказательства показывают, что использование трансплантата дополнительной артерии, а не венозного трансплантата, связано с улучшением долгосрочных результатов.
Более крупная подкожная вена и, в редких случаях, короткая подкожная вена являются наиболее регулярно используемыми венозными трансплантатами, тогда как внутренняя грудная (маммарная) артерия является наиболее часто используемой трансплантацией артерии. Трансплантат лучевой артерии был вновь введен в клиническую практику в 1990-х годах и продолжает демонстрировать высокие показатели проходимости - 80% и более после 10 лет наблюдения, особенно если стеноз целевого сосуда был более 90%.
Недостатком трансплантатов подкожных вен является то, что их проходимость со временем снижается: 10-20% блокируются через 1 год после операции из-за технических ошибок, тромбоза и гиперплазии интимы. Еще 1-2% венозных трансплантатов закупориваются каждый год в течение 1-5 лет после операции, и еще 4-5% закупориваются каждый год в течение 6-10 лет. Окклюзия венозного трансплантата, возникающая через один или несколько лет после КАБГ, вызвана атеросклерозом венозного трансплантата, который сопровождается развитием неоинтимальной гиперплазии.
Только 50-60% трансплантатов подкожных вен являются проходимыми через 10 лет после операции, и только половина из них не имеет ангиографического атеросклероза. В рамках надлежащей вторичной профилактики пациенты должны пожизненно принимать антитромбоцитарные препараты, чаще всего в виде ежедневного низкодозированного (81 мг) аспирина.
Трансплантаты внутренней грудной (маммарной) артерии, в отличие от трансплантатов подкожной вены, сохраняют свою проходимость в течение длительного времени. Более 90% трансплантатов внутренней грудной (маммарной) артерии остаются проходимыми через 10 лет. При шунтировании левой передней коронарной артерии в качестве кондуита следует использовать левую внутреннюю грудную (маммарную) артерию.
Кондуиты соединяются с новыми остиями, образованными в проксимальном отделе аорты, после того как хирург анастомозирует дистальные части. Затем кардиоплегия смывается, сердце начинает сокращаться, и хирург может осмотреть трансплантаты на предмет кровотока и компетентности, а также кровотечения из мест анастомоза. Затем грудная клетка закрывается стернальными проволоками, и пациент переводится в отделение реанимации для мониторинга гемодинамической стабильности и экстубации.
Осложнения
Инсульт, раневая инфекция, недостаточность трансплантата, почечная недостаточность, послеоперационная фибрилляция предсердий и смертность — все это возможные последствия АКШ. Частота инсульта после АКШ составляет от 1% до 2%, в зависимости от особенностей пациента и факторов риска инсульта, к которым относятся пожилой возраст, предыдущий инсульт, атеросклероз аорты, заболевания периферических артерий, периоперационная фибрилляция предсердий и диабет.
Уровень инфицирования грудной раны составляет около 1% и зависит от таких факторов риска, как ожирение, диабет, хроническая обструктивная болезнь легких (ХОБЛ) и продолжительность операции.
Несостоятельность трансплантата подкожной вены (СВГ) наиболее вероятна в течение 30 дней после операции и обусловлена множеством причин, таких как размер вены и ее чрезмерная длина, дистальный сток и плохой поток, а также гиперкоагуляция и тромбоз. При повторной ангиографии после АКШ частота несостоятельности СВГ достигает 25%. Альтернативные артериальные трансплантаты, такие как левая внутренняя грудная артерия (ЛВГА) и лучевые артериальные трансплантаты, служат дольше и имеют показатели проходимости, достигающие 90% через 10 лет.
Частота послеоперационной почечной недостаточности после АКШ варьируется от 2% до 3%, причем 1% нуждается в диализе. Предоперационная заболевание почек, пожилой возраст, диабет, тип хирургии, дисфункция ЛЖ и шок являются факторами риска. Хотя не было доказано, что какие-либо препараты снижают частоту почечной недостаточности, вызванной АКШ, АКШ без насоса может иметь преимущества перед АКШ с насосом.
Фибрилляция предсердий в течение первых 5 дней после АКШ встречается довольно часто, с частотой от 20% до 50%, и связана с повышенной заболеваемостью, включая повышенный риск эмболического инсульта и смерти. Доказано, что наиболее эффективной стратегией для минимизации частоты возникновения послеоперационной фибрилляции предсердий является предоперационная терапия бета-блокаторами и, возможно, амиодароном.
Риск периоперационной смертности после АКШ варьируется в зависимости от сопутствующих заболеваний, срочности и объема операций в учреждении, где проводится операция, в пределах от 1% до 2%.
Результаты
Согласно мета-анализу шести рандомизированных клинических исследований с участием 6055 пациентов, проведенных в эпоху трансплантации и стентирования артерий, шунтирование коронарных артерий ("АКШ") приводит к снижению долгосрочной смертности и инфарктов миокарда (ИМ), а также к сокращению числа повторных реваскуляризаций у пациентов с многососудистым коронарным заболеванием, независимо от того, являются ли пациенты диабетиками или нет.
Мета-анализ восьми рандомизированных исследований с участием 3612 взрослых пациентов с диабетом и многососудистой болезнью коронарной артерии (ИБС) показал, что АКШ снижает риск смерти от всех причин на 33% через 5 лет по сравнению с ЧКВ. Когда пациентов, которым была проведена АКШ, сравнивали с подгруппами пациентов, которым были установлены либо голые металлические стенты, либо стенты с лекарственным покрытием, относительное снижение риска существенно не отличалось.
Пациенты в возрасте от 51 до 70 лет и те, кто старше 70 лет, которые перенесли АКШ в один и тот же период времени, имели значительно худшие показатели выживаемости. Хроническая болезнь почек, низкая фракция выброса левого желудочка, заболевания периферических сосудов или хроническая обструктивная болезнь легких были основными факторами риска смерти от всех причин.
Исследование по расширению хирургического лечения ишемической сердечной недостаточности (ИРХЛИСН) показало, что показатели смертности от любой причины, смертности от сердечно-сосудистых причин, а также смертности от любой причины или госпитализации по сердечно-сосудистым причинам были значительно ниже у пациентов, перенесших АКШ и получавших медицинское лечение.
Кроме того, наблюдалась значительная дисперсия на уровне больниц в показателях ИРХЛИСН АКШ, и АКШ часто проводилась в течение 1-3 дней после ангиографии. Пациенты, которые перенесли и не перенесли АКШ, имели схожие показатели смертности в больнице.
Мета-анализ 6637 пациентов с незащищенной левой основной ИБС из девяти исследованиях за 14-летний период (2003-2016 гг.) показал, что ЧКВ с стентами, элюирующими лекарства, был связан с сопоставимой сердечной и всепричинной смертностью, но снижал частоту инсульта и более высокие показатели повторной реваскуляризации. Для значительных неблагоприятных сердечных и цереброваскулярных событий тенденция в пользу АКШ по сравнению с ЧКВ не достигла статистической значимости.
С точки зрения качества жизни после АКШ по сравнению с ЧКВ при многососудистом ИБС, обе процедуры улучшают частоту стенокардии. Тем не менее, через 1 месяц после процедуры пациенты с ЧКВ, как правило, быстрее выздоравливают и имеют лучшее краткосрочное состояние здоровья, чем пациенты с АКШ, однако через 6 месяцев и дольше после процедуры пациенты с АКШ, по-видимому, имеют лучшее облегчение стенокардии и качество жизни, чем пациенты с ЧКВ.
Заключение
Аортокоронарное шунтирование (АКШ) - это хирургический метод, используемый для лечения ишемической болезни сердца с целью улучшения качества жизни и снижения смертности, связанной с сердечным заболеванием. Он перенаправляет кровь вокруг суженных или закупоренных участков основных артерий, увеличивая кровоток и доставку кислорода к сердцу.