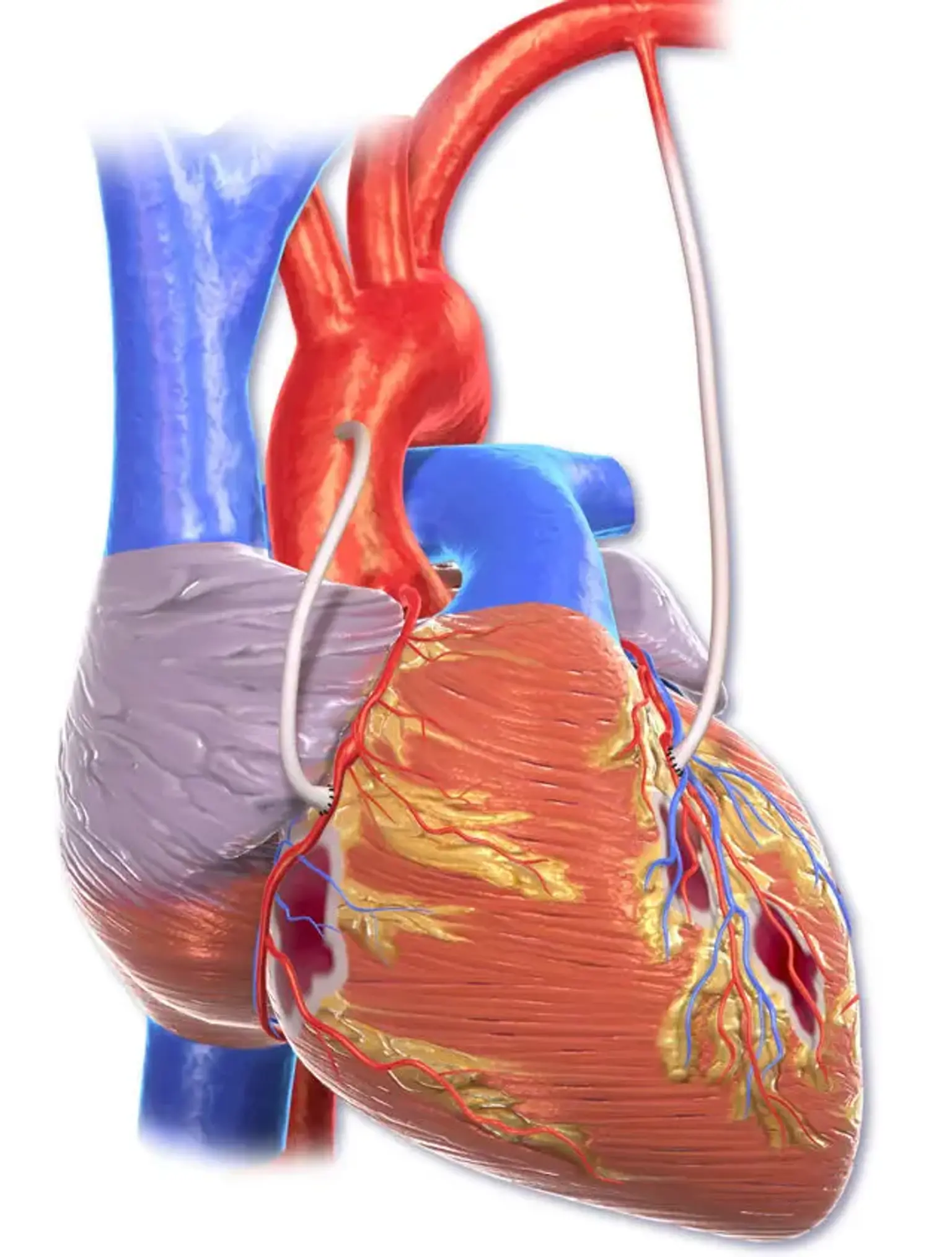
Koronar bypass-transplantat (CABG)
Överblick
CABG är ett signifikant kirurgiskt ingrepp där ateromatösa hinder i en patients kranskärl kringgås med hjälp av skördade venösa eller arteriella ledningar. Bypassen återställer blodflödet till det ischemiska myokardiet, återställer funktion och livskraft och lindrar anginala symtom.
Nästan 400 000 CABG-operationer genomförs varje år, vilket gör det till den mest regelbundet utförda större kirurgiska operationen; kirurgiska trender har dock förändrats eftersom alternativa val som medicinsk terapi och perkutan koronarintervention (PCI) har blivit mer populära.
CABG-kirurgi
Koronar bypass-ympning (CABG) är ett förfarande som används för att förbättra livskvaliteten och minimera hjärtrelaterad dödlighet hos individer med kranskärlssjukdom (CAD). CAD är den största dödsorsaken i USA och den industrialiserade världen och påverkar 16.5 miljoner amerikanska vuxna (20 år) varje år.
Det är ansvarigt för 530 989 dödsfall i USA varje år, och de långsiktiga konsekvenserna av CAD, inklusive som vänsterkammardysfunktion och hjärtsvikt, förväntas påverka nästan 8 miljoner personer över 18 år år 2030.
CABG-kirurgi utfördes först på 1960-talet med målet att ge symtomatisk lindring, förbättrad livskvalitet och förbättrad livslängd till CAD-patienter. Jämfört med medicinsk behandling ökade CABG överlevnaden hos individer med multivesselsjukdom och lämnade huvudsjukdomen på 1970-talet.
Det nya CAD-behandlingsparadigmet ber om ett hjärtteam-tillvägagångssätt där kardiologen och hjärtkirurgen utvärderar koronarangiografin tillsammans och ger patienten det bästa tillgängliga alternativet för koronar revaskularisering, oavsett om det är implantation av en perkutan koronar stent eller CABG. För närvarande är den genomsnittliga CABG-patienten äldre, har haft tidigare perkutan koronarintervention (PCI) och har mycket mer comorbiditeter.
Trots dessa risker är CABG fortfarande en av de viktigaste kirurgiska operationerna i modern medicinhistoria, efter att förmodligen ha räddat fler liv och erbjudit mer betydande symtomlindring än någon annan större operation. Nya minimalt invasiva tillvägagångssätt, genombrott inom anestesi- och intensivvårdsavdelning (ICU) och tekniska framsteg driver gränserna för denna operation till nya höjder.
I allmänhet finns det två typer av CABG-kirurgiska ingrepp: on-pump och off-pump, med skillnaden att en CABG på pumpen använder en kardiopulmonell bypass-krets och ett arresterat hjärta för att fungera. Den vänstra inre bröstartären (LIMA) och saphenösa ventransplantat (SVG) från nedre extremiteterna används vanligtvis som bypass-transplantatledningar.
Den högra inre bröstartären (RIMA), den radiella artären och den gastroepiploiska artären är några av de andra ledningarna som kan transplanteras. Transplantatens art och position bestäms av patientens anatomi och placeringen av de blockerade artärerna. LIMA ympas vanligtvis till den vänstra främre nedåtgående (LAD) artären, medan de andra ledningarna används för att komma åt de andra blockerade artärerna.
Anatomi och fysiologi
Två stora kranskärl levererar hjärtets myokardium: den vänstra kranskärlen och den högra kranskärlen (RCA). Den vänstra huvudkransartären är vanligtvis en kort sektion som delar sig i vänster främre nedåtgående (LAD) och cirkumflexartärer. LAD delar sig i diagonala grenar, medan circumflexartären delar sig i trubbiga marginalgrenar. RCA delar sig i två grenar: den bakre fallande artären (PDA) och de marginella grenarna.
Beroende på vilken artär som levererar interventrikulär septum och PDA kan koronarcirkulationen kategoriseras i vänsterdominerande, högerdominerande och samdominerande system. Den cirkumflexa artären levererar PDA i ett vänsterdominerande system, medan RCA levererar PDA i ett högerdominerande system. Med samdominant vaskulär tillförsel matas PDA av både RCA och circumflexartärerna samtidigt.
Blockeringar i någon av kranskärlen resulterar i en motsvarande brist i myokardiell perfusion, ischemi, och om de lämnas obehandlade kan det leda till permanent infarkt eller skada på hjärtat.
Historisk information
År 1912 tilldelades Alexis Carrel Nobelpriset i fysiologi och medicin för sitt arbete. Hans kunskap om förhållandet mellan angina pectoris och kranskärlsstenos gjorde det möjligt för honom att anastomosa ett halspulsådersegment från den fallande bröstkorgsaortan till vänster kranskärl i en hundmodell.
Arthur Vineberg, en anmärkningsvärd kanadensisk kirurg, transplanterade den vänstra inre bröstartären (bröst) direkt i myokardiet i den främre vänstra ventrikeln hos patienter med svår angina pectoralis i slutet av 1940-talet. Överraskande nog hade några individer betydande symtomreduktion som ett resultat av denna operation.
Sabiston genomförde den första planerade saphenösa venbypassproceduren för koronar revaskularisering vid Duke University 1962. Kolessov använde den vänstra inre bröstartären (bröstartären) för att kringgå den vänstra främre nedåtgående artären utan hjärt-lungräddning 1964, och Carpentier var banbrytande för användningen av radiella artärtransplantat som CABG-ledningar 1973.
CABG blomstrade som den enda behandlingen för CAD under 1970-talet och början av 1980-talet. Antalet CABG-operationer som gjordes minskade med utveckling, introduktion och utbredd användning av perkutan kranskärlsstenting på 1980- och 1990-talet. Flera multicenterstudier som jämför CABG med nuvarande stentbehandling har dock tydligt fastställt fördelarna med CABG, särskilt när specifika patientfunktioner som diabetes, multivessel CAD och ischemisk kardiomyopati ingår.
Indikationer för CABG
När det finns högkvalitativa blockeringar i någon av de viktigaste kranskärlen och / eller perkutan koronarintervention (PCI) har misslyckats med att eliminera blockeringarna, rekommenderas CABG ofta. Följande är klass 1-rekommendationerna från ACCF/AHA-riktlinjerna från 2011:
- Vänster huvudsjukdom större än 50%
- Trekärls kranskärlssjukdom på mer än 70% med eller utan proximal LAD-inblandning
- Tvåkärlssjukdom: LAD plus en annan större artär
- En svår stenos på mer än 70% hos en patient med betydande anginalsymtom trots maximal läkemedelsbehandling
- Hos en överlevande av plötslig hjärtdöd med ischemirelaterad ventrikulär takykardi var en kärlsjukdom mer än 70%.
Andra indikationer för CABG inkluderar följande:
- Inaktivera angina (klass I)
- Ischemi som kvarstår i samband med en icke-ST-segmenthöjning av hjärtinfarkt (NSTEMI) som är eldfast mot medicinsk behandling (klass I)
- Dålig vänster ventrikulär funktion, men livskraftig, icke-fungerande myokardium ovanför den anatomiska defekten som kan revaskulariseras.
- Kliniskt svår CAD med 70 procent eller högre stenos i ett eller flera kärl, samt eldfast kärlkramp trots läkemedelsbehandling och PCI
- Kliniskt svår CAD på 70% eller mer stenos i 1 eller flera kärl hos överlevande av plötsligt hjärtstopp som tros orsakas av ischemisk ventrikulär arytmi
- Kliniskt svår CAD med 50% eller mer stenos i 1 eller flera kärl hos patienter som genomgår hjärtkirurgi av andra skäl (t.ex. klaffbyte eller aortakirurgi)
CABG kan utföras som en akutbehandling i inställningen av en ST-segmenthöjning MI (STEMI) om perkutan koronarintervention (PCI) inte var möjlig eller om PCI misslyckades och det finns långvarig smärta och ischemi som påverkar en stor del av myokardiell trots medicinsk behandling.
Faktorer som ökar överlevnadsfördelen med CABG inkluderar följande:
- Vänster ventrikulär ejektionsfraktion på 45% eller mindre
- Diabetes mellitus
- Ischemisk mitral uppstötning
- PCI-fel, med eller utan akut felindikator (AMI)
Kontraindikationer
CABG rekommenderas inte för asymtomatiska individer som har låg risk för hjärtinfarkt eller dödsfall. Patienter som kommer att dra liten nytta av koronar revaskularisering är också uteslutna.
Även om högre ålder inte är en kontraindikation, bör CABG kontaktas med försiktighet hos äldre, särskilt de över 85 år. Dessa individer är också mer benägna att ha perioperativa problem efter CABG. Hos patienter med komplicerad CAD är en tvärvetenskaplig hjärtteammetod som betonar delat beslutsfattande avgörande för att ge patienten den bästa chansen till en framgångsrik revaskulariseringsplan.
CABG-förfarande
Förutom koronarangiografin som upptäckte kranskärlssjukdomen, kommer patienten att kräva olika tester som utförs som förberedelse för operationen. Laboratorietester såsom ett fullständigt blodtal (CBC), metaboliska paneler inklusive leverfunktionstester, koagulationspaneler och hemoglobin A1c kommer att krävas. Andra tester, inklusive som ett elektrokardiogram (EKG), ekokardiografi, karotisultraljud, röntgen i bröstet och kanske en CT-bröst- eller venkartläggning av underbenen, kan vara nödvändiga.
För att undvika arytmier som förmaksflimmer ges ofta preoperativa läkemedel som betablockerare under den perioperativa perioden. Tidigare hölls aspirin 5 till 7 dagar före operationen, men det föreslås nu att börja eller fortsätta preoperativt.
När patienten anländer till sjukhuset kommer intravenös åtkomst att upprättas och deras läkemedel och preoperativa tester kommer att undersökas. Hår kommer att tas bort från operationsplatserna och patienten kommer att få ett klorhexidinbad.
Utrustning
Denna betydande kirurgiska kirurgi kräver inte bara den utrustning som krävs för de flesta andra kirurgiska operationer, utan också flera specialiserade utrustningar, såsom en kardiopulmonell bypass-maskin med en värmekylare för att värma och kyla blodet.
Personal
Operationen utförs av ett specialiserat kardiovaskulärt kirurgiskt team med omfattande utbildning och erfarenhet av att ta hand om dessa komplexa patienter. Teamet består av kardiotorakisk kirurg och deras assistenter, anestesiologer, sjuksköterskor, kirurgiska tekniker och perfusionister
Riskbedömning
Riskmodeller för att förutsäga 30-dagars dödlighet efter isolerad CABG utvecklas. De vanligaste prediktorerna inom hjärtkirurgi är Euroscore-systemet och Society of Thoracic Surgeons (STS) 2008 Cardiac Surgery Risk Model. Ålder, tidigare MI, PVD, njursvikt, hemodynamisk status och EF är alla delade faktorer i dessa två enastående modeller. Åtta av de mest relevanta faktorerna, inklusive ålder, kirurgisk skärpa, reoperativ status, kreatininnivå, dialys, chock, kronisk lungsjukdom och EF, förklarar 78 procent av variationen i STS-modellen.
Premedicinering
Premedicinering syftar till att minska myokardiellt syrebehov genom att sänka hjärtfrekvensen och systemiskt arteriellt tryck, samt att öka myokardiellt blodflöde med hjälp av vasodilatatorer. Följande läkemedel ska tas fram till operationen:
- Betablockerare, kalciumkanalblockerare och nitrater
- Aspirin
Administrerade medel är följande:
- Temazepam omedelbart preoperativt
- Midazolam, en liten intravenös (IV) dos i operationssalen före artärlinjeinsättning
Varje patient ska få 2 enheter blod (för milda fall) eller 6 enheter blod, färskfryst plasma och blodplättar korsmatchade (för komplexa fall). Tranexamsyra (1-g bolus före kirurgiskt snitt, följt av en infusion på 400 mg/tim under operationen) kan övervägas för att minimera postoperativ mediastinal blödning och den mängd blodprodukter som behövs (dvs. röda blodkroppar och färskfryst plasma)
Anestesi
Hjärtkirurgi utförs oftast under djup generell anestesi med endotrakealt rör. Följande två typer av neuraxiell blockad används sällan som tillägg:
- Intratekal opioidinfusion
- Thorax epiduralanestesi (vanligtvis en lågdos lokalbedövnings-/opioidinfusion)
Teknik
Processen börjar efter att patienten är i operationssalen och är ansluten till standardmonitorer. Innan man inducerar generell anestesi kan en anestesiolog sätta in en arteriell linje för att övervaka patientens blodtryck invasivt. Efter induktion av generell anestesi och intubation av patienten kan en central linje för venös åtkomst och en lungartärkateter sättas in, följt av införandet av en transesofageal ekokardiografigivare.
Före det kirurgiska snittet förbereds och draperas patienten sterilt och en time-out administreras. Kirurgen utför en medial sternotomi för att förbereda sig för avlägsnande av LIMA för användning som ledning. En utbildad assistent, vanligtvis en läkarassistent, sjuksköterskans första assistent eller en annan kirurg, använder öppna eller videoassisterade procedurer för att ta bort den saphenösa venen från ett eller båda benen samtidigt.
Efter förvärvet av adekvata ledningar föreskriver kirurgen antikoagulation, oftast heparin, som ska administreras som förberedelse för kardiopulmonell bypass (CPB). Patientens aorta och hjärta är centralt kannulerade och slangen är ansluten till hjärt-lung-bypass-kretsen. Efter initieringen av CPB stoppas hjärtat med högkaliumkardioplegi så att kirurgen kan anastomosa de skördade ledningarna till kransartärerna som är avlägsna till hindren.
Som ledningar för kranskärlsbypasstransplantation kan antingen artärer eller vener användas (CABG). En nyckelpublikation från Cleveland Clinic bevisade överlevnadsfördelarna med att ympa den vänstra inre bröstartären (bröst) till den vänstra främre nedåtgående kransartären för många år sedan. Detta är fortfarande sant; Faktum är att om möjligt erbjuder bilateral intern bröstkorgstransplantation (bröst) en betydande långsiktig överlevnadsfördel. Starka bevis visar att användning av ett extra artärtransplantat snarare än ett venöst transplantat är relaterat till förbättrade långsiktiga resultat.
Den större saphenösa venen och i sällsynta fall den korta saphenösa venen är de mest regelbundet använda ventransplantaten, medan den inre bröstartären är den mest använda artärtransplantationen. Det radiella artärtransplantatet återinfördes i klinisk praxis på 1990-talet och fortsätter att visa höga patencyhastigheter på 80% eller mer efter 10 års uppföljning, särskilt om målvaskulär stenos var större än 90%.
Nackdelen med saphenösa ventransplantat är att deras patency minskar med tiden: 10-20% blockeras 1 år efter operationen på grund av tekniska misstag, trombos och intimal hyperplasi. Ytterligare 1-2 procent av ventransplantaten ockluderar varje år från 1 till 5 år efter operationen och ytterligare 4-5 procent ockluderar varje år från 6 till 10 år. Ocklusion av ventransplantat som inträffar ett eller flera år efter CABG orsakas av ventransplantat ateroskleros, vilket åtföljs av utvecklingen av neointimal hyperplasi.
Endast 50-60% av saphenösa ventransplantat är patent 10 år efter operationen, och endast hälften av dem är fria från angiografisk ateroskleros. Patienter bör ta livslång trombocythämmande medicin, oftast i form av daglig lågdos (81 mg) aspirin, som en del av korrekt sekundär profylax.
Interna bröstkorgsartärtransplantat, till skillnad från saphenösa ventransplantat, upprätthåller patency hela tiden. Mer än 90% av inre bröstkorgsartärtransplantat är fortfarande patent efter 10 år. När den vänstra främre kranskärlen kringgås, bör den vänstra inre bröstartären (bröst) användas som ledning.
Ledningarna är kopplade till ny ostia som genereras i den proximala aortan efter att kirurgen anastomoserar de distala delarna. Kardioplegi sköljs sedan bort, hjärtat börjar dra ihop sig och kirurgen kan undersöka transplantaten för blodflöde och kompetens samt blödning från anastomosställena. Bröstet stängs sedan med sternala ledningar och patienten flyttas till intensivvårdsavdelningen för hemodynamisk stabilitetsövervakning och extubation.
Komplikationer
Stroke, sårinfektion, transplantatsvikt, njursvikt, postoperativt förmaksflimmer och dödlighet är alla möjliga konsekvenser av CABG. Strokefrekvensen efter CABG har rapporterats variera mellan 1% och 2%, beroende på patientens egenskaper och riskfaktorer för stroke, som inkluderar hög ålder, tidigare stroke, aorta åderförkalkning, perifer artärsjukdom, perioperativ förmaksflimmer och diabetes.
Sternal sårinfektionshastigheter är cirka 1% och påverkas av riskvariabler som fetma, diabetes, kronisk obstruktiv lungsjukdom (KOL) och operationslängd.
Fel på ett saphenöst ventransplantat (SVG) är troligtvis inom 30 dagar efter operationen och orsakas av många orsaker som venstorlek och överdriven längd, distal avrinning och dåligt flöde och hyperkoagulerbarhet och trombos. Med upprepad angiografi efter CABG har frekvensen av SVG-fel så hög som 25% setts. Alternativt håller arteriella transplantat som den vänstra inre bröstartären (LIMA) och radiella arteriella transplantat längre och har patencyhastigheter som når 90% efter 10 år.
Postoperativ njursvikt efter CABG varierar från 2% till 3%, med 1% som behöver dialys. Preoperativ njursjukdom, ålderdom, diabetes, typ av operation, LV-dysfunktion och chock är alla riskfaktorer. Även om inga läkemedel definitivt har visat sig minska frekvensen av CABG-inducerat nedsatt njurfunktion, kan CABG utanför pumpen erbjuda en fördel jämfört med CABG på pumpen.
Förmaksflimmer inom de första 5 dagarna efter CABG är ganska frekvent, med frekvenser från 20% till 50%, och är kopplad till ökad sjuklighet, inklusive en större risk för embolisk stroke och död. Den mest effektiva strategin för att minimera förekomsten av postoperativt förmaksflimmer har visat sig vara preoperativ behandling med betablockerare och kanske amiodaron.
Risken för perioperativ dödlighet efter CABG varierar beroende på komorbiditeter, operationens brådska och fallvolymen på anläggningen där proceduren utförs, från 1% till 2%.
Resultat
Enligt en metaanalys av sex randomiserade kliniska prövningar med 6055 patienter från eran av arteriell ympning och stentning leder kranskärlsbypasstransplantation (CABG) till en minskning av långvarig dödlighet och hjärtinfarkt (MI) samt minskningar av upprepade revaskulariseringar hos patienter med multivessel kranskärlssjukdom, oavsett om patienterna är diabetiker eller inte.
En metaanalys av åtta randomiserade studier med 3612 vuxna patienter med diabetes och multivessel kranskärlssjukdom (CAD) fann att CABG sänkte risken för dödsfall av alla orsaker med 33% efter 5 år jämfört med PCI. När patienter som hade CABG jämfördes med undergrupper av patienter som fick antingen bare metal-stenter eller läkemedelseluerande stentar varierade den relativa riskminskningen inte nämnvärt.
Patienter i åldern 51 till 70 år och de äldre än 70 år som fick CABG inom samma tidsperiod klarade sig betydligt sämre när det gäller överlevnad. Kronisk njursjukdom, en låg ejektionsfraktion i vänster kammare, perifer kärlsjukdom eller kronisk obstruktiv lungsjukdom var de ledande riskfaktorerna för dödsfall av alla orsaker.
Den kirurgiska behandlingen för ischemisk hjärtsvikt (STICH) förlängningsstudie (STICHES) drog slutsatsen att dödsgraden av någon orsak, död av kardiovaskulära orsaker och död av någon orsak eller sjukhusvistelse för kardiovaskulära orsaker var signifikant lägre hos patienter som genomgick CABG och fick medicare.
Dessutom fanns det en betydande variation på sjukhusnivå i STEMI CABG-priser, och CABG gjordes ofta inom 1-3 dagar efter angiografi. Patienter som fick CABG och de som inte hade liknande dödstal på sjukhus.
En metaanalys av 6637 patienter med oskyddad vänster huvud-CAD från nio studier under en 14-årsperiod (2003-2016) fann att PCI med läkemedelseluerande stenter var associerad med jämförbar hjärt- och dödlighet av alla orsaker men minskade strokefrekvenser och högre frekvenser av upprepad revaskularisering. För signifikanta negativa hjärt- och cerebrovaskulära händelser uppnådde en trend som gynnade CABG vs PCI inte statistisk signifikans.
När det gäller livskvalitet efter CABG kontra PCI för multivessel CAD förbättrar båda procedurerna frekvensen av angina. Men vid 1 månad efter proceduren tenderar PCI-patienter att återhämta sig snabbare och ha bättre kortsiktig hälsostatus än CABG-patienter, men vid 6 månader och längre efterprocedur verkar CABG-patienter ha bättre anginalindring och livskvalitet än PCI-patienter.
Slutsats
Ett kranskärlsbypass-transplantat (CABG) är en kirurgisk teknik som används för att behandla kranskärlssjukdom med målet att förbättra livskvaliteten och sänka hjärtrelaterad dödlighet. Det omdirigerar blod runt trånga eller blockerade delar av huvudartärerna, vilket ökar blodflödet och syretillförseln till hjärtat.