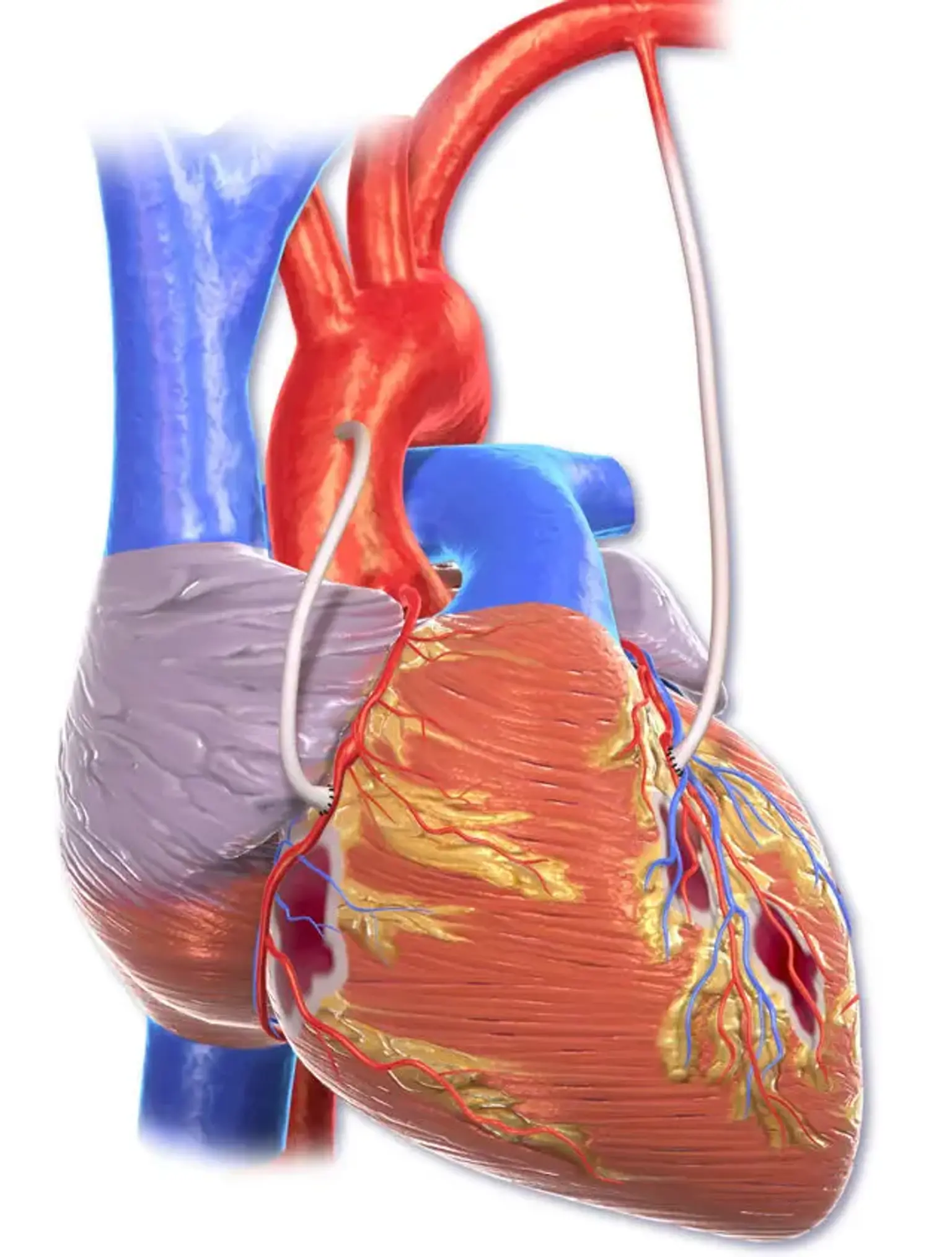
Аортокоронарне шунтування (АКШ)
Огляд
АКШ - це значна хірургічна процедура, при якій атероматозні обструкції в коронарних артеріях пацієнта обходять стороною за допомогою зібраних венозних або артеріальних каналів. Шунтування відновлює приплив крові до ішемічного міокарда, відновлюючи функцію і життєздатність і полегшуючи ангінальні симптоми.
Щороку проводиться майже 400 000 операцій АКШ, що робить його найбільш регулярно виконуваною великою хірургічною операцією; однак хірургічні тенденції змінилися, оскільки альтернативний вибір, такий як медикаментозна терапія та черезшкірне коронарне втручання (PCI), стали більш популярними.
Хірургія АКШ
Аортокоронарне шунтування (АКШ) - це процедура, яка використовується для підвищення якості життя та мінімізації смертності, пов'язаної з серцевими захворюваннями, у осіб з ішемічною хворобою серця (ІХС). САПР є найбільшою причиною смерті в Сполучених Штатах і промислово розвиненому світі, що вражає 16,5 мільйонів дорослих жителів США (у віці 20 років) щороку.
Він несе відповідальність за 530 989 летальних випадків у Сполучених Штатах щороку, а довгострокові наслідки ІХС, включаючи дисфункцію лівого шлуночка та серцеву недостатність, як очікується, торкнуться майже 8 мільйонів осіб у віці старше 18 років до 2030 року.
Хірургія CABG була вперше проведена в 1960-х роках з метою забезпечення симптоматичного полегшення, поліпшення якості життя та збільшення тривалості життя пацієнтів з ІХС. У порівнянні з медичним лікуванням, АКШ підвищив рівень виживання у осіб з багатоповерхівною хворобою і залишив основну хворобу до 1970-х років.
Нова парадигма лікування САПР вимагає підходу серцевої команди, в якому кардіолог і кардіохірург разом оцінюють коронарну ангіографію і надають пацієнту найкращу доступну альтернативу для коронарної реваскуляризації, будь то імплантація черезшкірного коронарного стента або АКШ. На даний момент середній пацієнт з АКШ є старшим, переніс попереднє черезшкірне коронарне втручання (PCI) і має набагато більше супутніх захворювань.
Незважаючи на ці ризики, CABG залишається однією з найважливіших хірургічних операцій в історії сучасної медицини, ймовірно, врятувавши більше життів і запропонувавши більш значне полегшення симптомів, ніж будь-яка інша велика операція. Нові малоінвазивні підходи, прориви в управлінні наркозом та відділенням інтенсивної терапії (ВІТ), а також технологічні досягнення висувають межі цієї операції на нові висоти.
Загалом, існує два типи хірургічних процедур CABG: увімкнення насоса та вимкнення насоса, з тією різницею, що CABG на насосі використовує для роботи схему штучного кровообігу та заарештоване серце. Ліва внутрішня молочна артерія (LIMA) та трансплантати підшкірних вен (SVG) з нижніх кінцівок зазвичай використовуються як шунтування трансплантатних каналів.
Права внутрішня молочна артерія (RIMA), променева артерія та гастроепіплоїчна артерія є деякими іншими каналами, які можна пересадити. Вид і положення трансплантатів визначаються анатомією пацієнта і розташуванням закупорених артерій. LIMA зазвичай прищеплюється до лівої передньої низхідної (LAD) артерії, тоді як інші канали використовуються для доступу до інших заблокованих артерій.
Анатомія і фізіологія
Дві великі коронарні артерії живлять міокард серця: ліву головну коронарну артерію і праву коронарну артерію (RCA). Ліва головна коронарна артерія, як правило, є коротким відділом, який ділиться на ліву передню низхідну (LAD) і циркумфлексну артерії. ЛАД ділиться на діагональні гілки, тоді як циркумфлексна артерія ділиться на тупі крайові гілки. RCA ділиться на дві гілки: задню низхідну артерію (КПК) і крайові гілки.
Залежно від того, яка артерія постачає міжшлуночкову перегородку і КПК, коронарний кровообіг можна класифікувати на ліво-домінантну, право-домінантну і ко-домінантну системи. Циркумфлексна артерія постачає КПК в ліво-домінантній системі, тоді як RCA постачає КПК в право-домінантній системі. При ко-домінантному судинному постачанні КПК живиться як RCA, так і циркумфлексними артеріями одночасно.
Закупорки в будь-якій з коронарних артерій призводять до відповідного дефіциту перфузії міокарда, ішемії, а при відсутності лікування можуть призвести до постійного інфаркту або пошкодження серця.
історичні відомості
У 1912 році Алексіс Каррель був удостоєний Нобелівської премії з фізіології і медицини за свої роботи. Його знання про взаємозв'язок між стенокардією стенокардії та стенозом коронарних артерій дозволили йому анастомізувати сегмент сонної артерії від низхідної грудної аорти до лівої коронарної артерії на собачій моделі.
Артур Вінеберг, відомий канадський хірург, пересадив ліву внутрішню грудну (молочну) артерію безпосередньо в міокард переднього лівого шлуночка у пацієнтів з важкою стенокардією в кінці 1940-х років. Дивно, але у кількох осіб в результаті цієї операції спостерігалося значне зменшення симптомів.
Сабістон провів першу заплановану процедуру шунтування підшкірних вен для коронарної реваскуляризації в Університеті Дьюка в 1962 році. У 1964 році Колессов використав ліву внутрішню грудну (молочну) артерію для обходу лівої передньої низхідної артерії без штучного кровообігу, а Карпентьє започаткував використання трансплантатів променевої артерії як каналів CABG у 1973 році.
CABG процвітав як єдине лікування САПР протягом 1970-х і початку 1980-х років. Кількість проведених операцій АКШ зменшилася з розвитком, впровадженням та широким впровадженням черезшкірного стентування коронарних артерій у 1980-х та 1990-х роках. Однак кілька багатоцентрових досліджень, що порівнюють АКШ з поточним лікуванням стентом, чітко встановили переваги АКШ, особливо коли включені специфічні особливості пацієнта, такі як діабет, багатосудинна ІХС та ішемічна кардіоміопатія.
Показання до застосування АКШ
Коли в будь-якій з основних коронарних артерій є повноцінні закупорки та/або черезшкірне коронарне втручання (PCI) не змогло усунути закупорки, часто рекомендується застосовувати АКШ. Нижче наведено рекомендації класу 1 з керівних принципів ACCF / AHA 2011 року:
- Основне захворювання лівого напрямку більше 50%
- Трисудинна ішемічна хвороба серця більше 70% з або без проксимального ураження ЛАД
- Захворювання двох судин: ЛАД плюс ще одна велика артерія
- Важкий стеноз більше 70% у пацієнта зі значними симптомами стенокардії, незважаючи на максимальне лікування ліками
- У тих, хто пережив раптову серцеву смерть з ішемією, пов'язаною з шлуночковою тахікардією, одне судинне захворювання становило понад 70%.
Інші показання до АКШ включають наступне:
- Інвалідизуюча стенокардія (I клас)
- Ішемія, яка зберігається в контексті інфаркту міокарда без сегмента ST (NSTEMI), який є рефрактерним до медикаментозного лікування (клас I)
- Погана функція лівого шлуночка, але життєздатна, нефункціонуюча міокарда вище анатомічного дефекту, який може бути реваскуляризований.
- Клінічно важка форма ІХС з 70 відсотками або вищим стенозом в одній або декількох судинах, а також рефрактерна стенокардія, незважаючи на медикаментозне лікування та PCI
- Клінічно важка ІХС 70% або більше стенозу в 1 або більше судинах у тих, хто пережив раптову зупинку серця, яка, як вважають, викликана ішемічною шлуночковою аритмією
- Клінічно важка ІХС з 50% і більше стенозом в 1 або більше судинах у пацієнтів, які перенесли кардіохірургічну операцію з інших причин (наприклад, заміна клапана або операція на аорті)
АКШ може бути проведена як невідкладна терапія в умовах елевації сегмента ST (STEMI), якщо черезшкірне коронарне втручання (PCI) було неможливим або якщо PCI не вдалося і спостерігається тривалий біль та ішемія, що впливають на значну частину міокарда, незважаючи на медикаментозну терапію.
Фактори, що підвищують користь АКШ від виживання, включають наступне:
- Фракція викиду лівого шлуночка 45% або менше
- Цукровий діабет
- Ішемічна мітральна регургітація
- Недостатність PCI, з гострим інфарктом міокарда або без нього (AMI)
Протипоказання
АКШ не рекомендується безсимптомним особам, які мають низький ризик інфаркту міокарда або смерті. Пацієнти, які мало отримають користі від коронарної реваскуляризації, також виключаються.
Хоча старший вік не є протипоказанням, до АКШ слід підходити з обережністю у людей похилого віку, особливо у віці старше 85 років. Ці особи також більш схильні до періопераційних проблем після АКШ. У пацієнтів зі складною ІХС мультидисциплінарний підхід кардіологічної команди, що підкреслює спільне прийняття рішень, має вирішальне значення для надання пацієнту найкращих шансів на успішний план реваскуляризації.
Процедура АКШ
Крім коронарної ангіографії, яка виявила ІХС, пацієнту будуть потрібні різні аналізи, проведені при підготовці до операції. Будуть потрібні лабораторні дослідження, такі як загальний аналіз крові (ЗАК), метаболічні панелі, включаючи печінкові тести, панелі згортання крові та гемоглобін A1c. Можуть знадобитися інші тести, в тому числі у вигляді електрокардіограми (ЕКГ), ехокардіографії, сонної ультрасонографії, рентгенографії грудної клітки і, можливо, КТ грудної клітки або вени, що відображає нижні кінцівки.
Щоб уникнути аритмій, таких як фібриляція передсердь, передопераційні препарати, такі як бета-блокатори, часто призначаються протягом періопераційного періоду. Раніше аспірин утримували за 5-7 днів до операції, але тепер його пропонують починати або продовжувати передопераційно.
Коли пацієнт прибуде до лікарні, буде встановлено внутрішньовенний доступ, а також будуть обстежені його медикаменти та передопераційні аналізи. Волосся буде видалено з місць операції, а пацієнту призначать ванночку з хлоргексидином.
Обладнання
Ця значна хірургічна операція вимагає не тільки обладнання, необхідного для більшості інших хірургічних операцій, але і декількох спеціалізованих одиниць обладнання, таких як апарат штучного кровообігу з нагрівачем-охолоджувачем для зігрівання і охолодження крові.
Персоналу
Операція проводиться спеціалізованою серцево-судинною хірургічною бригадою з великою підготовкою та досвідом догляду за цими складними пацієнтами. Команда складається з кардіоторакального хірурга та його асистентів, анестезіологів, медсестер, хірургічних техніків та перфузіоністів
Оцінка ризику
Розробляються моделі ризику для прогнозування 30-денної смертності після ізольованого АКШ. Найбільш часто використовуваними предикторами в кардіохірургії є система Euroscore і модель ризику кардіохірургії Товариства торакальних хірургів (STS) 2008 року. Вік, попередній інфаркт міокарда, ПСЗ, ниркова недостатність, гемодинамічний статус та ЕФ є спільними факторами в цих двох видатних моделях. Вісім найбільш релевантних факторів, включаючи вік, гостроту хірургічного втручання, реопераційний статус, рівень креатиніну, діаліз, шок, хронічне захворювання легенів та ЕФ, пояснюють 78 відсотків варіації моделі STS.
Премедикація
Премедикація спрямована на зниження потреб міокарда в кисні за рахунок зниження частоти серцевих скорочень і системного артеріального тиску, а також для збільшення кровотоку міокарда за допомогою судинорозширювальних засобів. До моменту операції слід приймати такі медикаменти:
- Бета-блокатори, блокатори кальцієвих каналів та нітрати
- Аспірин
Введені кошти наступні:
- Темазепам негайно передопераційно
- Мідазолам, мала внутрішньовенна (IV) доза в операційній перед введенням артеріальної лінії
Кожен пацієнт повинен отримати 2 одиниці крові (для легких випадків) або 6 одиниць крові, свіжозаморожену плазму і тромбоцити перехресно зіставлені (для складних випадків). Транексамова кислота (1-г болюс перед хірургічним розрізом, а потім інфузія 400 мг/год під час операції) може розглядатися для мінімізації післяопераційного крововиливу в середостіння та кількості необхідних препаратів крові (тобто еритроцитів та свіжозамороженої плазми)
Анестезія
Кардіохірургічні операції найчастіше проводяться під глибоким загальним наркозом за допомогою ендотрахеальної трубки. Наступні два типи нейроаксіальної блокади використовуються рідко в якості допоміжних засобів:
- Інтратекальна опіоїдна інфузія
- Грудна епідуральна анестезія (як правило, низька доза місцевого анестетика/опіоїдної інфузії)
Техніка
Процес починається після того, як пацієнт виявляється в операційній і підключається до стандартних моніторів. Перш ніж викликати загальний наркоз, анестезіолог може ввести артеріальну лінію для інвазивного моніторингу артеріального тиску пацієнта. Після індукції загальної анестезії та інтубації пацієнта може бути введена центральна лінія венозного доступу та катетер легеневої артерії з подальшим введенням трансезофагеального ехокардіографічного перетворювача.
Перед хірургічним розрізом пацієнта стерильно готують і драпірують, вводять тайм-аут. Хірург проводить медіальну стернотомію, щоб підготуватися до видалення ЛІМА для використання в якості трубопроводу. Навчений помічник, як правило, помічник лікаря, перший помічник медсестри або інший хірург, використовує відкриті або відео-допоміжні процедури для видалення підшкірної вени з однієї або обох ніг одночасно.
Після придбання адекватних каналів хірург призначає антикоагуляцію, найчастіше гепарин, для введення в рамках підготовки до штучного кровообігу (КФБ). Аорта і серце пацієнта централізовано канюльовані, а тюбінг підключений до ланцюга штучного кровообігу. Після початку CPB серце зупиняється при кардіоплегії з високим вмістом калію, щоб хірург міг анастомізувати зібрані канали до коронарних артерій, віддалених від обструкцій.
В якості каналів для аортокоронарного шунтування можуть використовуватися або артерії, або вени (АКШ). Ключова публікація з клініки Клівленда довела переваги виживання трансплантації лівої внутрішньої грудної (молочної залози) артерії до лівої передньої низхідної коронарної артерії багато років тому. Це все ще вірно; Насправді, якщо це можливо, двостороннє внутрішнє трансплантування грудної (молочної залози) артерії дає значну довгострокову користь для виживання. Вагомі докази показують, що використання додаткового трансплантата артерії, а не венозного трансплантата, пов'язане з поліпшенням довгострокових результатів.
Більша підшкірна вена і, в окремих випадках, коротка підшкірна вена вени є найбільш регулярно використовуваними трансплантатами вен, тоді як внутрішня грудна (молочна) артерія є найбільш часто використовуваною трансплантацією артерії. Трансплантат променевої артерії був знову введений в клінічну практику в 1990-х роках і продовжує демонструвати високі показники прохідності 80% і більше після 10 років спостереження, особливо якщо стеноз цільових судин був більше 90%.
Мінусом трансплантатів підшкірних вен є те, що їх прохідність з часом знижується: 10-20% блокуються через 1 рік після операції через технічні помилки, тромбозу, інтимальної гіперплазії. Ще 1-2 відсотки трансплантатів вен закупорюються щороку від 1 до 5 років після операції, а ще 4-5 відсотків оклюзуються щороку від 6 до 10 років. Оклюзія трансплантата вен, що виникає через один або кілька років після АКШ, викликається атеросклерозом трансплантата вен, який супроводжується розвитком неоінтимальної гіперплазії.
Лише 50-60% трансплантатів підшкірних вен запатентовані через 10 років після операції, і лише половина з них не має ангіографічного атеросклерозу. Пацієнти повинні приймати довічні антиагрегантні препарати, найчастіше у вигляді щоденних низьких доз (81 мг) аспірину, як частину належної вторинної профілактики.
Внутрішні грудні (молочні) трансплантати артерій, на відміну від трансплантатів підшкірних вен, зберігають прохідність протягом усього часу. Більше 90% трансплантатів внутрішніх грудних (молочних) артерій все ще патентуються через 10 років. При обході лівої передньої коронарної артерії в якості трубопроводу слід використовувати ліву внутрішню грудну (молочну) артерію.
Канали пов'язані з новими остіями, що утворюються в проксимальній аорті після того, як хірург анастомозирует дистальні частини. Потім кардіоплегія змивається, серце починає скорочуватися, і хірург може оглянути трансплантати на предмет кровотоку і компетентності, а також кровотечі з місць анастомозу. Потім грудну клітку закривають стернальними проводами, і пацієнта переміщують до відділення критичної допомоги для моніторингу гемодинамічної стабільності та екстубації.
Ускладнень
Інсульт, ранова інфекція, недостатність трансплантата, ниркова недостатність, післяопераційна фібриляція передсердь і смертність - все це можливі наслідки АКШ. Повідомляється, що частота інсульту після АКШ коливається від 1% до 2%, залежно від особливостей пацієнта та факторів ризику інсульту, які включають похилий вік, попередній інсульт, атеросклероз аорти, захворювання периферичних артерій, періопераційну фібриляцію передсердь та діабет.
Рівень інфекції стернальної рани становить близько 1% і на них впливають такі змінні ризику, як ожиріння, діабет, хронічне обструктивне захворювання легень (ХОЗЛ) та тривалість операції.
Недостатність трансплантата підшкірної вени (SVG), швидше за все, протягом 30 днів після операції і викликана численними причинами, такими як розмір вени і надмірна довжина, дистальний стік і поганий перебіг, а також гіперкоагуляція і тромбоз. При повторній ангіографії після АКШ спостерігалися показники збою SVG до 25%. Крім того, артеріальні трансплантати, такі як ліва внутрішня молочна артерія (LIMA) та променеві артеріальні трансплантати, зберігаються довше і мають показники прохідності, які досягають 90% через 10 років.
Показники післяопераційної ниркової недостатності після АКШ варіюються від 2% до 3%, при цьому 1% потребують діалізу. Передопераційні захворювання нирок, старість, діабет, тип операції, дисфункція ЛШ та шок - все це фактори ризику. Незважаючи на те, що жодні препарати, безумовно, не довели, що вони зменшують частоту ниркових порушень, викликаних АКШ, що не відкачуються, може запропонувати перевагу перед АКШ на насосі.
Миготлива аритмія протягом перших 5 днів після АКШ є досить частою, з показниками від 20% до 50%, і пов'язана з підвищеною захворюваністю, включаючи більший ризик емболічного інсульту та смерті. Доведено, що найбільш ефективною стратегією мінімізації частоти післяопераційної фібриляції передсердь є передопераційна терапія бета-блокаторами і, можливо, аміодароном.
Ризик періопераційної смертності після АКШ залежить від супутніх захворювань, терміновості операції та об'єму випадку, де проводиться процедура, коливається від 1% до 2%.
Результати
Згідно з мета-аналізом шести рандомізованих клінічних досліджень за участю 6055 пацієнтів епохи артеріальної пластики та стентування, аортокоронарне шунтування (АКШ) призводить до зниження довгострокової смертності та інфарктів міокарда (МІ), а також до зменшення повторних реваскуляризацій у пацієнтів з багатосудинною коронарною хворобою, незалежно від того, чи є пацієнти діабетичними чи ні.
Мета-аналіз восьми рандомізованих досліджень за участю 3612 дорослих пацієнтів з діабетом та багатосудинною ішемічною хворобою серця (ІХС) показав, що АКШ знизив ризик смерті з будь-яких причин на 33% через 5 років у порівнянні з PCI. Коли пацієнтів, які перенесли АКШ, порівнювали з підгрупами пацієнтів, які отримували або голі металеві стенти, або стенти, що вислизають від лікарських засобів, відносне зниження ризику суттєво не змінювалося.
Пацієнти у віці від 51 до 70 років і ті, хто старше 70 років, які отримували АКШ протягом того ж періоду часу, значно гірші з точки зору виживання. Хронічне захворювання нирок, низька фракція викиду лівого шлуночка, захворювання периферичних судин або хронічне обструктивне захворювання легень були провідними факторами ризику смерті з усіх причин.
Розширене дослідження хірургічного лікування ішемічної серцевої недостатності (STICH) (STICHES) дійшло висновку, що показники смертності від будь-якої причини, смерті від серцево-судинних причин та смерті від будь-якої причини або госпіталізації з серцево-судинних причин були значно нижчими у пацієнтів, які перенесли CABG та отримували медичну допомогу.
Крім того, спостерігалося значне відхилення показників STEMI CABG на рівні лікарні, і CABG часто робили протягом 1-3 днів після ангіографії. Пацієнти, які отримували АКШ, і ті, хто не мав подібних показників смертності в лікарні.
Мета-аналіз 6637 пацієнтів з незахищеною лівою основною ІХС з дев'яти досліджень за 14-річний період (2003-2016 рр.) показав, що PCI зі стентами, що вислизають від лікарських засобів, був пов'язаний з порівнянною смертністю серця та всіх причин, але зниженими показниками інсульту та більшими темпами повторної реваскуляризації. Для значних несприятливих серцевих та цереброваскулярних подій тенденція на користь CABG проти PCI не досягла статистичної значущості.
З точки зору якості життя після CABG проти PCI для багатосудинної САПР, обидві процедури покращують частоту стенокардії. Однак через 1 місяць після процедури пацієнти з PCI, як правило, швидше одужують і мають кращий короткочасний стан здоров'я, ніж пацієнти з АКШ, однак через 6 місяців і довше після процедури пацієнти з АКШ, як видається, мають краще полегшення стенокардії та якість життя, ніж пацієнти з PCI.
Висновок
Аортокоронарне шунтування (АКШ) - це хірургічна методика, яка використовується для лікування ішемічної хвороби серця з метою поліпшення якості життя та зниження смертності, пов'язаної з серцевою системою. Він перенаправляє кров навколо звужених або утруднених ділянок головних артерій, посилюючи кровотік і доставку кисню до серця.